2023届安徽省淮南市高三第一次模拟考试理综化学试题(原卷+解析版)
展开安徽省淮南市2023届高三第一次模拟考试
理科综合化学试题
注意事项:
1.答卷前,考生务必将自己的准考证、班级、姓名填写在答题卡上。
2.请将各题答案填在答题卡上。
3.可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cu-64
一、选择题:本题共7小题,每小题6分,共42分,在每小题给出的4个选项中,只有一个是符合题目要求的,把正确选项填写在答题卷上。
1. 化学在人类社会的可持续发展中发挥着重要作用。下列说法错误的是
A. 我国研制“超级钢”强度很大,在应用时实现了钢板的轻量化,这不仅节约材料,还可以降低能耗和减少环境污染等
B. 在规定范围内合理使用食品添加剂,对人体健康不会产生不良影响,甚至还可以补充某些必要的营养成分
C. 环境保护工程师的主要工作是预防和治理环境污染
D. 绿色化学也称环境友好化学,其核心思想就“先污染后治理”,利用化学原理和技术,消除有害化学物质
2. 下面甲、乙、丙、丁四个实验,实验现象和结论均正确的是
A. 装置甲中红布条均褪色,说明氯气具有漂白性
B. 装置乙中分别滴入酚酞,碳酸钠溶液呈红色,碳酸氢钠溶液呈浅红色,说明碳酸钠的水解程度大于碳酸氢钠
C. 装置丙用Cu与浓硫酸反应制取SO2,紫色石蕊、品红、酸性高锰酸钾均褪色,说明SO2具有酸性、漂白性和还原性
D. 装置丁中导管红墨水下降,说明铁丝发生吸氧腐蚀
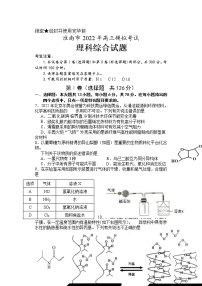
3. 20世纪40年代,传统法合成己二酸工艺就已成熟,一直沿用至今。2020年我国科学家利用8种酶采用“一锅催化法”高效绿色合成了己二酸,其流程如图:
下列说法错误的是
A. 温度越高,上述2种方法合成己二酸的速率越快
B. 传统法合成己二酸会产生大气污染物,原子利用率低
C. “一锅催化法”属于绿色化学工艺
D. 1mol己二酸与足量NaHCO3反应生成88gCO2
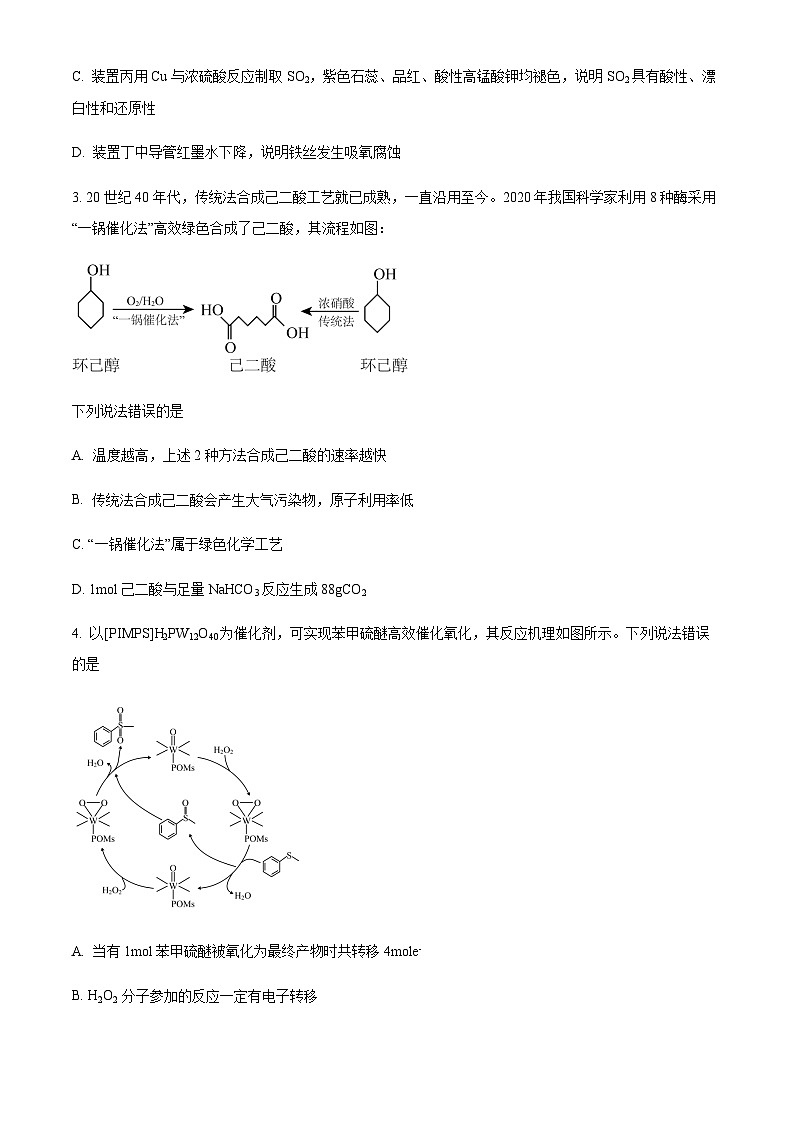
4. 以[PIMPS]H2PW12O40为催化剂,可实现苯甲硫醚高效催化氧化,其反应机理如图所示。下列说法错误的是
A. 当有1mol苯甲硫醚被氧化为最终产物时共转移4mole-
B. H2O2 分子参加的反应一定有电子转移
C. 苯甲硫醚的催化氧化最终生成 , 催化氧化过程中温度不宜过高
D. 催化剂中的-W=O部位与H2O2作用生成活性过氧物
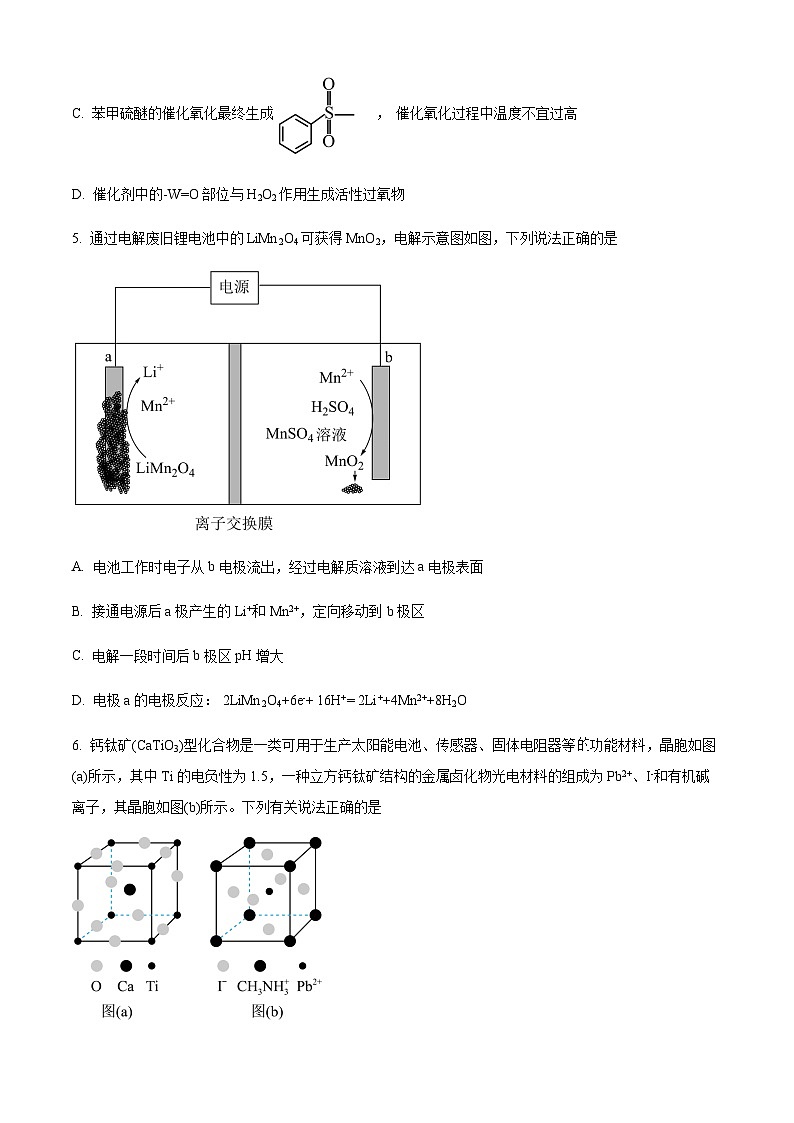
5. 通过电解废旧锂电池中的LiMn2O4可获得MnO2,电解示意图如图,下列说法正确的是
A. 电池工作时电子从b电极流出,经过电解质溶液到达a电极表面
B. 接通电源后a极产生的Li+和Mn2+,定向移动到b极区
C. 电解一段时间后b极区pH增大
D. 电极a的电极反应: 2LiMn2O4+6e-+ 16H+= 2Li++4Mn2++8H2O
6. 钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等功能材料,晶胞如图(a)所示,其中Ti的电负性为1.5,一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子,其晶胞如图(b)所示。下列有关说法正确的是
A. 基态Ti原子的核外电子排布式为1s22s22p63s23p64s23d2
B. TiF4、TiCl4、 TiBr4、 TiI4熔点依次升高
C. 用图(b) 晶胞中的金属卤化物光电材料制作的太阳能电池,在使用过程中产生单质铅和碘,会降低了器件效率和使用寿命。
D. 图(b)晶胞中Pb2+与图(a) 晶胞中Ca的空间位置相同
7. K2Cr2O7溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i)(aq) +H2O(1)2 (aq) K1=3.0×10-2(25℃)
(ii)(aq)(aq)+H+ (aq) K2=3.3×10-7(25℃);
25℃时,0.1 mol·L-1 K2Cr2O7溶液中随pH的变化关系如图所示,
下列说法正确的是
A. 加入少量K2Cr2O7固体,平衡时c2()与 c()的比值减小
B. c()+ 2c()+ c()= 0.1 mol/L
C. 当pH=9.0时,c()≈9.9× 10-4.2 mol/L
D. 若溶液pH减小,则 的值将增大
三、非选择题:共174分
8. 某化学实验小组为了探究氨气的性质设计了如下实验方案。
实验一:探究氨气的溶解性
氨气具有强刺激性气味,会污染空气。实验小组经过多次尝试,最终将氨气的制备、收集、检验和喷泉实验于一体,设计出如图装置。
(1)写出气体发生装置仪器A中产生氨气的方程式___________。
(2)仪器B的名称___________,为了保证喷泉实验的良好效果,B中可以放入的试剂___________。
(3)实验时,打开K2,关闭K3,打开K1,将注射器中的浓氨水注入A中开始制备和收集氨气。已知仪器C中放入的是滴有酚酞溶液的湿棉花,则仪器C的作用___________。在不拆除装置的前提下,引发喷泉的操作是___________。
实验二:探究氨气的还原性
已知: Cu2O 呈红色固体,在酸性溶液中不稳定: Cu2O+ H2SO4=Cu+CuSO4+ H2O。
(4)装置G用于制备氨气,仪器的链接顺序为e,f接___________、___________、___________、___________ 、___________ 、___________接i,________,装置H的作用___________。实验开始前应先通一段时间的N2,其目的是___________。
(5)反应结束后装置F中的氧化铜完全反应生成红色固体,为了探究红色固体的成分,进行了如下实验:取15.6g红色固体于烧杯中,加入足量稀硫酸充分搅拌、静置、过滤、洗涤、干燥、称重,得固体9.6g,则红色固体的成分及其物质的量为___________。
9. 锌的用途广泛,主要用于镀锌板及精密铸造等行业。以粗氧化锌(主要成分为ZnO及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的工艺流程如图所示:
已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH3)4]2+、[Cu(NH3)4]2+进入溶液:
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中≤2.0×10-6
回答下列问题:
(1)“滤渣1”的主要成分为Fe(OH)3、Mn(OH)2和___________(填化学式),“ 操作3”的名称为___________。
(2)“氧化除锰”时,H2O2将Mn2+转化为难溶的MnO2,该反应的离子方程式为___________。
(3)“沉淀除铜”时,锌的最终回收率、除铜效果[除铜效果以反应后溶液中铜锌比表示] 与“(NH4)2 S加入量”[以表示]的关系曲线如图所示。
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是___________(用离子方程式表示),该反应的平衡常数为___________。(已知) [ Zn(NH3)4]2+的=2. 9 ×109]
②“沉淀除铜”时(NH4 )2S加入量最好应选___________。
a.100% b.110% c.120% d.130%
(4)电解后溶液中的溶质主要成分是___________, 可用于循环使用。
10. 甲烷既是一种清洁能源,又是基础化工原料,在生产生活和科学研究中具有极其重要的作用。
(1)通过以下反应可获得新型能源二甲醚(CH3OCH3)
①CO(g)+H2O(g)=CO2(g)+H2(g) ΔH1 = a kJ·mol -1
②CO2(g)+3H2(g)=CH3OH(g)+ H2O(g) ΔH2 = b kJ·mol -1
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=c kJ·mol -1
反应2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的ΔH=___________ kJ·mol -1 (用含a、b、c的式子表示)
(2)已知: 2H2O(g)+CH4(g) CO2(g)+4H2(g)的平衡常数()与反应温度(t)之间的关系如图所示。
某研究小组,在温度t下,向容积为2L的抽空的密闭容器中通入0.02 mol CO2和0.08 mol H2,10 min后反应平衡,测得容器中c(H2O)=0.01 mol/L。
①则0~10 min内CH4的反应速率v=___________H2的转化率α=___________。
②反应温度t约为___________℃。
③在该条件下测定平衡体系的压强为 300 kPa,则该反应的标准平衡常数 =___________。(已知:对于反应dD(g)+eE(g) gG(g)+hH(g),,其中 =100kPa, PG、PH、PD、PE为各组分的平衡分压)。
(3)科学家们已经用甲烷制出了金刚石,人造金刚石在硬度上与天然金刚石几乎没有差别,请根据下图金刚石结构模型及晶胞,回答问题:
①1个金刚石晶胞中所含碳原子数为___________, 已知原子a、b的分数坐标为(0,0,0)和(0,, ), 原子c的分数坐标为___________。
②若碳原子半径为r nm,则金刚石晶胞的密度为___________g/cm3(用含r的计算式表示)。
11. 瑞替加滨(K)具有潜在的神经保护作用,它可以永久性减少大脑中动脉闭塞的梗死面积,可以逆转单侧颈动脉闭塞导致的功能缺失,可以治疗癫痫病。以下是K的两条合成路线图:
(1)A→B的反应类型为___________。
(2)ClCOOCH2CH3的化学名称是___________。
(3)K的结构简式___________。
(4)写出G→H的反应方程式___________。
(5)I分子中氮原子的杂化轨道类型为___________。
(6)J中的含氧官能团的名称是___________。
(7)路线图中设计F→G和H→I目的是___________。
(8)请写出满足下列条件的F的所有同分异构体___________。
①能与新制的氢氧化铜悬浊液反应产生砖红色沉淀
②碱性条件下能水解,酸化后得产物之一遇FeCl3溶液显色
③核磁共振氢谱显示峰面积之比为:1:2:2:3:4。
安徽省A10联盟2018届高三最后一卷理综化学试题(图片版): 这是一份安徽省A10联盟2018届高三最后一卷理综化学试题(图片版),文件包含安徽省A10联盟2018届高三最后一卷理综化学试题图片版1doc、安徽省A10联盟2018届高三最后一卷理综化学试题图片版doc、A10最后一卷理综·化学答案1pdf、A10最后一卷理综·化学答案pdf等4份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。
安徽省A10联盟2018届高三最后一卷理综化学试题(word版): 这是一份安徽省A10联盟2018届高三最后一卷理综化学试题(word版),共10页。
【解析版】安徽省A10联盟2018届高三最后一卷理综化学试题: 这是一份【解析版】安徽省A10联盟2018届高三最后一卷理综化学试题,共19页。试卷主要包含了 下列说法正确的是, 常温下,现有0, a 等内容,欢迎下载使用。