

2023届天津市耀华中学高三下学期5月模拟考试化学试卷含答案
展开
这是一份2023届天津市耀华中学高三下学期5月模拟考试化学试卷含答案,共14页。试卷主要包含了 他非诺喹是一种抗疟疾新药等内容,欢迎下载使用。
天津市耀华中学 2023 届高三年级5月模拟考试化学试卷本试卷分为第Ⅰ卷(选择题) 和第Ⅱ卷(非选择题) 两部分, 共 100 分, 考试时间 60 分钟。第Ⅰ卷 1 至 5 页,第Ⅱ卷 5 至 10 页。答卷前, 考生务必将姓名、班级、考号填在答题卡上。答卷时, 考生务必将答案 涂写在答题卡上, 答在试卷上的无效。考试结束后,将答题卡交回。祝各位考生考试顺利!以下数据可供解题时参考:相对原子质量: H-1 C-12 N-14 O-16 Al-27第 Ⅰ卷(共 36 分)注意事项:1. 每题选出答案后,用铅笔将答题卡对应题目的答案标号涂黑。如需改动,用橡皮 擦干净后,再选涂其他答案标号。2. 本卷共 12 题, 每题 3 分, 共 36 分。在每题给出的四个选项中,只有一项是最符 合题目要求的。1.实现中国梦, 离不开化学与科技的发展, 下列有关说法错误的是A .我国“天眼”的球面射电板上使用的铝合金板属于金属材料B .华为公司自主研发的“麒麟 9000”芯片的主要成分是单质硅C .新能源汽车电池使用的石墨烯电极材料属于有机高分子化合物D .“神舟十四号”宇宙飞船返回舱表层材料中的玻璃纤维属于无机非金属材料2 . 我国发布了《医用同位素中长期发展规划(2021-2035 年)》,对提升医用同位素相关产 业能力水平、保障健康中国战略实施具有重要意义。医用同位素有 14C 、18F 、 131I、 60Co 等,有关说法错误的是A .60Co 位于元素周期表的第四周期第 VIII 族B .18F 和 131I 的最外层电子数相同C .14C 与 12C 的化学性质几乎相同D .化合物 23Na18F 的中子总数为 41
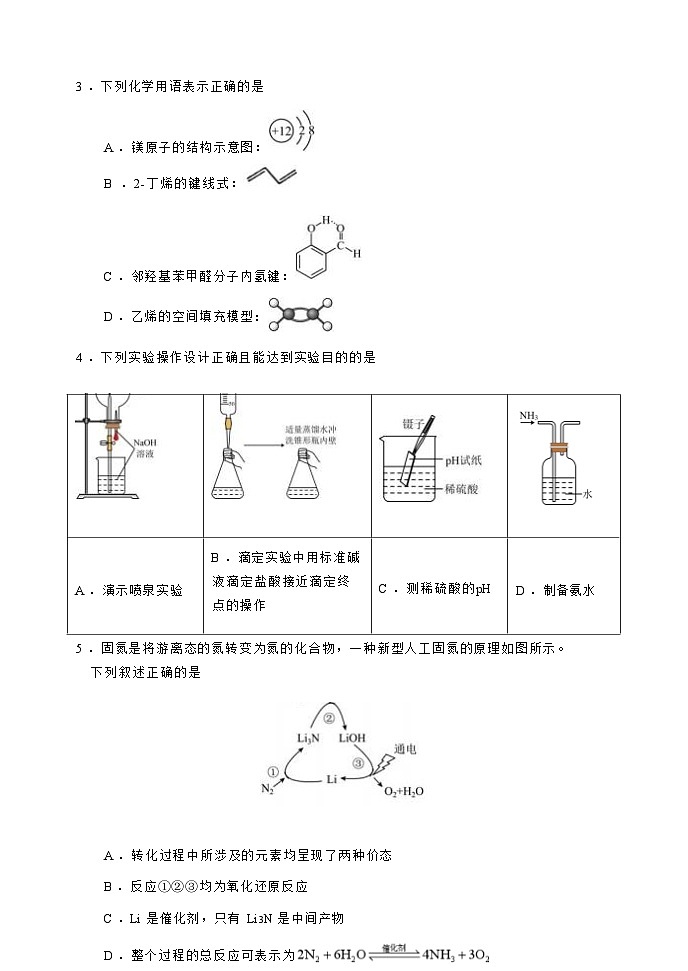
3 .下列化学用语表示正确的是A .镁原子的结构示意图: B .2-丁烯的键线式:C .邻羟基苯甲醛分子内氢键:D .乙烯的空间填充模型: 4 .下列实验操作设计正确且能达到实验目的的是 A .演示喷泉实验B .滴定实验中用标准碱 液滴定盐酸接近滴定终 点的操作 C .测稀硫酸的pH D .制备氨水5 .固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。 下列叙述正确的是A .转化过程中所涉及的元素均呈现了两种价态B .反应①②③均为氧化还原反应C .Li 是催化剂,只有 Li3N 是中间产物D .整个过程的总反应可表示为
6 .室温下,经指定操作后,下列各组溶液中的离子还能大量共存的是A .通入足量 SO2 :K+ 、Fe3+ 、Cl- 、NO3-B .通入适量 CO2 :Ca2+ 、Na+ 、Cl- 、I-C .通入足量 HCl :Mg2+ 、K+ 、MnO4- 、SO42-D .通入足量 NH3 :Cu2+ 、Na+ 、SO42- 、NO3-7 .类比法是一种学习化学的重要方法,下列类比法结论错误的是A .NF3 的空间结构为三角锥形,则PCl3 的空间结构也为三角锥形B .乙炔的分子结构为直线形,则HCN的分子结构也为直线形C .酸性强于 ,则可推出酸性强于D .NaCl固体与浓硫酸共热可制HCl ,则NaI固体与浓硫酸共热可制HI8 . 以下元素为短周期元素,其原子半径及主要化合价见下表。 元素XYZWT原子半径/nm0. 1520. 1860.0660. 1020.099最外层电子数11667下列有关说法正确的是A .简单离子的半径:Y>Z>XB .气态氢化物的热稳定性:W>ZC .Y 与 Z 形成的化合物可能具有强氧化性D .常温下,W 单质的分子间作用力小于 T 单质9 .NA 为阿伏加德罗常数的值,下列说法正确的是A .2.8g CO和N2 的混合气体中含有的孤电子对数为 0.2NAB .中键的个数为 10NAC .22.4L SO2溶于水,溶液中H2 SO3 、HSO3 - 、SO32-的数目总和为NAD .葡萄糖与新制的Cu(OH)2 反应生成 1molCu2O ,转移电子数为NA
10.近期科学家研发出了一种新型铝电池,电极分别为铝和硒,熔盐电解质由氯化钠、 氯化钾和氯化铝组成,如图所示。其中电池放电过程中会形成 AlnCl3n+ 1- ,放电总反 应为 2Al+3Se=Al2Se3 (该物质难溶于熔盐) 。下列说法错误的是A .充电时,电极 Al 为阴极B .放电时,Al 电极附近的阴离子浓度降低C .放电时,电路中每转移 1mol 电子,理论上正极质量增加 9gD .充电时,阳极的电极反应式为(n- 1) Al - 3(n- 1)e-+ (3n+ 1) AlCl4 -= 4AlnCl3n+ 1-11.已知 Ag2SO4 的 Ksp 为 2×10-5 ,将适量 Ag2SO4 固体溶于 100mL 水中至刚好饱和,该 过程中 Ag+和 SO42-浓度随时间变化关系如图。若 t1 时刻在上述体系中加入 100mL 0.02mol ·L- 1Na2 SO4 溶液,下列示意图中能正确表示 t1 时刻后 Ag+和 SO42-浓度随时间 变化趋势的是
12.难溶物 SrF2 可溶于盐酸。常温下,用HCl调节SrF2 浊液的pH,测得在不同pH条件下, 体系中(X为或)与的关系如图所示。下列说法正确的是A .代表与的变化曲线B .a 、c两点的溶液中均存在C .的数量级为D .c点的溶液中存在第Ⅱ卷 (共 64 分)注意事项:1. 用黑色墨水的钢笔或签字笔将答案写在答题卡上。2. 本卷共 4 题,共 64 分。13.(14 分)I .已知氯化钠的晶胞如下图所示。( 1)下列关于氯化钠的说法正确的是_____________。A .基态 Na+ 的电子有 5 种空间运动状态B .钠是第一电离能最大的碱金属元素C .氯原子的价电子排布式可写成 [Ne]3s23p5D .每个氯离子周围与它最近且等距的氯离子有 12 个
(2)已知 NaCl 的密度为ρg· cm-3 ,NaCl 的摩尔质量为 M g/mol ,阿伏加德罗常数的值为 NA ,则在 NaCl 晶体里 Na+和 Cl- 的最短距离为_______pm。II.过氧化氢(H2O2)是重要的化工产品,广泛应用于绿色化学合成、医疗消毒等领域。 已知:H2O2(l) H+(aq)+HO2-(aq) K=2.24×10- 12 (25℃)完成下列填空:(3)氧原子核外电子能级数为 ,H2O2 的电子式 。 对 H2O2 分子结构,有以下两种推测:要确定 H2O2 分子结构,需要测定 H2O2 分子中的_______ 。(选填序号)a. H—O 键长 b. O—O 键长 c. H—O—O 键角 d. H—O 、O—O 键能(4) 25oC ,pH(H2O2) ______pH(H2O) (选填“>” 、“<”或“=”) 。研究表明,H2O2 溶液中 HO2-浓度越大,H2O2 的分解速率越快。某温度下,经过相同时间,不同浓度 H2O2 分解率 与 pH 的关系如图所示。一定浓度的 H2O2 ,pH 增大 H2O2 分解率增大的原因是 。相同 pH 下,H2O2 浓度越大 H2O2 分解率越低的原因是 。(5) 蓝色的 CrO5 遇 H2O2 会褪色,此反应可用于检验 H2O2 ,配平下列方程式: ___CrO5+___H2O2+___H+=___Cr3++___O2 ↑+___H2O。
14.(18 分) 他非诺喹是一种抗疟疾新药。其中间体 K 的合成路线如下(部分条件已省略) 已知:|| || || ||① R1 COR2 R3 CH2 COR4—ⅰ.C2H5ONa R1 C|C HCOR4R2 OH R ② || || |5 6 7 2 5 7 6( 1) A 可以与NaHCO3 溶液反应放出 CO2 ,A 中官能团为_______________。 (2 ) E F 的反应类型为___________________。(3) B D 的化学方程式为___________________________________。(4) X 是 D 的同分异构体,符合下列条件的 X 的结构简式是_______________。①1molX 能与足量银氨溶液生成 4molAg②X 中核磁共振氢谱中出现 3 组吸收峰,峰面积比为 1 ∶ 1 ∶3(5) 一种由G 制备 H 的电化学方法:在 H2SO4 和 CH3OH 混合水溶液中加入 G ,通电。 G H 电极反应为___________________________。(6) 由 J 生成 K 可以看作三步反应,如图所示。J 的分子式为 ,P 中有两个六元环结构。Q 的结构简式为_______。
(7) 根据已有知识并结合相关信息,写出以环己醇、乙醇为原料合成的合成路线(其余试剂任选) 。已知:15.( 18 分)已知甲酸铜是一种重要的化工原料,常温常压下稳定,可溶于水,难溶于乙 醇,具有还原性,某实验小组在实验室用废铜屑制备甲酸铜晶体CuHCOO2 4H2 O ,实验流程如下: 回答下列问题:( 1) 若甲同学设计方案:铜屑、稀硫酸加热通入氧气制得硫酸铜溶液,再与甲酸反应生成 甲酸铜溶液,再结晶。请判断: 甲同学_______(填“能”或“不能”)制得甲酸铜晶体。(2) 步骤Ⅱ制备CuOH2 CuCO3 时,写出 CuSO4 和 NaHCO3 物质的量之比为 1 :2 时的离子方程式: 。(3) 操作步骤Ⅲ:向盛CuOH2 CuCO3 烧杯中加入一定量热蒸馏水,逐滴加入甲酸至固体恰好全部溶解,然后除去少量不溶性杂质,过程中为了防止甲酸铜结晶损失,可 采取___________操作;接着冷却结晶,过滤,再洗涤晶体2~3 次,为使固体快速干 燥,可选___________(填写序号)来洗涤。得到产品。A .冷水 B .乙醇 C .四氯化碳 D .饱和甲酸铜溶液
(4) 晶体中甲酸根含量的测定: 1 下列仪器可供步骤A 选用的是___________(写名称,下同);可供步骤C 中滴定选 用的是___________。 2 溶液恒温 80℃30min 时应采取的操作方法是___________ ,步骤 C 滴定时当观察 到___________ 即达到滴定终点。③ 计算晶体中甲酸根的质量分数为___________。16.( 14 分) 溴代烷的制备,分“氧化”和“溴化”两个过程,回答下列问题。( 1) 氧化过程:HBr(g)与 O2(g)在合适温度下制备 Br2(g),已知:T°C 时,相关物质的相对能量如下表所示: 物质HBr(g)O2(g)H2O(g)Br2(g)相对能量/ x y z w此温度下,在恒容密闭容器中充入 4mol HBr(g)和 1mol O2(g) ,测得反应物的平衡 转化率为 60%。若保持其他条件不变,改为绝热状态,平衡时, 测得放出热量为 Q kJ, 则下列关系正确的是_______(填标号)。
(2) 溴化过程:在 T °C 下,向 10 L 容器中投入初始浓度均为 0. 1的 Br2(g) 和 CH4(g) ,发生反应: 。保持温度不变,压缩容器体积,分别测得不同容积下 CH3Br(g)的平衡浓度如下表: 容器体积 V/L10V03 V0V0 m 0.09 0.25当容器体积从 10 V0 L 缩小到 3 V0 L 时,测得此时容器内仍有四种气态组分,则 m=_______ ;容器体积缩小到 V0 L 时,平衡_______移动(填“正向” 、“逆向”或“不”)。T °C 时,此反应在容积为 10 V0L 和 V0L 时化学平衡常数分别为 、 ,则_______(填“大于” 、“小于”或“等于”)。(3)新工艺可将甲烃、HBr 和 O2 混合,直接催化“氧化溴化”: 。反应起始物料 n(CH4) 、n(HBr) 、n(O2)分别为 2mol 、2mol 、1mol 时,在不同条件下 达到平衡,设体系中 CH3Br 的物质的量分数为 x(CH3Br),在 T 为 500°C 下的 x(CH3Br)~p 、在 p 为 3×105Pa 下的 x(CH3Br)~T 如图所示。 1 图中 a 点对应的反应条件为_________ ,此时用各物质平衡分压表示的平衡常数Kp= Pa- 1 (列计算式,某气体分压=总压×该气体的物质的量百分数)② b 点对应的甲烷转化率_______(保留三位有效数字)。
相关试卷
这是一份天津市耀华中学2023届高三下学期第二次模拟考试化学试题(含解析),共19页。试卷主要包含了单选题,结构与性质,有机推断题,实验题,原理综合题等内容,欢迎下载使用。
这是一份天津市耀华中学2023届高三下学期第二次模拟考试化学试题(无答案),共8页。试卷主要包含了下列图示错误的是,已知,下列离子方程式正确的是等内容,欢迎下载使用。
这是一份2023届天津市耀华中学高三下学期5月模拟考试化学试卷PDF版含答案,共12页。









