化学九年级下册第二节 几种常见的酸练习
展开
这是一份化学九年级下册第二节 几种常见的酸练习,共4页。试卷主要包含了下列对盐酸的叙述正确的是,某些植物的花汁可作为酸碱指示剂等内容,欢迎下载使用。
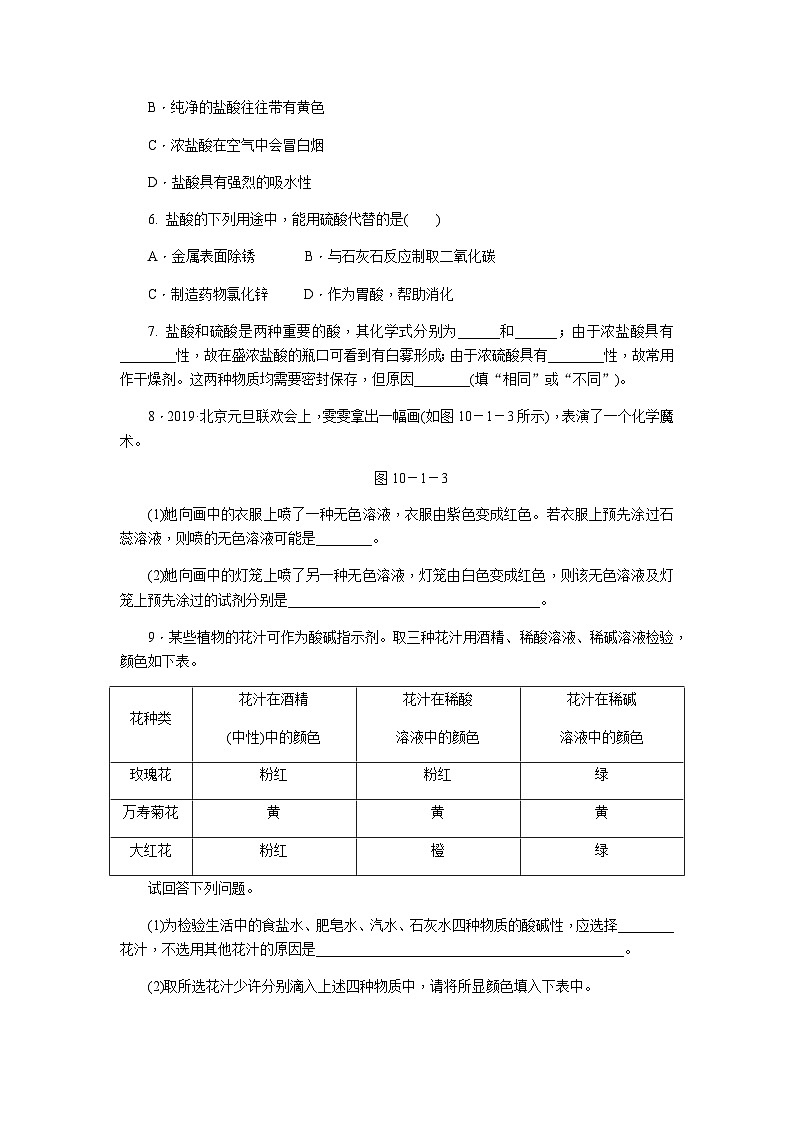
第1课时 酸碱指示剂 几种常见的酸知识点 1 对常见酸和碱的认识1.根据下列物质的名称和化学式,判断该物质是酸还是碱,填写在横线上。①盐酸(HCl)________;②硫酸(H2SO4)________;③碳酸(H2CO3)________;④氢氧化钠(NaOH)________;⑤氢氧化钙[Ca(OH)2]________;⑥氨水(NH3·H2O)________。2.下列常见生活物品中不含酸性物质的是( )图10-1-1知识点 2 酸、碱与指示剂的作用3.分别将石蕊溶液和酚酞溶液滴入如图10-1-2所示的溶液中,下列说法错误的是( )图10-1-2A.在白醋和苹果汁中石蕊变红,酚酞不变色B.在石灰水和氢氧化钠溶液中石蕊变蓝,酚酞变红C.石蕊和酚酞是常用的酸碱指示剂D.实验说明指示剂能使酸或碱的溶液改变颜色4.紫甘蓝汁在酸性溶液中会变红,在碱性溶液中会变绿,故紫甘蓝汁______(填“能”或“不能”)用作酸碱指示剂。将紫甘蓝汁分别加入盐酸和石灰水中,溶液变为________色的是盐酸,变为________色的是石灰水。知识点 3 盐酸和硫酸的物理性质和用途5.下列对盐酸的叙述正确的是( )A.盐酸是氯化氢气体的水溶液B.纯净的盐酸往往带有黄色C.浓盐酸在空气中会冒白烟D.盐酸具有强烈的吸水性6. 盐酸的下列用途中,能用硫酸代替的是( )A.金属表面除锈 B.与石灰石反应制取二氧化碳C.制造药物氯化锌 D.作为胃酸,帮助消化7. 盐酸和硫酸是两种重要的酸,其化学式分别为______和______;由于浓盐酸具有________性,故在盛浓盐酸的瓶口可看到有白雾形成;由于浓硫酸具有________性,故常用作干燥剂。这两种物质均需要密封保存,但原因________(填“相同”或“不同”)。8.2019·北京元旦联欢会上,雯雯拿出一幅画(如图10-1-3所示),表演了一个化学魔术。图10-1-3(1)她向画中的衣服上喷了一种无色溶液,衣服由紫色变成红色。若衣服上预先涂过石蕊溶液,则喷的无色溶液可能是________。(2)她向画中的灯笼上喷了另一种无色溶液,灯笼由白色变成红色,则该无色溶液及灯笼上预先涂过的试剂分别是____________________________________。9.某些植物的花汁可作为酸碱指示剂。取三种花汁用酒精、稀酸溶液、稀碱溶液检验,颜色如下表。花种类花汁在酒精(中性)中的颜色花汁在稀酸溶液中的颜色花汁在稀碱溶液中的颜色玫瑰花粉红粉红绿万寿菊花黄黄黄大红花粉红橙绿试回答下列问题。(1)为检验生活中的食盐水、肥皂水、汽水、石灰水四种物质的酸碱性,应选择________花汁,不选用其他花汁的原因是____________________________________________。(2)取所选花汁少许分别滴入上述四种物质中,请将所显颜色填入下表中。检验物质食盐水肥皂水汽水石灰水所显颜色 10.用Y形管或Y形导管完成如图10-1-4所示实验。图10-1-4(1)图甲中Y形管左侧管中加入无色酚酞溶液,右侧管中加入浓氨水,一段时间后,可观察到的现象是__________________________,用分子的观点解释这一现象:________________________________________________________________________。(2)图乙中Y形导管平放于桌面,实验中可观察到的现象是______________________________________________________________________,用化学方程式解释原因:_________________________________;若把Y形导管固定在铁架台上(如图丙),a管位于上方,b管位于下方,两石蕊试纸均为湿润的,可观察到b管中试纸变色比a管中明显,原因是________________________________________________。11.73 g质量分数为20%的盐酸与足量大理石反应,生成二氧化碳的质量是多少?12.2019·北京节选如图10-1-5所示,在白色点滴板1~6的孔穴中,分别滴加2滴紫色石蕊溶液。图10-1-5(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显________(填“酸性”或“碱性”)。(2)溶液变为红色的孔穴有________(填孔穴序号,下同)。(3)作为空白对照实验的孔穴是________。详解详析1.①酸 ②酸 ③酸 ④碱 ⑤碱 ⑥碱2.D3.D [解析] 指示剂与酸或碱溶液混合后,颜色发生改变的是指示剂,而不是酸或碱。4.能 红 绿5.A [解析] 纯净的盐酸是无色的;浓盐酸在空气中会形成白雾而不是白烟;盐酸具有挥发性,不具有吸水性。6.A7.HCl H2SO4 挥发 吸水 不同[解析] 浓盐酸因为易挥发,所以需要密封保存;浓硫酸因为易吸水,所以需要密封保存。8.(1)稀盐酸(无色的酸性溶液都可以)(2)酚酞溶液和石灰水(其他合理答案也可)9.(1)大红花 玫瑰花花汁鉴别不出酸性和中性溶液,而万寿菊花花汁则不能鉴别酸性、碱性和中性溶液 (2)粉红 绿 橙 绿10.(1)无色酚酞溶液变为红色 分子是不断运动的(2)湿润的紫色石蕊试纸变红,干燥的紫色石蕊试纸无明显变化 H2O+CO2===H2CO3 二氧化碳的密度比空气的大,主要从b管中通过11.解:73 g质量分数为20%的盐酸中溶质的质量为73 g×20%=14.6 g。设14.6 g HCl与足量大理石反应,生成二氧化碳的质量为x。CaCO3+2HCl===CaCl2+CO2↑+H2O 73 44 14.6 g x= x=8.8 g答:生成二氧化碳的质量为8.8 g。12.(1)碱性 (2)2、5 (3)3
相关试卷
这是一份初中化学北京课改版九年级下册第11章 酸与碱第二节 几种常见的酸同步练习题,共14页。试卷主要包含了选择题,判断题,综合应用题等内容,欢迎下载使用。
这是一份初中化学北京课改版九年级下册第二节 几种常见的酸练习,共13页。试卷主要包含了选择题,判断题,综合应用题等内容,欢迎下载使用。
这是一份初中化学北京课改版九年级下册第二节 几种常见的酸课时训练,共15页。试卷主要包含了选择题,判断题,科学探究题,综合应用题等内容,欢迎下载使用。