

广东省广州市天河区2022-2023学年高二下学期期末考试化学试题(无答案)
展开
这是一份广东省广州市天河区2022-2023学年高二下学期期末考试化学试题(无答案),共9页。试卷主要包含了实验是化学研究的一种重要手段,尿素又称碳酰胺,其合成原理为等内容,欢迎下载使用。
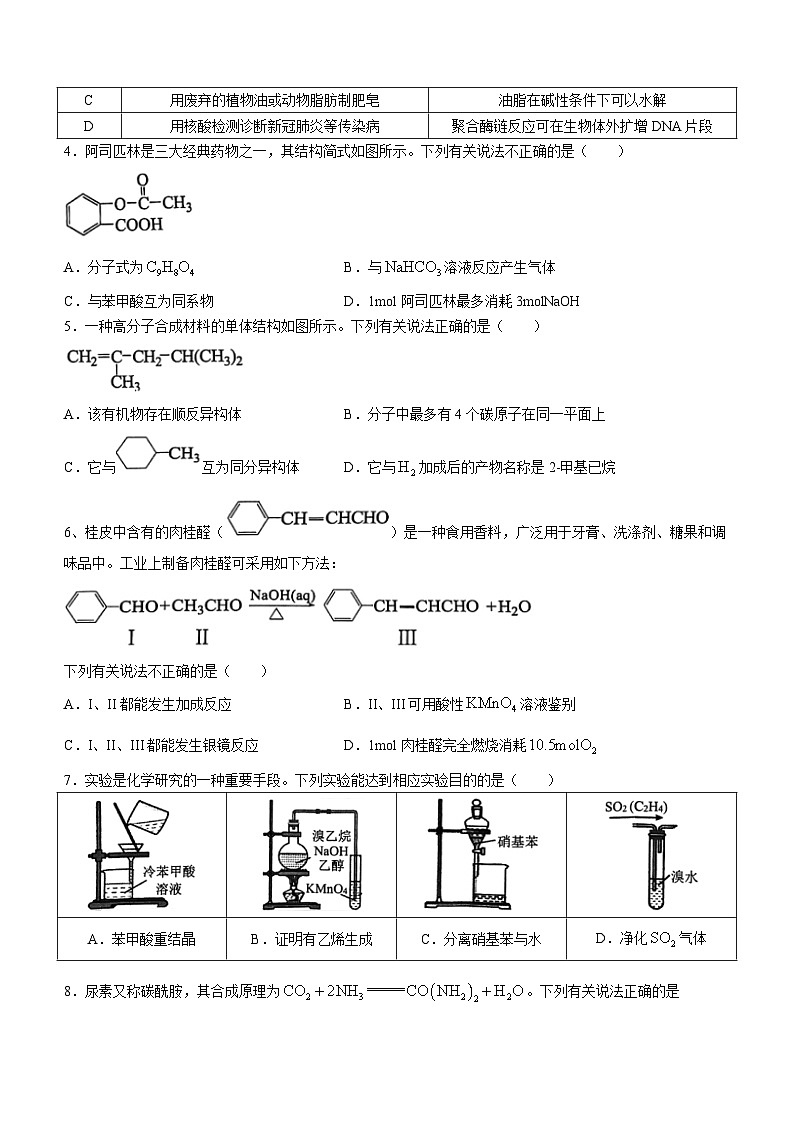
2022学年第二学期天河区期末考试高二化学本试卷共8页,满分为100分,考试用时75分钟。注意事项:1.答卷前,考生必须用黑色字迹的钢笔或签字笔将自己的学校、姓名、班级、座位号和考生号填写在答题卡相应的位置上,再用2B铅笔把考号的对应数字涂黑。2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案;不能答在试卷上。3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔或涂改液。不按以上要求作答的答案无效。4.考生必须保证答题卡的整洁,考试结束后,将试卷和答题卡一并交回。可能用到的相对原子质量:H:1 C:12 O:16 Li:7 Cl:35.5 Mn:55 Cu:64 Br:80一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。1.我国文化遗产众多,下图是北宋名画“千里江山图”的局部色彩。下列关于色彩所用颜料的化学成分不正确的是( )A.水墨底:炭黑B.赭石红:C.石绿:D.石青:2.北京冬奥会成功举办、“天宫课堂”授课、神舟十五号载人飞船发射成功以及“C919”飞机翱翔蓝天等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是( )A.冬奥会“飞扬”火炬所用的燃料为氧化性气体B.“天宫课堂”中用到的乙酸钠过饱和溶液显酸性C.载人飞船的太阳能电池能将化学能转化为电能D.“C919”机身使用的碳纤维属于新型无机非金属材料3.劳动开创未来。下列劳动项目与所述的化学知识没有关联的是( )选项劳动项目化学知识A用秸秆生产燃料乙醇淀粉水解产生葡萄糖B用波尔多液防治农作物灾害重金属离子可使蛋白质变性C用废弃的植物油或动物脂肪制肥皂油脂在碱性条件下可以水解D用核酸检测诊断新冠肺炎等传染病聚合酶链反应可在生物体外扩增DNA片段4.阿司匹林是三大经典药物之一,其结构简式如图所示。下列有关说法不正确的是( )A.分子式为 B.与溶液反应产生气体C.与苯甲酸互为同系物 D.1mol阿司匹林最多消耗3molNaOH5.一种高分子合成材料的单体结构如图所示。下列有关说法正确的是( )A.该有机物存在顺反异构体 B.分子中最多有4个碳原子在同一平面上C.它与互为同分异构体 D.它与加成后的产物名称是2-甲基已烷6、桂皮中含有的肉桂醛()是一种食用香料,广泛用于牙膏、洗涤剂、糖果和调味品中。工业上制备肉桂醛可采用如下方法:下列有关说法不正确的是( )A.I、II都能发生加成反应 B.II、III可用酸性溶液鉴别C.I、II、III都能发生银镜反应 D.1mol肉桂醛完全燃烧消耗7.实验是化学研究的一种重要手段。下列实验能达到相应实验目的的是( )A.苯甲酸重结晶B.证明有乙烯生成C.分离硝基苯与水D.净化气体8.尿素又称碳酰胺,其合成原理为。下列有关说法正确的是( )A.是含有极性键的极性分子 B.第一电离能C.分子中N原子采取杂化 D.尿素分子与水分子间可形成氢键,尿素易溶于水9.向盛有溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色的透明溶液。下列有关说法不正确的是( )A.难溶物为B.深蓝色透明溶液中加入乙醇会析出晶体C.深蓝色透明溶液含有配离子D.中为配体,配位数为410.图像可以直观地表示两个科学量之间的关系。下列图像正确的是( )ABCD11.为阿伏加德罗常数的值。下列说法正确的是( )A.含有的电子数为B.4.2g乙烯与丙烯的混合气体含碳原子数为C.标准状况下,所含分子数为D.与在光照条件下完全反应生成2molHCl12.丙烯与HBr发生加成反应的机理及反应体系中的能量变化如图所示。下列说法不正确的是( )A.曲线a表示反应2的能量变化 B.反应1和反应2都是放热反应C.反应1和反应2的决速步骤都是第1步 D.相同条件下反应2的速率比反应1大13.近期,我国科学家提出了一种双极膜硝酸盐还原工艺,原理如图。双极膜中间层中的解离为和,在外加直流电场作用下分别向两极迁移。下列说法不正确的是( )A.m是B.b接电源正极C.产生的与的物质的量之比为4:5D.左室电极反应为14.一种麻醉剂的分子结构式如图所示。其中,X、Y、Z、W、E为原子序数依次增大的短周期元素,元素E的原子比W原子多8个电子。下列说法不正确的是( )A.XEZ是一种强氧化性弱酸 B.电负性:C.原子半径:Y>Z>W>X D.该分子中所有原子均满足8电子稳定结构15.磷锡青铜合金广泛用于仪器仪表中的耐磨零件和抗磁元件等,其晶胞结构如图所示。下列说法不正确的是( )A.基态P原子的价层电子轨道表示式B.磷锡青铜合金具有各向异性的特点C.磷锡青铜合金的化学式为D.该晶胞中与Sn原子最近且等距离的Cu原子有12个16.常温下,向某浓度的溶液中逐滴加入某浓度的KOH溶液,测得溶液中、、三种微粒的物质的量分数与溶液pH的关系如图所示。下列说法不正确的是( )A.曲线1代表,曲线3代表B.的第一步电离常数C.KHA溶液呈碱性D.时,溶液中二、非选择题:本题共4小题,共56分。17.(14分)1,2-二溴乙烷可制造杀虫剂、药品等,也是有机合成的重要中间体。实验室用乙醇和浓硫酸反应制乙烯(含少量、),再用溴与之反应生成1,2-二滇乙烷。实验中用到下列仪器(短接口或橡皮管均已略去),回答下列问题:(1)气体流向从左到右:将B插入A①中,D接A②,A③接C,接________接________接________。(2)A中温度计水银球的位置________,若用分液漏斗代替装置D,可能会产生的问题是________。(3)加热三颈烧瓶前,先将E与其前面连接装置断开,再加热,待温度升到约120℃时,连接E与其前面装置,并迅速升温至160~180℃,从D中慢慢滴加乙醇-浓硫酸混合液,保持乙烯气体均匀地通入装有3.20mL液溴和3mL水的E试管,直至反应结束。①加热三颈烧瓶前将E与其前面连接装置断开的目的是________。②判断反应结束的现象是________。(4)将粗产品通过以下操作提纯得到1,2-二溴乙烷。a.水洗涤b.氢氧化钠溶液洗涤c.过滤d.用无水氯化钙干燥e.蒸馏收集129~133℃馏分,最后得到7.896g1,2-二溴乙烷。①粗品提纯的顺序是a→b→a→________(填序号)。②1,2-二溴乙烷的产率为________。(5)检验溴乙烷中含有溴元素,通常采用的实验方法与现象是:取少量溴乙烷于试管中,加入NaOH溶液并加热,静置冷却后,________。18.(14分)工业上可用低品位锰矿(主要成分,含Fe、Al、Ni、Pb等元素的杂质)与废硫酸亚铁制备高纯,其工艺流程和煅烧时的条件如图所示。物质MnSPbSNiS25℃时溶度积常数(1)“焙烧”时,将低品位锰矿和废硫酸亚铁粉碎后填入焙烧炉内,同时鼓入大量空气使粉末呈沸腾状,目的是________,反应中的氧化剂是________。(2)“除铝”的离子方程是________。(3)“除重金属”是除去溶液中极少量的和,若溶液中,则和完全除尽时,需控制物质的量浓度的范围是________,实际操作中很难控制,可以用________(填化学式)代替BaS。(4)“沉锰”的化学反应方程式是________,“煅烧”时应采取的条件是________。(5)基态Mn原子的价层电子排布式是________,锰的化合物是一种锂电池材料,其晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为apm,则晶体密度为________。19.(14分)近年来我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”,将转化为高附加值化学品成为科学家研究的重要课题。I.催化和生产甲醇。① ② (1)已知: ,则________。(2)已知:反应①的正反应速率可表示为,逆反应速率可表示为,其中、为速率常数。图中能够代表的曲线为________(填“”,“”、“”或“”)。(3)对于上述反应体系,下列说法正确的是________。A.增大的浓度,反应①、②的正反应速率均增加,逆反应速率均减小B.恒容密闭容器中气体密度不变时,反应达到平衡状态C.加入催化剂,的平衡转化率不变D.温度为时,反应①的化学平衡常数(4)不同条件下,按照投料,的平衡转化率如图所示。①压强、、由大到小的顺序是________,压强为时,温度高于570℃之后,随着温度升高平衡转化率增大的原因是________。②图中点,此时压强为0.1MPa,的选择性为(选择性:转化的中生成占整个转化的的百分比)。则该温度时反应①的平衡常数________(分压=总压物质的量分数)。II.电化学法还原制乙烯在强酸性溶液中通入,用情性电极进行电解可制得乙烯。其原理如图所示:(5)阴极电极反应式为________。20.(14分)苯氧乙酸()是一种重要的化工原料和制药中间体,有关苯氧乙酸衍生物的合成路线如下。回答下列有关问题:已知:①②(1)试剂所含官能团的名称为________。(2)A→B的反应类型为________,C的核磁共振氢谱图上峰的组数为________。(3)B→C的化学方程式为________。(4)D的分子式为________,,E的结构式为________。(5)化合物B的芳香族同分异构体中,同时满足如下条件的有________种,写出其中任意一种的结构简式________。a.苯环上只有两个取代基; b.能与新制反应,产生砖红色沉淀;c.与发生显色反应; d.最多能与2倍物质的量的NaOH反应;。(6)结合题中已知信息,设计由苯酚和乙醇为起始原料制备苯氧乙酸的合成路线(无机试剂任选)。
相关试卷
这是一份2022-2023学年广东省广州市天河区高二(下)期末化学试卷(含详细答案解析),共24页。试卷主要包含了单选题,流程题,实验题,简答题等内容,欢迎下载使用。
这是一份广东省广州市天河区2022-2023学年高二下学期期末考试化学试题(解析版),共37页。试卷主要包含了5 Mn, 劳动开创未来, 实验是化学研究的一种重要手段, 尿素又称碳酰胺,其合成原理为等内容,欢迎下载使用。
这是一份精品解析:广东省广州市天河区2021-2022学年高二下学期期末化学试题(解析版),共20页。试卷主要包含了5 Br-80,2ml,标况下对应气体体积为4, 下列实验操作或装置不正确的是等内容,欢迎下载使用。









