




还剩8页未读,
继续阅读
成套系列资料,整套一键下载
2023九年级化学下册第十单元酸和碱课题2酸和碱的中和反应第2课时溶液酸碱度的表示方法__pH课件新版新人教版
展开
这是一份2023九年级化学下册第十单元酸和碱课题2酸和碱的中和反应第2课时溶液酸碱度的表示方法__pH课件新版新人教版,共15页。
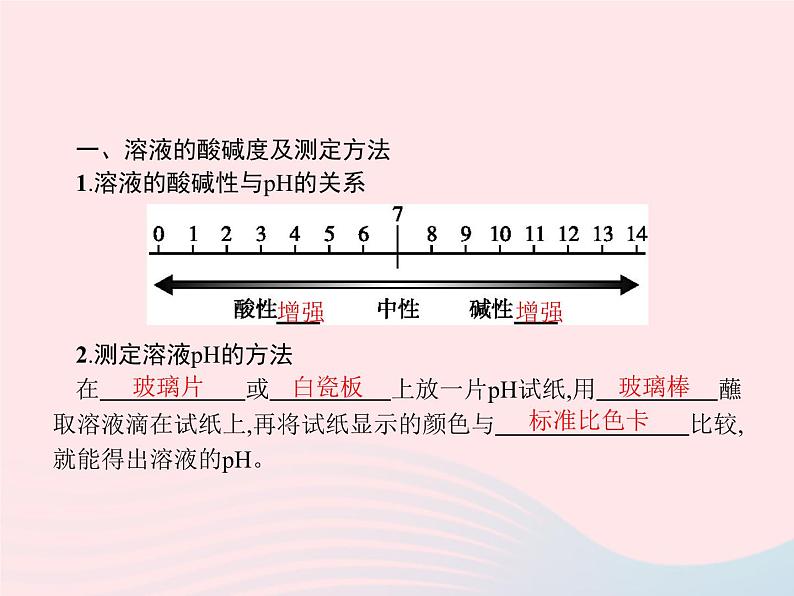
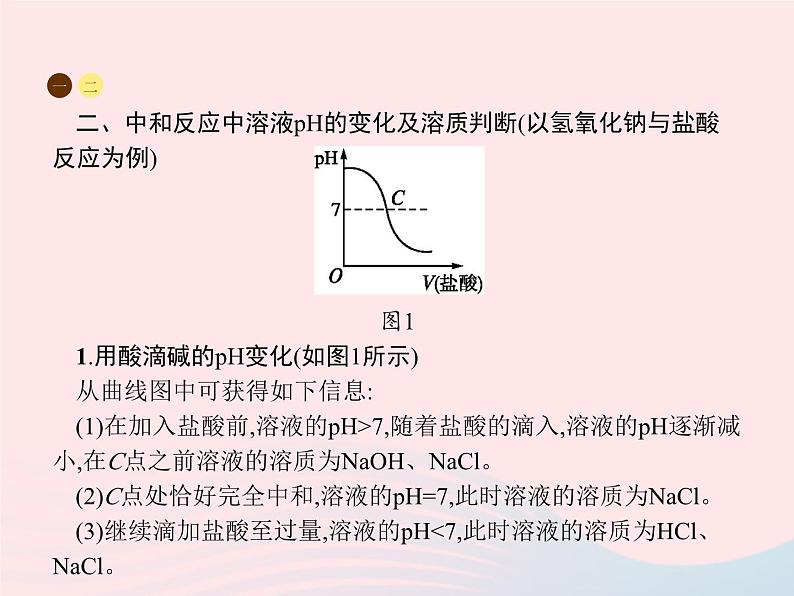
第2课时 溶液酸碱度的表示方法 ——pH一、溶液的酸碱度及测定方法1.溶液的酸碱性与pH的关系2.测定溶液pH的方法在 或 上放一片pH试纸,用 蘸取溶液滴在试纸上,再将试纸显示的颜色与 比较,就能得出溶液的pH。 增强增强玻璃片 白瓷板 玻璃棒 标准比色卡 二、了解溶液酸碱性的意义1.化工生产中要控制pH范围。2.农作物适宜在pH为 或接近 的土壤中生长。 3.测定雨水的pH,正常雨水pH约为 ,pH小于5.6的雨水为 。 4.测定人体内或排出液体的pH,可以帮助人们了解身体健康状况。7 7 5.6 酸雨 一、正确使用pH试纸需注意的问题1.试纸不可直接伸入溶液,以免污染溶液。2.测定溶液的pH时,试纸不可事先用蒸馏水润湿,因为润湿试纸相当于稀释被检验的溶液,这会导致测量不准确。若该溶液为酸性溶液,则pH偏高;若该溶液为碱性溶液,则pH偏低。3.取出试纸后,应将盛放试纸的容器盖严,以免被实验室的一些药品污染。一二【例题1】 某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )A.用湿润的pH试纸测定稀硫酸的pHB.用干燥的pH试纸测定二氧化碳气体的pHC.用干燥的pH试纸测定浓硫酸的pHD.用干燥的pH试纸测定氢氧化钠稀溶液的pH解析:答案:D 一二一二二、中和反应中溶液pH的变化及溶质判断(以氢氧化钠与盐酸反应为例)图11.用酸滴碱的pH变化(如图1所示)从曲线图中可获得如下信息:(1)在加入盐酸前,溶液的pH>7,随着盐酸的滴入,溶液的pH逐渐减小,在C点之前溶液的溶质为NaOH、NaCl。(2)C点处恰好完全中和,溶液的pH=7,此时溶液的溶质为NaCl。(3)继续滴加盐酸至过量,溶液的pH<7,此时溶液的溶质为HCl、NaCl。一二2.用碱滴酸的pH变化(如图2所示)从曲线图中可获得如下信息:(1)在加入氢氧化钠溶液前,溶液的pH<7,随着氢氧化钠溶液的滴入,溶液的pH逐渐增大,在C点之前溶液的溶质为HCl、NaCl。(2)C点处恰好完全中和,溶液的pH=7,此时溶液的溶质为NaCl。(3)继续滴加氢氧化钠溶液至过量,溶液的pH>7,此时溶液的溶质为NaOH、NaCl。一二【例题2】某校化学兴趣小组利用数字化传感器探究稀盐酸与氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示,下列说法正确的是( )A.图中A点所示溶液中,含有的溶质是NaCl和NaOHB.由A点到B点的pH变化过程证明酸与碱发生了中和反应C.向图中C点所示溶液中滴加无色酚酞,溶液不变色D.该实验是将盐酸逐滴滴入盛有氢氧化钠溶液的烧杯中一二解析:A点时溶液的pH小于7,溶液显酸性,说明稀盐酸有剩余,所得溶液中的溶质为HCl和NaCl,A错误;由A点到B点的pH变化过程,图像中pH的变化是从小于7逐渐增大到等于7,溶液由酸性变为中性,说明酸与碱发生了中和反应,B正确;C点时溶液的pH大于7,溶液显碱性,能使酚酞溶液变红色,C错误;图像中pH的变化是从小于7逐渐增大到大于7,可知原溶液显酸性,然后不断地加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,D错误。答案:B123456 答案1.人体内一些液体的正常pH范围如下,其中呈酸性的是( )A.血浆7.35~7.45 B.胃液0.9~1.5C.胆汁7.1~7.3 D.胰液7.5~8.01234562.下表是生活中几种常见物质的pH,其中能使无色酚酞溶液变红的是( ) 答案解析1234563.有A、B、C三种溶液,A能使紫色石蕊溶液变红,B能使无色酚酞溶液变红,C遇紫色石蕊溶液和无色酚酞溶液均无变化,则三种溶液的pH由大到小的顺序是( )A.A>C>B B.C>B>AC.B>A>C D.B>C>A 答案1234564.今有①肥皂水 ②食盐水 ③杨梅汁 ④白糖水⑤蒸馏水五种液体,根据你的生活经验判断,其中pH<7的是 ; pH>7的是 (填序号)。 答案5.下图表示身边一些物质的pH,看图回答下列问题: (1)农作物一般适宜在pH为 或接近 的土壤中生长。 (2)正常雨水pH为5.6,是因为溶有CO2,某市所降雨水pH为4.9,此雨可称为 。 123456 答案1234566.某植物的花瓣汁液(以下简称:X汁液)呈紫色,X汁液分别滴加到盛有下列溶液的试管中有如下现象:(1)据上表推测,X汁液 (填“能”或“不能”)作酸碱指示剂。 (2)将X汁液滴入肥皂水中溶液呈绿色,则肥皂水显 (填“酸”“碱”或“中”)性,pH (填“>”“<”或“=”)7。 (3)粗略测定雨水的酸碱度可使用 。 答案
第2课时 溶液酸碱度的表示方法 ——pH一、溶液的酸碱度及测定方法1.溶液的酸碱性与pH的关系2.测定溶液pH的方法在 或 上放一片pH试纸,用 蘸取溶液滴在试纸上,再将试纸显示的颜色与 比较,就能得出溶液的pH。 增强增强玻璃片 白瓷板 玻璃棒 标准比色卡 二、了解溶液酸碱性的意义1.化工生产中要控制pH范围。2.农作物适宜在pH为 或接近 的土壤中生长。 3.测定雨水的pH,正常雨水pH约为 ,pH小于5.6的雨水为 。 4.测定人体内或排出液体的pH,可以帮助人们了解身体健康状况。7 7 5.6 酸雨 一、正确使用pH试纸需注意的问题1.试纸不可直接伸入溶液,以免污染溶液。2.测定溶液的pH时,试纸不可事先用蒸馏水润湿,因为润湿试纸相当于稀释被检验的溶液,这会导致测量不准确。若该溶液为酸性溶液,则pH偏高;若该溶液为碱性溶液,则pH偏低。3.取出试纸后,应将盛放试纸的容器盖严,以免被实验室的一些药品污染。一二【例题1】 某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )A.用湿润的pH试纸测定稀硫酸的pHB.用干燥的pH试纸测定二氧化碳气体的pHC.用干燥的pH试纸测定浓硫酸的pHD.用干燥的pH试纸测定氢氧化钠稀溶液的pH解析:答案:D 一二一二二、中和反应中溶液pH的变化及溶质判断(以氢氧化钠与盐酸反应为例)图11.用酸滴碱的pH变化(如图1所示)从曲线图中可获得如下信息:(1)在加入盐酸前,溶液的pH>7,随着盐酸的滴入,溶液的pH逐渐减小,在C点之前溶液的溶质为NaOH、NaCl。(2)C点处恰好完全中和,溶液的pH=7,此时溶液的溶质为NaCl。(3)继续滴加盐酸至过量,溶液的pH<7,此时溶液的溶质为HCl、NaCl。一二2.用碱滴酸的pH变化(如图2所示)从曲线图中可获得如下信息:(1)在加入氢氧化钠溶液前,溶液的pH<7,随着氢氧化钠溶液的滴入,溶液的pH逐渐增大,在C点之前溶液的溶质为HCl、NaCl。(2)C点处恰好完全中和,溶液的pH=7,此时溶液的溶质为NaCl。(3)继续滴加氢氧化钠溶液至过量,溶液的pH>7,此时溶液的溶质为NaOH、NaCl。一二【例题2】某校化学兴趣小组利用数字化传感器探究稀盐酸与氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示,下列说法正确的是( )A.图中A点所示溶液中,含有的溶质是NaCl和NaOHB.由A点到B点的pH变化过程证明酸与碱发生了中和反应C.向图中C点所示溶液中滴加无色酚酞,溶液不变色D.该实验是将盐酸逐滴滴入盛有氢氧化钠溶液的烧杯中一二解析:A点时溶液的pH小于7,溶液显酸性,说明稀盐酸有剩余,所得溶液中的溶质为HCl和NaCl,A错误;由A点到B点的pH变化过程,图像中pH的变化是从小于7逐渐增大到等于7,溶液由酸性变为中性,说明酸与碱发生了中和反应,B正确;C点时溶液的pH大于7,溶液显碱性,能使酚酞溶液变红色,C错误;图像中pH的变化是从小于7逐渐增大到大于7,可知原溶液显酸性,然后不断地加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,D错误。答案:B123456 答案1.人体内一些液体的正常pH范围如下,其中呈酸性的是( )A.血浆7.35~7.45 B.胃液0.9~1.5C.胆汁7.1~7.3 D.胰液7.5~8.01234562.下表是生活中几种常见物质的pH,其中能使无色酚酞溶液变红的是( ) 答案解析1234563.有A、B、C三种溶液,A能使紫色石蕊溶液变红,B能使无色酚酞溶液变红,C遇紫色石蕊溶液和无色酚酞溶液均无变化,则三种溶液的pH由大到小的顺序是( )A.A>C>B B.C>B>AC.B>A>C D.B>C>A 答案1234564.今有①肥皂水 ②食盐水 ③杨梅汁 ④白糖水⑤蒸馏水五种液体,根据你的生活经验判断,其中pH<7的是 ; pH>7的是 (填序号)。 答案5.下图表示身边一些物质的pH,看图回答下列问题: (1)农作物一般适宜在pH为 或接近 的土壤中生长。 (2)正常雨水pH为5.6,是因为溶有CO2,某市所降雨水pH为4.9,此雨可称为 。 123456 答案1234566.某植物的花瓣汁液(以下简称:X汁液)呈紫色,X汁液分别滴加到盛有下列溶液的试管中有如下现象:(1)据上表推测,X汁液 (填“能”或“不能”)作酸碱指示剂。 (2)将X汁液滴入肥皂水中溶液呈绿色,则肥皂水显 (填“酸”“碱”或“中”)性,pH (填“>”“<”或“=”)7。 (3)粗略测定雨水的酸碱度可使用 。 答案
相关资料
更多









