












高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第一节 钠及其化合物优秀ppt课件
展开第二章 海水中的重要元素——钠和氯
人教版高中化学必修一
2.1.3 钠及其化合物
在面粉发酵或油条制作时常常用到纯碱或小苏打,你知道纯碱、小苏打的成分是什么吗?
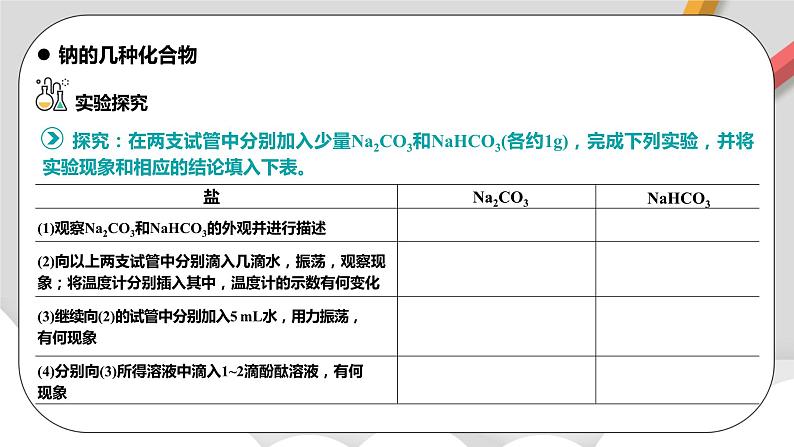
钠的几种化合物
碳酸钠和碳酸氢钠
俗称:
纯碱
苏打
俗称:
小苏打
碳酸钠的用途
碳酸氢钠的用途
探究:在两支试管中分别加入少量Na2CO3和NaHCO3(各约1g),完成下列实验,并将实验现象和相应的结论填入下表。
钠的几种化合物
钠的几种化合物
(1)观察Na2CO3和NaHCO3的外观并进行描述
(2)向以上两支试管中分别滴入几滴水,振荡,观察现象;将温度计分别插入其中,温度计的示数有何变化
(3)继续向(2)的试管中分别加入5 mL水,用力振荡,有何现象
(4)分别向(3)所得溶液中滴入1~2滴酚酞溶液,有何现象
盐
Na2CO3
NaHCO3
碳酸钠、碳酸氢钠的水溶性及酸碱性的实验探究
细小的白色晶体
加水后_____________,温度计示数_____
加水后_____________,温度计示数_____
振荡一段时间后可溶解
固体量减少
溶液_____,溶液碱性较强
溶液_______,溶液碱性较弱
初步结论
碳酸钠、碳酸氢钠均___溶于水,在水中的溶解度:________>________,Na2CO3溶于水___热,NaHCO3溶于水___热,水溶液均显___性,碱性:________>________
白色粉末
结块变成晶体
升高
部分溶解
降低
变红
变浅红
易
Na2CO3
NaHCO3
放
吸
碱
Na2CO3
NaHCO3
探究:如图,分别加热Na2CO3和NaHCO3 ,观察现象,比较Na2CO3和NaHCO3的热稳定性。
钠的几种化合物
钠的几种化合物
碳酸钠、碳酸氢钠热稳定性的实验探究
不变浑浊
Na2CO3很稳定,受热不易发生分解
变浑浊
NaHCO3不稳定,受热容易分解
2NaHCO3====Na2CO3+CO2↑+H2O
△
与盐酸的反应:
NaHCO3+NaOH===Na2CO3+H2O
钠的几种化合物
碳酸钠、碳酸氢钠与酸、碱的反应
①碳酸钠:不反应;②碳酸氢钠:________________________________________________。
与NaOH溶液的反应:
碳酸钠、碳酸氢钠分别与过量盐酸反应的离子方程式:
①碳酸钠:_________________________________________________;
②碳酸氢钠:_______________________________________________。
CO32-+2H+===CO2↑+H2O
HCO-+H+===CO2↑+H2O
问题1:试着利用图像粗略描述上述两种情况,Ⅰ.向Na2CO3溶液中逐滴滴入盐酸,Ⅱ.向盐酸中逐滴滴入Na2CO3溶液。
答案:
问题2:能否用加Ba(OH)2的方法鉴别Na2CO3、NaHCO3溶液?试用离子方程式说明原因。
不能鉴别均,有白色沉淀。
【例1】有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是( )
C
【例2】除去Na2CO3固体中少量NaHCO3的最佳方法是( )A.加入适量盐酸 B.加入NaOH溶液C.加热灼烧 D.配成溶液后通入CO2
C
定义
焰色试验
金属或它们的化合物
很多___________________在灼烧时都会使火焰呈现出特征颜色。根据火焰呈现的特征颜色,可以判断试样所含的金属元素,化学上把这样的定性分析操作称为焰色试验。
操作
盐酸
原火焰颜色相同
试样
火焰的颜色
紫红
黄
紫
砖红
黄绿
绿
几种金属的焰色
焰色试验
检验_________的存在,如鉴别NaCl和KCl溶液。
金属元素
应用
焰色试验
利用焰色试验制节日烟花。
【例1】焰色反应表现的是离子的化学性质吗?作焰色反应的载体为什么用铂丝?能用别的材料代替铂丝吗?
焰色反应表现的是元素的性质,为物理性质。因为铂丝灼烧时火焰没有特殊颜色,因此常用铂丝作焰色反应的载体,其他金属,如光洁无锈的铁丝或镍、铬、钨丝等灼烧时火焰也没有特殊颜色,也可以用作焰色反应的载体。
欧内斯特·索尔维E.Ernest Solvay 1838-1922
比利时工业化学家,1860年索尔维到其叔父的煤气厂工作,研究煤气废液的用途。他想从废液中提取碳酸铵,但实验失败。1861年他又用氨溶液、二氧化碳与食盐混合制成碳酸钠(称为氨碱法),但不知此反应已为前人发现过了。当年他获得比利时政府给他的专利,在布鲁塞尔开设一个小厂从事试验。1863年创办一个正式的制碱工厂,实现了氨碱法的工业化,使制碱生产实现了连续化,食盐的利用率也提高了很多。产品由于质量纯净,而被称为纯碱。
1.下列可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法及现象是( )A.加热时无气体放出B.滴加盐酸时有气泡放出C.溶于水后滴加BaCl2稀溶液有白色沉淀生成D.溶于水后滴加澄清石灰水有白色沉淀生成
D
2.关于NaHCO3的性质,下列说法正确的是( )A.热稳定性比Na2CO3强B.相同温度下溶解度比Na2CO3要大C.NaHCO3只能和酸反应不能和碱反应D.和酸反应放出等量的CO2所消耗的酸比Na2CO3少
D
3.要除去碳酸氢钠溶液中混有的少量碳酸钠,最好采用( )A.加入过量的澄清石灰水B.通入足量的CO2气体C.将溶液加热蒸干并灼烧D.加入适量的氢氧化钠溶液
B
4.下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。请观察如图实验装置并分析实验原理,判断下列说法错误的是( )A.甲为小苏打,乙为纯碱B.甲为Na2CO3,乙为NaHCO3C.要证明物质受热能产生水,可在两支试管内塞上沾有无水硫酸铜粉末的棉花球D.整个实验过程中可以看到丙烧杯的澄清石灰水不变浑浊
B
5.焰火“脚印”“笑脸”“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色试验”知识相关。下列说法中正确的是( )A.焰色试验是化学变化B.用稀盐酸清洗做焰色试验的铂丝(镍丝或铁丝)C.焰色试验均应透过蓝色钴玻璃观察D.利用焰色试验可区分NaCl与Na2CO3固体
B
6.过量的NaHCO3与Na2O2混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是( )A.Na2O和Na2O2 B.Na2O2和Na2CO3C.Na2CO3 D.Na2O
C
课程结束
高中化学人教版 (2019)必修 第一册第一节 钠及其化合物获奖课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一节 钠及其化合物获奖课件ppt,文件包含人教版高中化学必修一211《钠及其化合物》课件pptx、人教版高中化学必修一211《钠及其化合物》同步练习解析版docx、人教版高中化学必修一211《钠及其化合物》同步练习原卷版docx等3份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
高中人教版 (2019)第三节 氧化还原反应优秀课件ppt: 这是一份高中人教版 (2019)第三节 氧化还原反应优秀课件ppt,文件包含人教版高中化学必修一133《氧化还原反应》课件pptx、人教版高中化学必修一133《氧化还原反应》同步练习解析版docx、人教版高中化学必修一133《氧化还原反应》同步练习原卷版docx等3份课件配套教学资源,其中PPT共22页, 欢迎下载使用。
高中化学人教版 (2019)必修 第一册第三节 氧化还原反应完美版课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第三节 氧化还原反应完美版课件ppt,文件包含人教版高中化学必修一132《氧化还原反应》课件pptx、人教版高中化学必修一132《氧化还原反应》同步练习解析版docx、人教版高中化学必修一132《氧化还原反应》同步练习原卷版docx等3份课件配套教学资源,其中PPT共24页, 欢迎下载使用。













