




人教版 (2019)选择性必修1第一节 反应热精品课后测评
展开第1课时 反应热 焓变
1. 熟记常见的吸热反应和放热反应, 将知识应用与证据推理等核心素养有机结合。
2. 理解、掌握化学反应的能量变化及描述方法。
3. 了解反应热、焓、焓变的概念及其表示方法,了解焓变与反应热、物质能量之间的关系。
4. 了解定量测定反应热的基本原理和方法。
一、化学反应的反应热
1.基本概念
2.化学反应的反应热
(1)定义:在等温条件下,化学反应体系向环境 或从环境 的热量称为化学反应的热效应,简称为 。
【说明】等温条件指化学反应发生后,使反应后体系的温度恢复到反应前体系的温度,即反应前后体系的温度相同。
(2)表示符号:Q
Q>0表示吸热;Q<0表示放热。
3.化学变化中能量变化的原因
(1)化学反应中的物质变化和能量变化
化学反应的反应热是由于在化学反应过程中,当反应物分子间的 时,需要克服原子间的相互作用,这需要吸收能量;当原子重新结合成分子时,即 时,又需要释放能量。
(2)反应热与键能的关系
化学反应的过程是原子间的重新组合,反应物中化学键的断裂需要吸收能量(E1),形成新的化学化学键时会释放能量(E2);反应热:Q=E1-E2或Q=E4-E3,即Q等于反应物的键能总和减去生成物的键能总和,或生成物具有的总能量减去反应物具有的总能量。E1>E2或E4>E3时,反应吸收能量;反之,释放能量。
【衔接扩展】
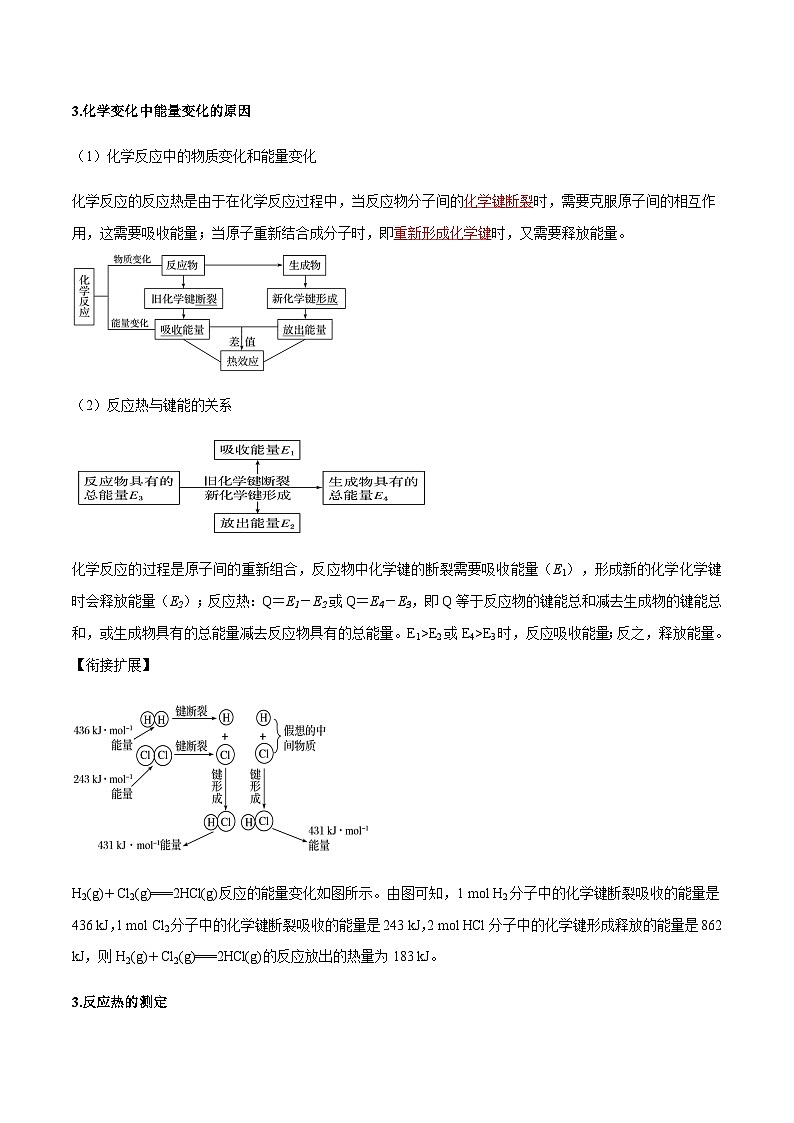
H2(g)+Cl2(g)===2HCl(g)反应的能量变化如图所示。由图可知,1 ml H2分子中的化学键断裂吸收的能量是436 kJ,1 ml Cl2分子中的化学键断裂吸收的能量是243 kJ,2 ml HCl分子中的化学键形成释放的能量是862 kJ,则H2(g)+Cl2(g)===2HCl(g)的反应放出的热量为183 kJ。
3.反应热的测定
(1)仪器——量热计
量热计由内外两个筒组成,内筒是反应容器,外筒 (如图)。
温度计的作用:测定反应前后溶液的 。
搅拌器的作用:使反应前后 、体系的 。
外筒作用: 。
内筒作用: 。
(2)操作——将两种反应物的溶液加入内筒并使之迅速混合,测量 的变化值,即可计算反应热。
(3)计算:反应热的计算公式为Q=-C(T2-T1),式中C代表反应体系的热容,单位是J·K-1,T1、T2分别代表反应前和反应后体系的温度,单位为K。
【知识扩展】T(K)=T(℃)+273.15(T为热力学温度,t为摄氏温度)
二、化学反应的焓变
1.焓
2.焓变
(1)定义:反应产物的总焓与反应物总焓 。
(2)表达式:ΔH=ΔH(反应产物)+ΔH(反应物),单位kJ·ml-1。
(3)与反应热的关系:等压条件下,反应中的 全部转化为 时,焓变与化学反应的反应热相等,即ΔH=Qp(等压条件下化学反应的反应热)。
(4)意义:常用焓变来描述化学反应的反应热;ΔH>0,即反应产物的总焓大于反应物的总焓,反应吸收热量,为吸热反应;ΔH<0,即反应产物的总焓小于反应物的总焓,反应释放热量,为放热反应。
3.焓变的计算
4.吸热反应与放热反应
(1)常见的吸热反应和放热反应
(2)吸热反应与放热反应的比较
三、中和热的含义及测量
1.中和热是指在稀溶液中,强酸跟强碱发生中和反应生成1 ml 时的反应热。
2.测量原理:先将反应器置于绝热容器中,然后在反应器内将酸、碱稀溶液混合,发生中和反应,放出的热传入水(稀溶液)中,测量出水(稀溶液)的温度变化,根据水的质量、比热容等即可求出反应放出的热量。
3.实验装置
(1)实验装置中各仪器(或物品)的名称如下图所示
(2)实验过程中,还需要的其他仪器有50 mL量筒(2个)。
4.实验步骤
①在量热器内测量1.0ml/L100ml盐酸的温度T1;
②向250ml的烧杯中加入1.0 ml·L-1 NaOH溶液100ml,调节其温度,使之 相同。
③迅速将烧杯内的碱液倒入量热计内,盖好杯盖,插入温度计,匀速搅拌,并测量体系达到的最高温度T2。
④近似认为溶液的比热等于水的比热,根据溶液温度升高的数值,计算 。
⑤用同样的方法分别测量KOH溶液与盐酸反应、NaOH溶液与硝酸反应的反应热。
⑥比较上述3个中和反应的反应热是否相同,并说出其中的原因是什么?
5.实验记录
6.实验数据处理
(1)本实验中,所用一元酸、一元碱均为强酸、强碱,体积均为100ml,浓度均为1.0ml/L。(2)由于是稀溶液,为了方便计算,近似认为所用酸、碱溶液,其密度近似地认为都是1 g·cm-3,则酸碱溶液的质量均为100g;反应后所得溶液的比热容c=4.18 kJ·kg-1·K-1。
(3)该实验中酸、碱溶液反应放出的热量Q=-C(T2-T1)=-mc(T2-T1)=-(100+100)×10-3×4.18(T2-T1)=-0.836(T2-T1)kJ,所用中和热为8.36(T2-T1)kJ·ml-1。代入T1、T2即可。
7.实验结论及解释
三个不同反应的反应热是 ,因为中和反应的实质是H+和OH-结合生成H2O,即三者的离子方程式均为H+(aq)+OH-(aq)===H2O(l) 。
【中和热测定实验中应注意的事项】
(1)隔热——防止热量散失的方法:
a.两个烧杯口要相平;
b.在两个烧杯之间填充碎泡沫塑料或碎纸片;
c.用玻璃棒搅拌,而不能用金属棒(丝)搅拌;
d.实验时动作要迅速,尽量减少热量损失。
(2)要使用同一只温度计。测量酸碱及混合液的温度时,测量完一种溶液的温度后,温度计必须用水冲洗干净并用滤纸擦干。
(3)应当使用 ,因为弱酸、弱碱在水溶液中不能完全电离,且弱酸、弱碱的电离是吸热过程,使所测得反应热数据偏小。
(4)测量中和热时不能够使用浓的强酸、强碱,因为浓酸、浓碱溶于水时一般放热,使测得的数据偏大。
(5)实验时所用的 配好后要充分冷却至室温后才能实验。
(6)为了减小误差,重复实验2-3次,取其平均值。
【归纳提升】
中和反应热的测定实验步骤
注意事项:①稀溶液是指物质溶于大量水中,因为 的过程中,由于离子的水合或者说溶剂化的过程中,会伴随能量的变化,一般是会放热。
②中和热不包括离子在水溶液中的生成热、物质的溶解热、电解质电离时的热效应;
③必须是强酸、强碱,因为弱酸和弱碱在中和反应中,还伴随着电离过程、溶剂化过程,所以影响了弱酸与弱碱反应的反应热,
④以生成1mlH2O(l)为基准,中和反应的实质是H+和OH-化合生成H2O,即H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·ml-1。
【例1】(2022秋·辽宁朝阳·高二建平县实验中学校考期中)反应的能量变化与反应进程关系如图所示,下列说法正确的是
A.图中实线表示加入了催化剂
B.该反应的焓变
C.图中虚线表示的反应I、反应II均为吸热反应
D.加入催化剂,速率加快是因为改变了反应的焓变
【变式1-1】(2022秋·湖北十堰·高二校联考期中)已知:H2(g)+F2(g)=2HF(g)的能量变化如图所示,下列有关叙述正确的是
A.氟化氢气体分解生成氢气和氟气的反应是吸热反应
B.1mlH2与1mlF2反应生成2ml液态HF放出的热量小于270kJ
C.在相同条件下,1mlH2与1mlF2的能量总和小于2mlHF气体的能量
D.断裂1mlH-H键和1mlF-F键吸收的能量大于形成2mlH-F键放出的能量
【变式1-2】(2023春·吉林长春·高一长春市解放大路学校校考阶段练习)在25℃、101kPa的条件下。
(1)由,当生成时,要___________(填“吸收”或“放出”)436kJ的能量;由,当断裂中的共价键时,要___________(填“吸收”或“放出”)243kJ的能量。
(2)对于反应,测得生成时,反应过程中放出183kJ的热量,则断开1ml H—Cl键所需的能量是___________kJ。
(3)两个反应:a.,b.。这两个反应的能量转化方式主要是___________能转化为______能。
【例2】已知H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•ml﹣1.用50mL0.50ml•L﹣1盐酸与50mL0.55ml•L﹣1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
①从实验装置上看,图中尚缺少的一种玻璃仪器是 .
②为了测定酸碱反应的中和热,计算时至少需要的数据是
a.酸的浓度和体积 b.碱的浓度和体积 c.比热容
d.反应后溶液的质量 e.生成水的物质的量
f.反应前后温度的变化 g.操作所需时间
A.abcf B.acde
C.cdef D.全部
③若通过该实验测定中和热的△H,其结果常常大于﹣57.3kJ•ml﹣1,其原因可能: .
④用相同浓度和体积的氨水(NH3•H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”或“无影响”).
【变式2-1】(2023秋·浙江宁波·高二统考期末)用如图装置测定盐酸与NaOH溶液反应的中和热。下列说法不正确的是
A.将盐酸、NaOH溶液及发生的反应看成体系
B.盐酸与NaOH溶液反应放热使体系温度升高
C.碎泡沫塑料的作用是保温、隔热
D.反应时将NaOH溶液分多次倒入量热计中
【变式2-2】(2023春·上海浦东新·高二华师大二附中校考期中)在如图所示量热计中,将溶液与溶液混合,温度从25.0℃升高到27.7℃。下列说法错误的是
A.若量热计的保温瓶绝热效果不好,则所测偏大
B.搅拌器可选用导热性能好的金属搅拌器
C.若选用同浓度同体积的盐酸,则溶液温度将升高至超过27.7℃
D.所加NaOH溶液稍微过量,目的是保证溶液完全被中和
1.(2023春·福建南平·高一统考期中)下列变化过程,既属于氧化还原反应又是放热反应的是
A.与反应B.浓稀释
C.灼热的炭与反应D.甲烷与的燃烧反应
2.(2023春·四川成都·高一统考期中)图像法是研究化学反应的一种常用方法。已知化学反应A2(g)+B2(g)=2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是
A.A2(g)+B2(g)=2AB(g)是一个放热反应
B.A2(g)与B2(g)每生成2mlAB(g)时吸收bkJ能量
C.该反应中反应物的总能量低于生成物的总能量
D.断裂1mlA-A键和1mlB-B键时放出akJ能量
3.(2023春·广东佛山·高一顺德市李兆基中学校考期中)下列变化过程中能量变化符合如图所示的是
A.
B.
C.
D.
4.(2023春·浙江·高一浙江大学附属中学校考期中)下列反应既是氧化还原反应又是吸热反应的是
A.和反应B.和反应
C.和反应D.C与反应
5.(2023春·安徽六安·高一六安二中校考期中)化学反应的能量变化如图所示,则下列说法正确的是
A.该反应是吸热反应
B.断裂键和键能放出的能量
C.断裂键需要吸收ykJ的能量
D.的总能量高于1mlA2和1mlB2的总能量
6.(2023春·上海浦东新·高二华师大二附中校考期中)已知:由最稳定的单质合成1 ml某物质的反应焓变叫做该物质的摩尔生成焓,用表示,最稳定的单质的摩尔生成焓为0;有关物质的如图所示,下列有关判断正确的是
A.的摩尔生成焓
B.相同状况下,比稳定
C.依据上表所给数据,可求得的燃烧热
D.与充分反应,放出45.9 kJ的热量
7.(2023秋·湖北武汉·高二武汉市育才高级中学校联考期末)已知:。若生成键、键释放的能量分别为,则断裂键需要吸收的能量为
A.B.C.D.
8.(2022秋·陕西西安·高二长安一中校考期末)根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中的能量变化情况判断,下列说法正确的是
A.NO(g)分解为N2(g)和O2(g)的反应是放热反应
B.2 ml O原子结合生成O2(g)时需要吸收498 kJ能量
C.1 ml NO(g)分子中的化学键断裂时需要吸收1264 kJ能量
D.2 ml N(g)和2 ml O(g)的总能量为1444 kJ
9.(2023春·浙江宁波·高二余姚中学校考期中)氢卤酸的能量关系如图所示下列说法正确的是
A.已知HF气体溶于水放热,则
B.相同条件下,的比的小
C.,
D.相同条件下,的比HI的大
10.(2023春·江苏盐城·高二盐城市第一中学校联考期中)长征二号F遥十二运载火箭发动机发生的反应为:。下列有关说法正确的是
A.偏二甲肼的结构简式为(CH3)2N=NH2
B.N2O4在反应中做还原剂
C.该反应的△H<0、△S<0
D.用E总表示键能之和,该反应的 E总(反应物)< E总(生成物)
二、实验题
11.(2022秋·陕西西安·高二长安一中校考期末)用0.5ml·L-1的盐酸与0.55ml·L-1的NaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是___________,如不改正,求得的中和热会___________(填“偏大”、“偏小”或“无影响”)。
(2)实验时取用相同体积的盐酸和NaOH溶液进行反应,NaOH溶液浓度稍大于盐酸的浓度,原因是___________。
(3)取50 mL NaOH溶液和50mL盐酸溶液进行实验,实验数据如下表。
①由上述实验数据可得,温度差的平均值为___________℃
②近似认为0.55 ml·L-1 NaOH溶液和0.50 ml·L-1盐酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),则中和热ΔH=___________kJ·ml-1(取小数点后一位)。
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钡溶液、稀氨水分别和0.5 L 1 ml·L−1的稀硫酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为___________。
12.(2022秋·四川资阳·高二四川省资阳中学校考期末)I.完成下列问题。
(1)的盐酸与的溶液在如下图所示的装置中进行中和反应。烧杯间填满碎泡沫塑料的作用是___________。大烧杯上如不盖硬纸板,则求得的中和热数值___________(填“偏大”、“偏小”或“无影响”)。
(2)向的溶液中分别加入稍过量的稀醋酸、稀盐酸、浓硫酸,则完全反应时的放出热量从大到小的排序是___________。
(3)已知;。现有下列反应
①;
②;
③;
④;
⑤
其中反应热符合的是___________(写序号)
Ⅱ.以为催化剂的光热化学循环分解(生成一氧化碳和氧气)反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
(4)上述过程中,能量的变化形式是由___________转化为___________,上述过程的的热化学方程式为___________。
放热反应
吸热反应
①燃烧反应。如C、CO、C2H5OH等的燃烧。
②酸碱中和反应。如2KOH+H2SO4=K2SO4+2H2O
③活泼金属与水或酸的反应。如2Al+6HCl=2AlCl3+3H2↑
④多数化合反应。如Na2O+H2O=2NaOH,SO3+H2O=H2SO4
⑤物质的缓慢氧化。
⑥自发进行的氧化还原反应。
⑦铝热反应
①多数分解反应,如CaCO3CaO+CO2↑
②铵盐与碱的反应,
如:2NH4Cl(s)+Ba(OH)2·8H2O (s)=BaCl2+2NH3 ↑+10H2O
③C(s)+H2O(g)CO+H2
④CO2+C2CO
吸热反应
放热反应
能量角度(宏观)
图示
变化
E(反应物)
化学键角度(微观)
断键吸收的总能量大于成键释放的总能量
断键吸收的总能量小于成键释放的总能量
实验
溶液温度/K
反应热/J
T1
T2
NaOH溶液与盐酸反应
290.5
297.4
KOH溶液与盐酸反应
290.3
297.2
NaOH溶液与硝酸反应
290.6
290.5
温度
实验次数
起始温度T1/℃
终止温度T2/℃
HCl
NaOH
平均值
1
26.2
26.0
26.1
29.1
2
25.9
25.9
25.9
29
3
27.0
27.4
27.2
31.7
4
26.4
26.2
26.3
29.5
高中化学人教版 (2019)选择性必修1第一章 化学反应的热效应第一节 反应热课后作业题: 这是一份高中化学人教版 (2019)选择性必修1<a href="/hx/tb_c4002415_t7/?tag_id=28" target="_blank">第一章 化学反应的热效应第一节 反应热课后作业题</a>,共37页。试卷主要包含了18J/,6 kJ等内容,欢迎下载使用。
人教版 (2019)选择性必修1第一章 化学反应的热效应第一节 反应热精练: 这是一份人教版 (2019)选择性必修1第一章 化学反应的热效应第一节 反应热精练,共21页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第一节 反应热精品同步训练题: 这是一份高中化学人教版 (2019)选择性必修1第一节 反应热精品同步训练题,文件包含111反应热焓变-高二化学同步精品讲义+分层练习人教版选择性必修1原卷版docx、111反应热焓变-高二化学同步精品讲义+分层练习人教版选择性必修1解析版docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。













