初中课题 1 质量守恒定律优秀第2课时教案设计
展开《质量守恒定律》第二课时
一、教学目标
1.知道什么是化学方程式,能说出化学方程式表示的意义。
2.会从质、量、数等方面读出化学方程式。
二、教学重难点
教学重点:化学方程式表示的意义。
教学难点:化学方程式中各物质之间的质量比。
三、教学用具
教学课件等。
四、相关资源
《化学方程式表示的意义》图片资源等。
五、教学过程
【课堂引入】
【提问】你能用符号表达出下列化学反应吗?
(1)碳在氧气中燃烧;(2)磷在氧气中燃烧;(3)电解水;(4)过氧化氢分解;(5)加热高锰酸钾。
【回答】(1)C+O2![]() CO2;(2)P+O2
CO2;(2)P+O2![]() P2O5;(3)H2O
P2O5;(3)H2O![]() H2+O2;(4)H2O2
H2+O2;(4)H2O2![]() H2O+O2;(5)KMnO4
H2O+O2;(5)KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2
同学们认为这种表达方式直观吗?我们怎样用化学语言简明、科学地把这些化学反应表示出来呢?学完本节课你就知道啦。
【新知讲解】
一、化学方程式
【过渡】在前面,我们用文字和化学式去表示化学反应。这种式子只能表示哪些物质发生反应,生成了什么物质,但不能表示反应过程的质量关系。我们可以用国际上通用的化学方程式来表示。
【阅读】指导学生阅读课本,了解什么是化学方程式。
【总结】用化学式表示化学反应的式子,叫做化学方程式。如木炭在氧气中燃烧的化学方程式可表示为C+O2![]() CO2;磷在氧气中燃烧的反应可表示为4P+5O2
CO2;磷在氧气中燃烧的反应可表示为4P+5O2![]() 2P2O5。
2P2O5。
化学方程式把“质”和“量”有机地结合在一起,既表示出了化学反应地反应物和生成物,又表示出了各反应物和生成物量上的关系。
【过渡】下面,我们再来认识化学方程式具有哪些意义。
【展示】教师播放图片《化学方程式表示的意义》。
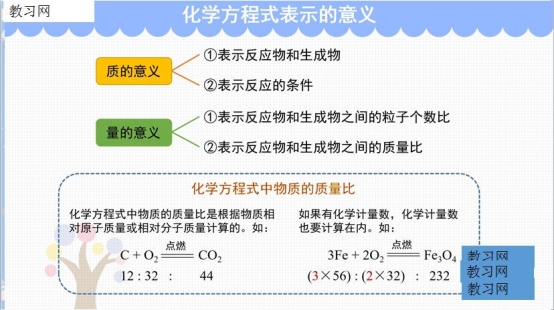
(插入图片《化学方程式表示的意义》)
【总结】化学方程式的意义:
(1)表示出了反应物、生成物和反应条件。
(2)表示出了反应物与生成物间的质量比。
(3)化学反应中各物质之间的微粒个数比。
【练习】对于4P+5O2![]() 2P2O5这个反应,反应物与生成物间的质量比如何表示?
2P2O5这个反应,反应物与生成物间的质量比如何表示?
【答案】计算过程如下:
4P + 5O2 ![]() 2P2O5
2P2O5
31×4 ∶ 16×2×5 ∶ (31×2+16×5)×2
124 ∶ 160 ∶ 284
31 ∶ 40 ∶ 71
【讲解】计算反应物与生成物之间的质量比时,应将反应物与生成物的相对分子质量乘以各物质前面的化学计量数,这样的计算才遵守质量守恒定律,而且将反应物与生成物的质量比化简后仍遵守质量守恒定律。
【提问】化学方程式应该怎么读?
【总结】化学方程式能直观地反映出化学反应中“质”和“量”的变化及关系,将其中的“+”读成“和”,反应物和生成物中间的“![]() ”读成“生成”,不能读成“等于”。以磷燃烧为例:
”读成“生成”,不能读成“等于”。以磷燃烧为例:
(1)宏观读法:磷和氧气在点燃的条件下生成了五氧化二磷。
(2)微观读法:每4个磷原子在点燃条件下与5个氧分子完全反应,生成2个五氧化二磷分子。
(3)质量读法:每124份质量的磷在点燃的情况下,与160份质量的氧气完全反应,生成284份质量的五氧化二磷。
【讨论】从物质种类、质量和反应条件等方面考虑,下列反应的化学方程式能提供给你哪些信息?
1.硫在氧气中燃烧的反应:S+O2![]() SO2
SO2
2.铁与硫酸铜溶液的反应:Fe+CuSO4=FeSO4+Cu
3.铜丝表面的氧化铜与氢气在加热条件下反应:CuO+H2![]() Cu+H2O
Cu+H2O
【总结】可见化学方程式能给我们提供很多有用的信息,我们可以利用它所提供的这些信息选择适当的物质和条件来制取我们所需要的物质。
典型例题
例1.不能根据化学方程式获得的信息是( )
A.反应中的反应物和生成物
B.各反应物、生成物之间的质量比
C.化学反应速率的大小
D.反应发生所需要的条件
解析:化学方程式表示出了各反应物和生成物的组成,表示出了反应进行所需要的条件,表示出了质量守恒定律,很明显地看到原子的种类和数目没有发生变化,不能表示反应速率的大小。
答案:C
例2.根据化学反应方程式4NH3+5O24X+6H2O,推断X的化学式为( )
A.NO B.N2 C.N2O5 D.NO2
解析:据质量守恒定律可知,化学反应前后原子的种类、个数不变,反应前有10个氧原子、4个氮原子、12个氢原子,反应后有12个氢原子、6个氧原子,所以一个X的分子中有1个氧原子、1个氮原子;X的化学式为NO,选A。
答案:A
例3.下列关于化学方程式:2H2+O2![]() 2H2O的叙述中,错误的是( )
2H2O的叙述中,错误的是( )
A.氢气和氧气在点燃的条件下反应生成水
B.每2个氢分子与1个氧分子反应生成2个水分子
C.每2份质量的氢气和1份质量的氧气通过点燃生成2份质量的水
D.每4份质量的氢气和32份质量的氧气恰好完全反应,生成36份质量的水
解析:氢气和氧气在点燃条件下反应生成水,A正确。每2个氢分子与1个氧分子在点燃条件下结合成2个水分子,B正确。该化学方程式表示每4份质量的氢气和32份质量的氧气通过点燃生成36份质量的水,C错误,D正确。
答案:C
六、课堂总结
通过本节课的学习,我们知道什么是化学方程式以及它能告诉我们关于化学反应的很多信息,化学方程式是学习化学的一种非常有用的工具。
七、板书设计
第五单元 化学方程式
课题1 质量守恒定律
第二课时
化学方程式
1.定义:用化学式表示化学反应的式子,叫做化学方程式。
2.意义:(1)表示反应物、生成物以及反应条件;
(2)表示反应物、生成物之间的质量比;
(3)表示反应物、生成物之间的粒子数比。
3.读法
初中化学人教版九年级上册课题 1 质量守恒定律获奖第1课时教案: 这是一份初中化学人教版九年级上册课题 1 质量守恒定律获奖第1课时教案,共6页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。
初中化学人教版九年级上册课题 1 质量守恒定律第2课时教案: 这是一份初中化学人教版九年级上册课题 1 质量守恒定律第2课时教案,共5页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。
初中化学人教版九年级上册课题 1 质量守恒定律第2课时教案: 这是一份初中化学人教版九年级上册课题 1 质量守恒定律第2课时教案,共4页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。