






所属成套资源:2023高考化学二轮专题复习与测课件(16份)
2023高考化学二轮专题复习与测试第一部分专题三离子反应氧化还原反应课件
展开
这是一份2023高考化学二轮专题复习与测试第一部分专题三离子反应氧化还原反应课件,共60页。PPT课件主要包含了高考调研明晰考向,答案B,核心整合热点突破,2特殊检验方法,常见阴离子的检验,答案D,答案A等内容,欢迎下载使用。
专题三 离子反应 氧化还原反应
3.(2022·浙江卷)关于反应Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O,下列说法正确的是( )A.H2SO4发生还原反应B.Na2S2O3既是氧化剂又是还原剂C.氧化产物与还原产物的物质的量之比为2∶1D.1 ml Na2S2O3发生反应,转移4 ml电子
解析:Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O,该反应的本质是硫代硫酸根离子在酸性条件下发生歧化反应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用是提供酸性环境。H2SO4转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发生还原反应,A说法不正确;
Na2S2O3中的S的化合价为+2,其发生歧化反应生成S(0价)和SO2(+4价),故其既是氧化剂又是还原剂,B说法正确;该反应的氧化产物是SO2,还原产物为S,氧化产物与还原产物的物质的量之比为1∶1,C说法不正确;根据其中S元素的化合价变化情况可知,1 ml Na2S2O3发生反应,要转移2 ml电子,D说法不正确。故选B。
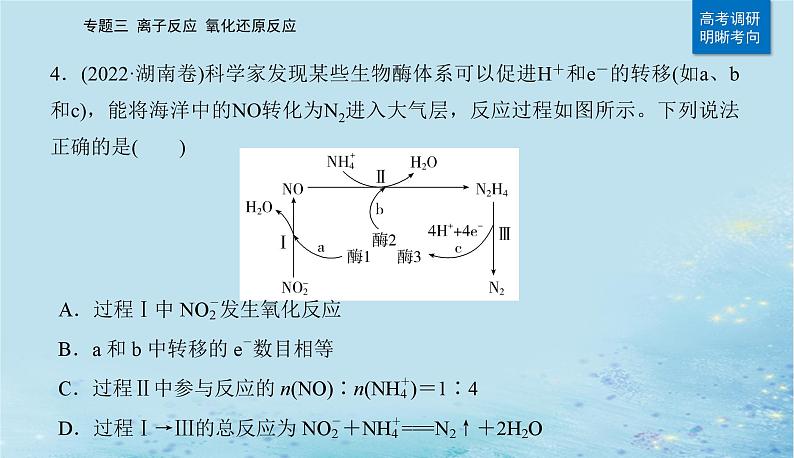
4.(2022·湖南卷)科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO转化为N2进入大气层,反应过程如图所示。下列说法正确的是( )
离子反应是化学反应中的一种重要反应类型,与生产、生活以及科研都关系密切。离子方程式的正误判断常以选择题的形式呈现,非选择题常与氧化还原反应理论、化学工艺流程、实验滴定(沉淀滴定、氧化还原滴定)相结合,书写相关反应的离子方程式。氧化还原型离子方程式的书写是近几年高考命题的热点内容。结合近几年高考的命题特点,依据离子方程式的书写规则,通过题组训练,掌握离子方程式的书写技巧,特别是与“量”有关的离子方程式更是训练的重点。氧化还原反应是高中化学的核心理论,贯穿于高中化学学习的始终,也是高考考查的重点和热点内容,通常会融入其他专题进行考查。陌生的氧化还原反应方程式的书写成为近年来考查的亮点,书写提供信息的陌生氧化还原反应(或离子反应)方程式时,应利用所给信息依据相关反应原理预测反应产物,然后加以配平即可写出相应的反应方程式。
答案:(1)× (2)× (3)× (4)× (5)× (6)× (7)× (8)× (9)× (10)√
考点一 离子方程式书写
2.离子方程式中拆写原则(1)溶于水的强电解质可以拆,弱电解质以及固体不可以拆。(2)多元弱酸的酸式酸根离子不可以拆,多元强酸的酸式酸根离子可以拆。(3)微溶物的处理:如澄清石灰水可以拆,石灰乳不可以拆。3.与量有关的离子反应方程的书写(1)反应的先后顺序:①氧化还原型离子反应要注意氧化性或还原性的强弱:如还原性:I->Fe2+>Br->Cl-;氧化性:Ag+>Fe3+>Cu2+>H+>Fe2+>Zn2+。根据强弱规律判断反应顺序。②生成沉淀:先生成更难溶的沉淀
1.离子方程式正误判断的思维流程
2.“四两”破千题——离子方程式正误判断要注意“四个两”
考点二 离子检验和离子共存1.常见阳离子的检验(1)加入NaOH溶液,生成沉淀或气体:
(3)焰色试验:金属离子还可以使用焰色试验进行检验,其中K的焰色要透过蓝色钴玻璃观察。
1.离子共存解题策略判断多种离子能否大量共存于同一溶液中,方法有:一色:溶液的颜色;二性:溶液的酸、碱性;三特殊:在给定的条件下,可能会出现一些特殊的离子,如焰色试验时焰色呈黄色,还要考虑是否有K+;四反应:同种离子在不同的条件下可能发生不同的反应。
2.坚持“四项”基本原则,突破离子推断问题
离子共存问题审题技巧(1)注意判断离子共存的情况:如,“能”“不能”“一定”“可能”“一定不能”。(2)注意题干中提示的溶液酸碱性:酸性溶液中一定存在H+,碱性溶液中一定存在OH-。(3)注意题干中提示的溶液颜色:无色溶液中不可能存在Cu2+、Fe2+、Fe3+、MnO等有色离子。(4)注意正确理解“透明溶液”:透明溶液可以有色,如CuSO4溶液。(5)注意题干中水的电离程度:常温下当水电离产生的c(H+)氧化产物;还原性:还原剂>还原产物。2.守恒规律:得失电子守恒。3.价态规律:同一元素不同价态之间转化时,价态只靠近不交叉,相邻价态不反应。4.优先规律:当存在多种氧化剂(或还原剂)时,还原剂(或氧化剂)优先与氧化性(或还原性)强的氧化剂(或还原剂)反应。该原则常用于判断某一氧化还原反应方程式是否正确,判断物质发生氧化还原反应的先后顺序。
1.解答氧化还原反应概念题的“三个步骤”
2.新情境下氧化还原方程式的书写(1)新信息或流程图→判断反应物和部分生成物。(2)分析化合价的变化→确定氧化产物或还原产物。(3)化合价升降总数相等→配平参与氧化还原反应的各物质计量数。(4)体系环境、电荷守恒→补加反应物或生成物配平。
解析:由氢原子吸引电子的能力介于碳原子和硅原子之间可知,三氯硅烷中硅元素为+4价、氢元素为-1价。由题给方程式可知,反应中氢元素的化合价降低被还原,氯化氢是反应的氧化剂,氢气是还原产物,故A项正确;由题给方程式可知,反应中氢元素的化合价降低被还原,氯化氢是反应的氧化剂,硅元素化合价升高被氧化,硅为反应的还原剂,则三氯硅烷即是氧化产物,也是还原产物,故B项正确;由题给方程式可知,反应中氢元素的化合价降低被还原,氯化氢是反应的氧化剂,硅元素化合价升高被氧化,硅为反应的还原剂,还原剂与氧化剂的物质的量比1∶3,故C项正确;由题给方程式可知,反应中氢元素的化合价降低被还原,氯化氢是反应的氧化剂,硅元素化合价升高被氧化,硅为反应的还原剂,则反应中生成1 ml三氯硅烷转移4 ml电子,故D项错误。故选D。
理解概念抓实质,解题应用靠特征,即从氧化还原反应的实质——电子转移去分析理解有关概念,而在实际解题过程中,应从分析元素化合价入手。具体方法是“找变价,判类型,分升降,定其他”。信息型化学方程式的书写首先依据氧化还原反应原理判断反应物或生成物,然后进行配平,最后缺的物质一般是酸、碱、水、H+、OH-等。
解析:根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A项错误;硅元素化合价由-4价升为+4价,故SiH4发生氧化反应,B项错误;反应中氧化剂为二氧化碳,还原剂为SiH4,则氧化剂与还原剂的物质的量之比为4∶1,C项错误;根据反应方程式可知,Si元素的化合价由-4价升高至+4价,因此生成1 ml SiO2时,转移8 ml电子,D项正确。故选D。
2.(2021·天津卷)关于反应H2SO4+Na2SO3===Na2SO4+SO2↑+H2O所涉及的物质,下列说法错误的是( )A.H2SO4在该反应中为氧化剂B.Na2SO3容易被空气中的O2氧化变质C.Na2SO4是含有共价键的离子化合物D.SO2是导致酸雨的主要有害污染物
解析:H2SO4+Na2SO3===Na2SO4+SO2↑+H2O中无化合价的变化,不属于氧化还原反应,所以该反应中无氧化剂,故A项错误;Na2SO3不稳定,容易被空气中的O2氧化成硫酸钠变质,故B项正确;Na2SO4含有阴、阳离子,存在离子键,硫酸根中含有共价键,故C项正确;SO2在空去中会转化成硫酸,形成酸雨,所以二氧化硫是导致酸雨的主要有害污染物,故D项正确。故选A。
4.(2021·浙江卷)关于反应8NH3+6NO2===7N2+12H2O,下列说法正确的是( )A.NH3中H元素被氧化B.NO2在反应过程中失去电子C.还原剂与氧化剂的物质的量之比为3∶4D.氧化产物与还原产物的质量之比为4∶3
解析:NH3中H元素的化合价没有发生变化,故其未被氧化,被氧化的是N元素,A项不正确;NO2在反应过程中得到电子,B项不正确;该反应中,NH3是还原剂,NO2是氧化剂,由化学方程式可知,还原剂与氧化剂的物质的量之比为4∶3,C项不正确;该反应中氧化产物和还原产物均为N2,还原剂被氧化后得到氧化产物,氧化剂被还原后得到还原产物,还原剂与氧化剂的物质的量之比为4∶3,因此,氧化产物与还原产物的质量之比为4∶3 ,D项正确。故选D。
5.(2022·深圳二模)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2的工艺的主要反应机理如图所示。下列说法不正确的是( )
6.(2022·茂名二模)I2的一种制备方法如图所示。下列说法正确的是( )
A.“富集”时发生的离子方程式为Ag++I-===AgI↓B.转化反应为Fe+2AgI===Fe2++2Ag+2I-,说明Fe2+的还原性大于I-C.通入过量Cl2,氧化产物只有一种D.制备的I2可直接用于加碘盐
相关课件
这是一份2024届高考化学二轮专题复习与测试第一部分专题三离子反应氧化还原反应课件,共48页。PPT课件主要包含了高考调研明晰考向,答案C,答案B,核心整合热点突破,答案D等内容,欢迎下载使用。
这是一份新高考化学二轮总复习 专题突破课件 专题三 离子反应 氧化还原反应(含解析),共60页。PPT课件主要包含了Ⅱ常见阴离子的检验,Al3+,Ba2+,Na+,焰色反应,答案A,答案C,答案D,答案B,答案BD等内容,欢迎下载使用。
这是一份新高考化学二轮复习精品课件专题三氧化还原反应离子反应(含解析),共60页。PPT课件主要包含了内容索引,核心考点聚焦,专项热考突破,专题体系构建,N2O4,C2H8N2,6NA,答案B,答案D,AgNO3溶液等内容,欢迎下载使用。








