




高中化学人教版 (2019)选择性必修1第一节 电离平衡教课内容ppt课件
展开将1 mL 1×10-5 ml·L-1的盐酸,稀释至1000 mL。分别计算稀释前、后溶液中的H+的物质的量浓度及溶液的pH.
[任务1]寻找证明水的电离很微弱的证据
活动1 水的导电性实验
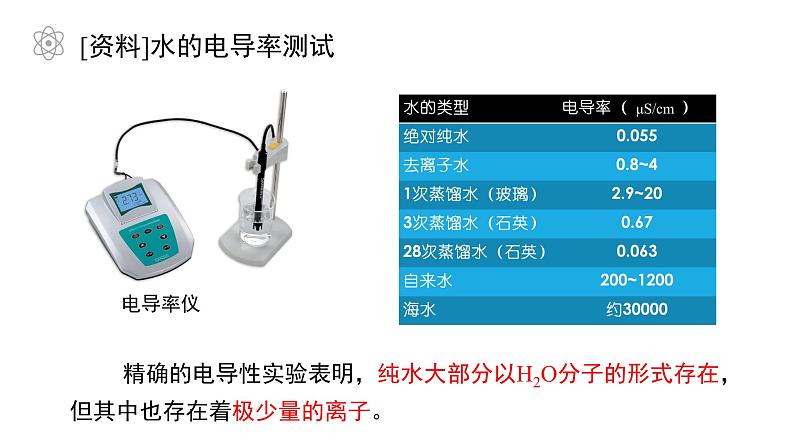
[资料]水的电导率测试
精确的电导性实验表明,纯水大部分以H2O分子的形式存在,但其中也存在着极少量的离子。
[活动2]测定纯水的pH(常温)
pH试纸使用方法将pH试纸放在玻璃片上,用干燥、洁净的玻璃棒蘸取待测液点在pH试纸上,然后与标准比色卡进行对照,读出所测溶液的pH。
测定结果:常温下,纯水的pH=7
[活动3]依据常温下水的pH=7,计算常温下水中的H+和OH-的浓度,以及水的电离度。
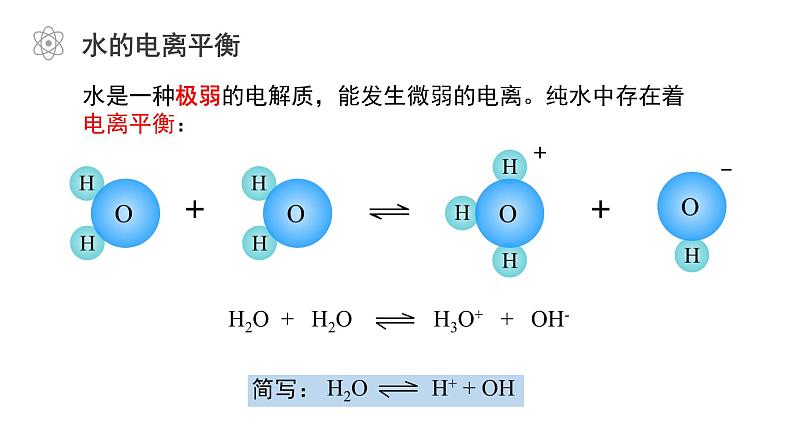
水是一种极弱的电解质,能发生微弱的电离。纯水中存在着电离平衡:
H2O + H2O H3O+ + OH-
H2O H+ + OH -
当水的电离达到平衡时,电离平衡常数K的表达式为:
水的离子积常数Kw,简称水的离子积
(1) Kw只受温度影响。温度升高,水的离子积增大;(2)室温(25℃)下, Kw = 1.0×10-14; 100℃下, Kw = 54.5×10-14 ≈ 1.0×10-12
[计算]常温下,向纯水中加入碱,计算下列各项:
水的离子积常数Kw不仅适用于纯水体系,也适用于稀的电解质溶液
Kw的表达式中c(H+)或c(OH-)是指体系中的H+浓度或OH-浓度
水的电离平衡的影响因素
H2O H+ + OH- ∆H>0
[小结]水的电离平衡的影响因素
(1)温度升高,促进水的电离,Kw增大;(2) 酸、碱抑制水的电离,Kw不变;(3)外加能与H+、OH- 反应的物质,会促进水的电离,Kw不变。
常温时,将1 mL 1×10-5 ml/L的盐酸稀释至1000 mL,测得稀释后溶液的pH为6.96。试分析:(1)稀释后溶液中存在哪些粒子?(2)这些粒子的来源是什么?(3)每种离子的浓度是多少?
高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH课文配套课件ppt: 这是一份高中化学人教版 (2019)选择性必修1第二节 水的电离和溶液的pH课文配套课件ppt,文件包含第2课时酸碱中和滴定及pH的简单计算pptx、第1课时水的电离溶液的酸碱性与pHpptx等2份课件配套教学资源,其中PPT共104页, 欢迎下载使用。
人教版 (2019)选择性必修1第一节 电离平衡图文ppt课件: 这是一份人教版 (2019)选择性必修1第一节 电离平衡图文ppt课件,文件包含311pptx、312pptx等2份课件配套教学资源,其中PPT共36页, 欢迎下载使用。
人教版 (2019)选择性必修1第二节 水的电离和溶液的pH多媒体教学ppt课件: 这是一份人教版 (2019)选择性必修1第二节 水的电离和溶液的pH多媒体教学ppt课件,文件包含选择性必修1第三章第二节第1课时水的电离和溶液的pH-教学课件pptx、选择性必修1第三章第二节第1课时水的电离和溶液的pH-学案docx、选择性必修1第三章第二节第1课时水的电离和溶液的pH-教学设计docx、选择性必修1第三章第二节第1课时水的电离和溶液的pH-作业设计docx等4份课件配套教学资源,其中PPT共29页, 欢迎下载使用。













