

所属成套资源:2022年高中化学必修二课时练习(含答案)
2022年高中化学必修二课时练习:离子键 Word版含答案
展开
这是一份2022年高中化学必修二课时练习:离子键 Word版含答案,共4页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
离子键一、选择题1.下列叙述不正确的是( )A.活泼金属与活泼非金属化合时,能形成离子键B.阴、阳离子通过静电引力所形成的化学键叫做离子键C.离子所带电荷的符号和数目与原子成键时得失电子有关D.阳离子半径比相应的原子半径小,而阴离子半径比相应的原子半径大 2.下列不属于离子化合物的是( )A.Na2O2 B.CaF2 C.SO2 D.Ba(OH) 2 3.下列表达方法正确的是( )。A.Na2O的电子式:![]() B.硫离子的电子式:
B.硫离子的电子式:![]() C.Na+的结构示意图:
C.Na+的结构示意图: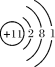 D.碳13:C4.下列关于电子式的说法不正确的是( )。A.每种元素的原子都可以写出电子式 B.简单阳离子的电子式与它的离子符号相同C.阴离子的电子式要加方括号表示 D.电子式就是核外电子排布的式子5.A和B两元素能形成AB2型离子化合物,则A和B原子的原子序数可能是( )。A.6和8 B.11和6 C.20和10 D.20和176.具有以下所述价电子数的原子,最难形成离子的是( )。A.L层6个 B.L层4个 C.M层2个 D.M层7个7.由电子层结构相同的两种离子组成的离子化合物是( )。A.CO B.SO2 C.Na2O D.Na2S8.某元素最高正价与最低负价的代数和为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是( )。A.K2S B.MgO C. MgS D.NaF9.下列性质中,可以证明某化合物内一定存在离子键的是( )A.水溶液能导电 B.由金属和非金属元素的原子组成C.熔融状态能导电 D.可以溶于水 10.下列数值表示有关元素的原子序数,各原子能以离子键相互结合成稳定的化合物的是( )A.10与19 B.6与16 C.11与17 D.14与8 11.下列化合物的电子式书写正确的是( )
D.碳13:C4.下列关于电子式的说法不正确的是( )。A.每种元素的原子都可以写出电子式 B.简单阳离子的电子式与它的离子符号相同C.阴离子的电子式要加方括号表示 D.电子式就是核外电子排布的式子5.A和B两元素能形成AB2型离子化合物,则A和B原子的原子序数可能是( )。A.6和8 B.11和6 C.20和10 D.20和176.具有以下所述价电子数的原子,最难形成离子的是( )。A.L层6个 B.L层4个 C.M层2个 D.M层7个7.由电子层结构相同的两种离子组成的离子化合物是( )。A.CO B.SO2 C.Na2O D.Na2S8.某元素最高正价与最低负价的代数和为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是( )。A.K2S B.MgO C. MgS D.NaF9.下列性质中,可以证明某化合物内一定存在离子键的是( )A.水溶液能导电 B.由金属和非金属元素的原子组成C.熔融状态能导电 D.可以溶于水 10.下列数值表示有关元素的原子序数,各原子能以离子键相互结合成稳定的化合物的是( )A.10与19 B.6与16 C.11与17 D.14与8 11.下列化合物的电子式书写正确的是( )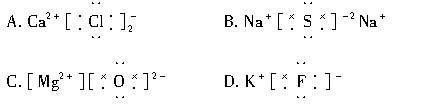 12.下列说法不正确的是 ( )A.凡金属跟非金属元素化合时都能形成离子键B.原子间先通过得失电子变成阴阳离子后,阴阳离子间才能形成离子键C.具有强得电子能力的原子与具有强失电子能力的原子相遇时,能形成离子键D.一般情况下,活泼金属(IA、ⅡA族金属)和活泼的非金属(ⅥA、ⅦA族非金属)它们之间化合时,都易形成离子键 13.下列哪一组元素的原子间反应容易形成离子键( )。原子abcdefgM层电子数1234567①a和c ②a和f ③d和g ④b和gA.①② B.②④ C.②③ D.③④14.下列有关离子键和离子化合物的说法正确的是( )A.凡含离子键的化合物,一定含金属元素B.在化合物MgCl2中,两个氯离子之间也存在离子键C.离子化合物一定能导电D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 15.下列各式用电子式表示的物质的形成过程,其中正确的是( )
12.下列说法不正确的是 ( )A.凡金属跟非金属元素化合时都能形成离子键B.原子间先通过得失电子变成阴阳离子后,阴阳离子间才能形成离子键C.具有强得电子能力的原子与具有强失电子能力的原子相遇时,能形成离子键D.一般情况下,活泼金属(IA、ⅡA族金属)和活泼的非金属(ⅥA、ⅦA族非金属)它们之间化合时,都易形成离子键 13.下列哪一组元素的原子间反应容易形成离子键( )。原子abcdefgM层电子数1234567①a和c ②a和f ③d和g ④b和gA.①② B.②④ C.②③ D.③④14.下列有关离子键和离子化合物的说法正确的是( )A.凡含离子键的化合物,一定含金属元素B.在化合物MgCl2中,两个氯离子之间也存在离子键C.离子化合物一定能导电D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 15.下列各式用电子式表示的物质的形成过程,其中正确的是( )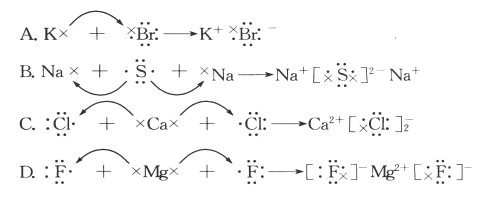 二、非选择题16.⑴写出下列原子的电子式原子NaMgAlSiPSClAr电子式[源:] ⑵书写出下列简单阳离子的电子式离子Na+Mg2+Al3+Ca2+Fe2+Fe3+Cu2+电子式 ⑶书写出下列简单阴离子的电子式离子Cl-O2-N3-H-Br-F-S2-电子式 ⑵用电子式表示离子化合物的形成物质用电子式表示物质的形成NaCl Na2O MgCl2 K2S 17.短周期主族元素A、B、C、D的原子序数依次增大,其中C为金属元素,C的最外层电子数和A相等;C、D两元素原子的质子数之和为A、B两元素质子数之和的3倍。请回答:(1)A为__________B为__________C为__________D为__________;(2)A、B、C、D的原子半径大小顺序为________;(3)A和C形成化合物CA的电子式________;(4)用电子式表示C与D形成化合物C2D的过程_______________________________。
二、非选择题16.⑴写出下列原子的电子式原子NaMgAlSiPSClAr电子式[源:] ⑵书写出下列简单阳离子的电子式离子Na+Mg2+Al3+Ca2+Fe2+Fe3+Cu2+电子式 ⑶书写出下列简单阴离子的电子式离子Cl-O2-N3-H-Br-F-S2-电子式 ⑵用电子式表示离子化合物的形成物质用电子式表示物质的形成NaCl Na2O MgCl2 K2S 17.短周期主族元素A、B、C、D的原子序数依次增大,其中C为金属元素,C的最外层电子数和A相等;C、D两元素原子的质子数之和为A、B两元素质子数之和的3倍。请回答:(1)A为__________B为__________C为__________D为__________;(2)A、B、C、D的原子半径大小顺序为________;(3)A和C形成化合物CA的电子式________;(4)用电子式表示C与D形成化合物C2D的过程_______________________________。
第一章第三节第1课时 离子键1-5:BCDDD 6-10:BCACC 11-15:DABDD16.略 17. (1)H O Na S (2)r(Na)>r(S)>r(O)>r(H) (3)Na+[H]-(4)![]() ―→Na+[]2-Na+
―→Na+[]2-Na+
相关试卷
这是一份2022年高中化学必修二课时练习:元素的性质与原子结构 Word版含答案,共4页。
这是一份2022年高中化学必修二课时练习:时共价键 Word版含答案,共4页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份2022年高中化学必修二课时练习:化学反应与能量A Word版含答案,共8页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。









