




所属成套资源:人教版化学初三上学期PPT课件全套
初中化学人教版九年级上册课题2 原子的结构教课课件ppt
展开
这是一份初中化学人教版九年级上册课题2 原子的结构教课课件ppt,共38页。PPT课件主要包含了C和D等内容,欢迎下载使用。
氢原子的结构(1个电子)
原子核外电子运动的模拟动画
一、情景引入,导入新知
原子核外电子排布有什么规律?
二、自主学习,发现疑问
原子结构示意图表示哪些意义?
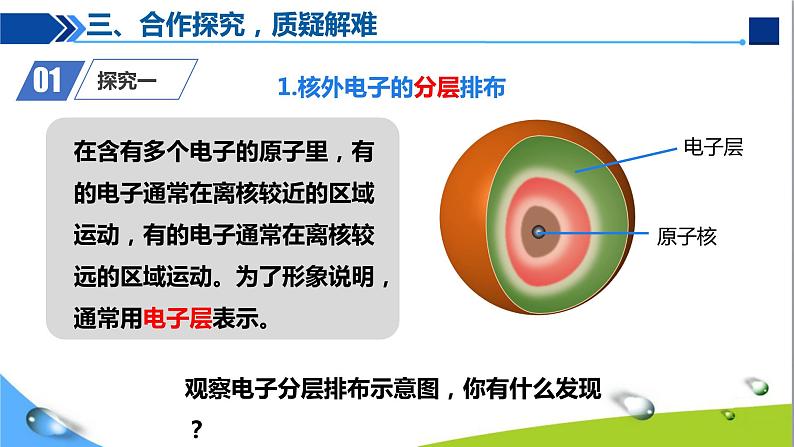
观察电子分层排布示意图,你有什么发现?
1.核外电子的分层排布
三、合作探究,质疑解难
电子层: 离核远近: 能量高低:
一 二 三 四 五 六 七
低 高
近 远
离核最远的电子层叫作最外层,最外层电子数不超过 8 个;只有一层的,电子数不超过 2 个。
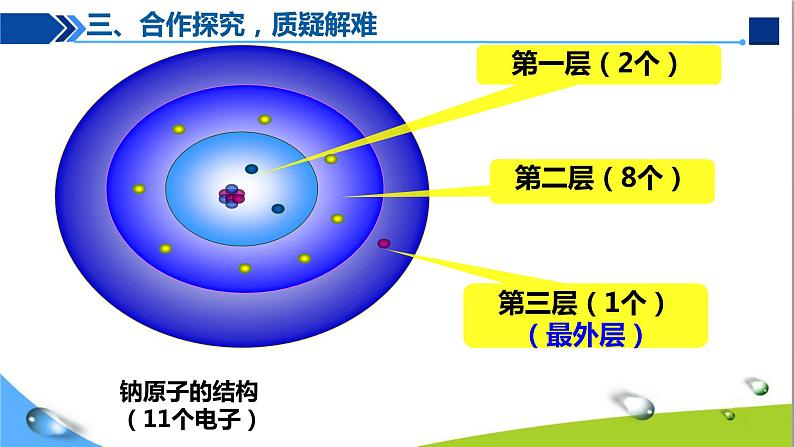
第三层(1个)(最外层)
钠原子的结构(11个电子)
2.下列原子结构示意图是否正确?如有错误,指出错误的原因,并画出正确的原子结构示意图。
1.某原子结构示意图如图:则该原子核电荷数为 ,核外有 个电子,第二层上有 个电子,最外层有 个电子。
观察课本P54的原子结构示意图,思考它们的原子结构有何特点?
金属原子:最外层电子数一般少于4个
非金属原子:最外层电子数一般等于或多于4个
稀有气体原子:最外层电子数等于8个(氦原子除外,最外层电子数为2)
既不得电子,也不失电子
1.原子的最外层电子数决定原子的化学性质2.通常,原子最外层电子数相同,化学性质就相似
相对稳定结构:最外层排满的结构,即最外层为8个电子(氦为两个电子)
易得电子的原子的是 ;
(2)易失电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
(4)属于稀有气体原子的是 。
1.根据下列原子的结构示意图,回答下列问题:
(3)化学性质相似的是 ;
多数金属原子容易失去电子,非金属原子容易得到电子,那么原子失去/得到电子之后变成了什么?
1.带电的原子或原子团,叫做离子
带正电的原子,叫阳离子
带负电的原子,叫阴离子
在元素符号的右上角标明离子所带电荷的电性和数目;
数字在前,正负号在后,若数字为1,必须省略不写。
铝离子:带3个单位正电荷:
镁离子:带2个单位正电荷:
钠离子:带1个单位正电荷:
氧离子:带2个单位负电荷:
氯离子:带1个单位负电荷:
硫离子:带2个单位负电荷:
质子数 电子数
拓展:除单个原子带电形成离子外,带电的原子团也形成离子,又叫“根”。
原子团:2个或2个以上的原子集合在一起形成的一个整体。
离子所带电荷数等于原子失去或得到的电子数
1个氯离子带1个单位负电荷
1个铝离子带3个单位正电荷
1.区别(比较质子数与电子数)(1)原子:质子数 电子数(2)离子:质子数 电子数(3)阳离子:质子数 电子数(4)阴离子:质子数 电子数
氯化钠:由Na+、Cl-构成,Na+、Cl-数目比为1:1
氯化钠是由氯化钠离子构成。( )
氯化钠是由离子构成。( )
1.请你说说下列两种原子是如何变成对应离子的,并写出对应的离子符号
原子形成离子:(1)失为正,得为负; (2)得失电子数=电荷数
2.如图是五种粒子的结构示意图,下列说法错误的是( )
A.表示原子的是①③④ B.表示阴离子的是③⑤C.具有相对稳定结构的是②③⑤ D.④表示的粒子在化学反应中易失去电子
最外层排满,8电子结构
最外层
相关课件
这是一份人教版九年级上册课题2 原子的结构背景图课件ppt,共35页。
这是一份化学人教版课题2 原子的结构教学ppt课件,共30页。PPT课件主要包含了48cm,知识点1原子的构成,“电子云”模型,不带电,原子的内部结构,核电荷数,原子对外不显电性,即电中性,氢原子没有中子,典例1等内容,欢迎下载使用。
这是一份化学课题2 原子的结构教学课件ppt,共29页。PPT课件主要包含了知识点1离子,阳离子,阴离子,阳离子+,失电子,阴离子-,得电子,离子的表示方法,离子符号的意义,Mg2+等内容,欢迎下载使用。










