









所属成套资源:2024版新教材高考化学全程一轮总复习1物质的组成性质和分类(课件+课时作业+学生用书)
- 2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第10讲氯及其重要化合物(课件+课时作业+学生用书)(3份) 课件 0 次下载
- 2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第11讲硫及其重要化合物(课件+课时作业+学生用书)(3份) 课件 0 次下载
- 2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第13讲无机非金属材料(课件+课时作业+学生用书)(3份) 课件 0 次下载
- 2024版新教材高考化学全程一轮总复习第五章物质结构与性质元素周期律第14讲原子结构核外电子排布(课件+课时作业+学生用书)(3份) 课件 0 次下载
- 2024版新教材高考化学全程一轮总复习第五章物质结构与性质元素周期律第15讲元素周期表元素周期律(课件+课时作业+学生用书)(3份) 课件 0 次下载
2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第12讲氮及其化合物(课件+课时作业+学生用书)(3份)
展开这是一份2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第12讲氮及其化合物(课件+课时作业+学生用书)(3份),文件包含2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第12讲氮及其化合物课件pptx、2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第12讲氮及其化合物学生用书doc、2024版新教材高考化学全程一轮总复习课时作业12氮及其化合物doc等3份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
复 习 目 标1.了解氮元素单质及其重要化合物的制备方法,掌握其主要性质及应用;2.了解氮的化合物对环境的影响;3.了解氮及其化合物的转化关系;4.了解NOx与H2O、金属与HNO3的相关计算;5.了解其他含氮化合物的性质。
考点一 氮气及氮的氧化物必备知识整理1.氮的存在和氮的固定
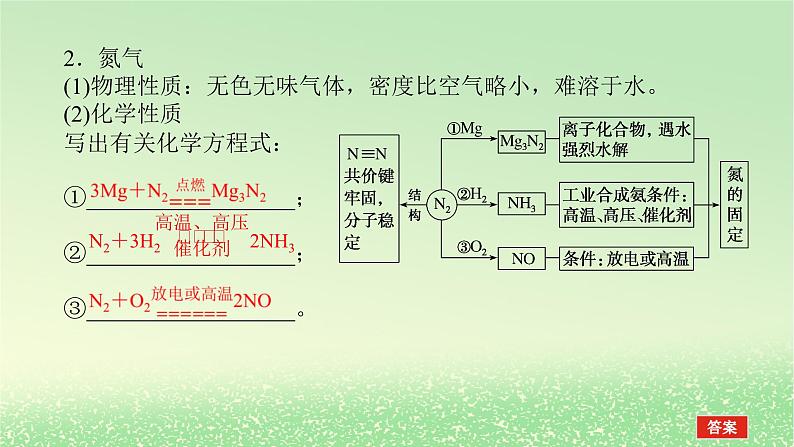
2.氮气(1)物理性质:无色无味气体,密度比空气略小,难溶于水。(2)化学性质写出有关化学方程式:①__________________;②__________________;③__________________。
N2+3H2 2NH3
特别提醒(1)N2到NO2不能一步转化完成。(2)Mg3N2只能干态制取,遇水强烈反应,生成氢氧化镁沉淀,放出氨气。
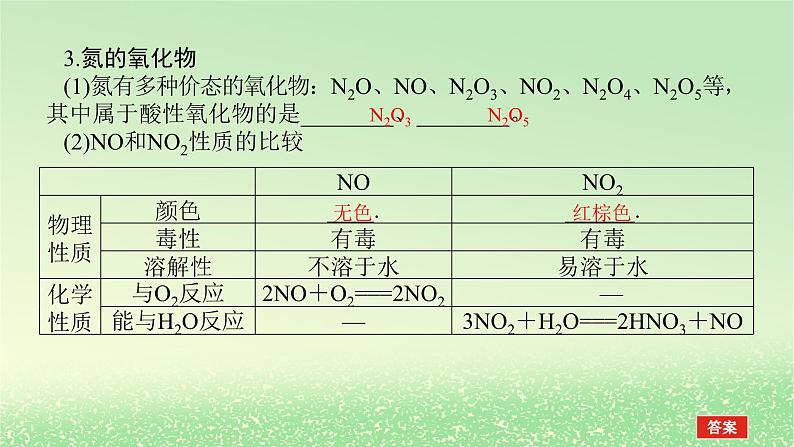
3.氮的氧化物(1)氮有多种价态的氧化物:N2O、NO、N2O3、NO2、N2O4、N2O5等,其中属于酸性氧化物的是________、________。(2)NO和NO2性质的比较
特别提醒(1)氮的氧化物都有毒,其中NO2与N2O4存在下列平衡:2NO2⇌N2O4,因此实验测得NO2的相对分子质量总大于46。(2)验证某无色气体为NO的方法是向无色气体中通入O2(或空气),无色气体变为红棕色。(3)NO与血红蛋白结合使人中毒。
4.氮氧化物对环境的污染及防治(1)常见的污染类型
(2)常见的NOx尾气处理方法①碱液吸收法:_______________________________、____________________________ 。NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)________n(NO),一般适合于工业尾气中NOx的处理。②催化转化法在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N2)或NOx与CO在一定温度下催化转化为无毒气体(N2和CO2),一般适用于汽车尾气的处理。
2NO2+2NaOH===NaNO3+NaNO2+H2O
NO2+NO+2NaOH===2NaNO2+H2O
[正误判断] (1)固氮反应一定属于氧化还原反应( )(2)N2分子的结构稳定,因而氮气不支持任何物质的燃烧( )(3)N2与O2在放电条件下直接化合成NO2( )(4)NO2与水反应生成硝酸,故NO2是酸性氧化物( )(5)制取二氧化氮时,用水或NaOH溶液吸收尾气( )
× Mg可以在氮气中燃烧
× 放电条件下,N2与O2生成NO
× NO2与H2O反应生成HNO3和NO,所以NO2不是酸性氧化物
× NO2与水反应生成硝酸和NO,不能用水吸收,但可以用NaOH溶液吸收
(6)溴蒸气和NO2都是红棕色气体,可用湿润的淀粉KI试纸和NaOH溶液鉴别( )(7)CO、NO、NO2都是大气污染气体,在空气中都能稳定存在( )(8)用向上排空气法收集铜粉与稀硝酸反应产生的气体( )(9)NO2溶于水时,NO2是氧化剂,水是还原剂( )
× 溴蒸气和NO2都能使湿润的淀粉KI试纸变蓝。
× NO与空气中的O2反应
× Cu与稀硝酸生成NO,NO与空气中的O2反应,不能用排空气法收集
× NO2与H2O反应,NO2既是氧化剂又是还原剂
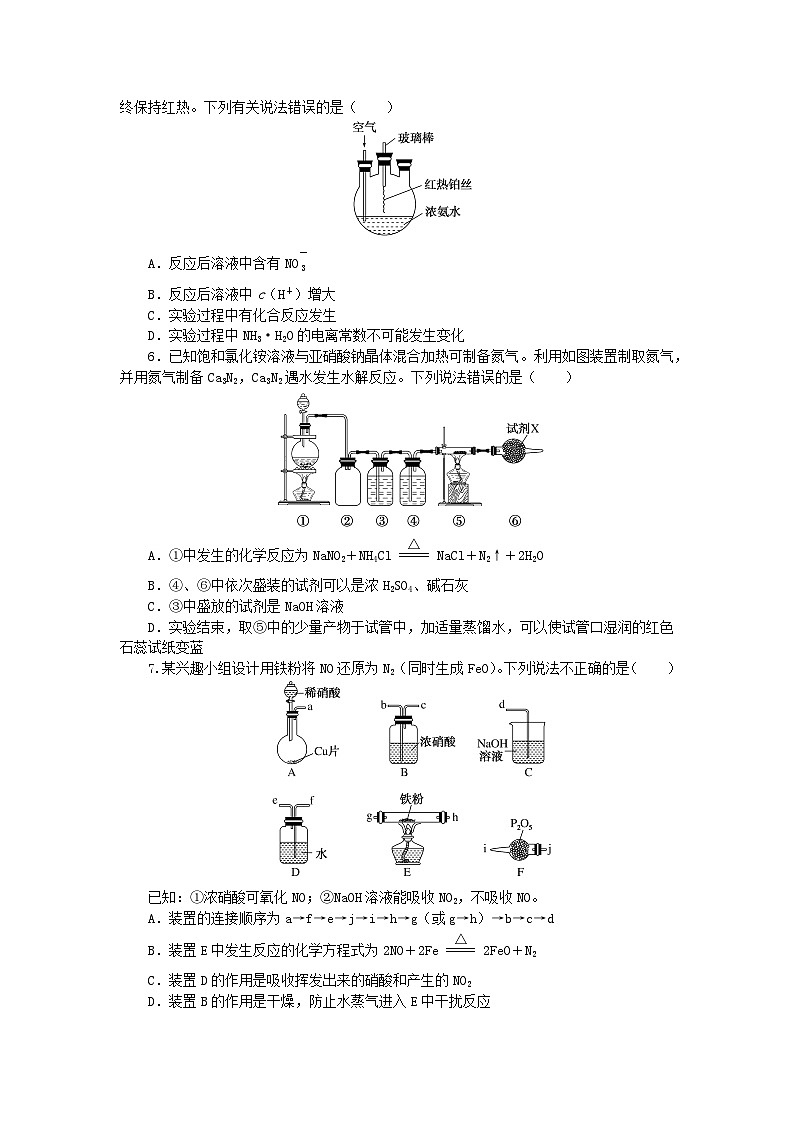
对点题组训练题组一 氮及其氧化物的性质和应用1.常温常压下,注射器甲中装有NO2气体,注射器乙中装有相同体积的空气,注射器与U形管连通,固定活塞。如图所示,打开两个止水夹,足够时间后,将会看到U形管中液面( )A.a端上升,b端下降B.a端下降,b端上升C.U形管中液面无变化D.无法判断
解析:注射器甲中的NO2与水反应:3NO2+H2O===2HNO3+NO,注射器甲中气体的量减小,注射器乙中的空气与水不反应,气体量不变,故a端液面上升,b端液面下降。
2.如图为装有活塞的密闭容器,内盛22.4 mL一氧化氮。若通入11.2 mL氧气(气体体积均在标准状况下测定),保持温度、压强不变,则容器内物质的密度为( )A.等于1.369 g·L-1B.等于2.054 g·L-1C.在1.369 g·L-1和2.054 g·L-1之间D.大于2.054 g·L-1
解析:一氧化氮与氧气恰好发生反应生成了二氧化氮,2NO + O2 === 2NO2 2 1 222.4 mL 11.2 mL 22.4 mL反应后生成了22.4 mL二氧化氮,假设二氧化氮的体积不变,则容器中气体的密度为ρ(NO2)= ≈2.054 g·L-1,因存在转化平衡:2NO2⇌N2O4,则混合气体的体积小于22.4 mL,所以容器中气体的密度应大于2.054 g·L-1。
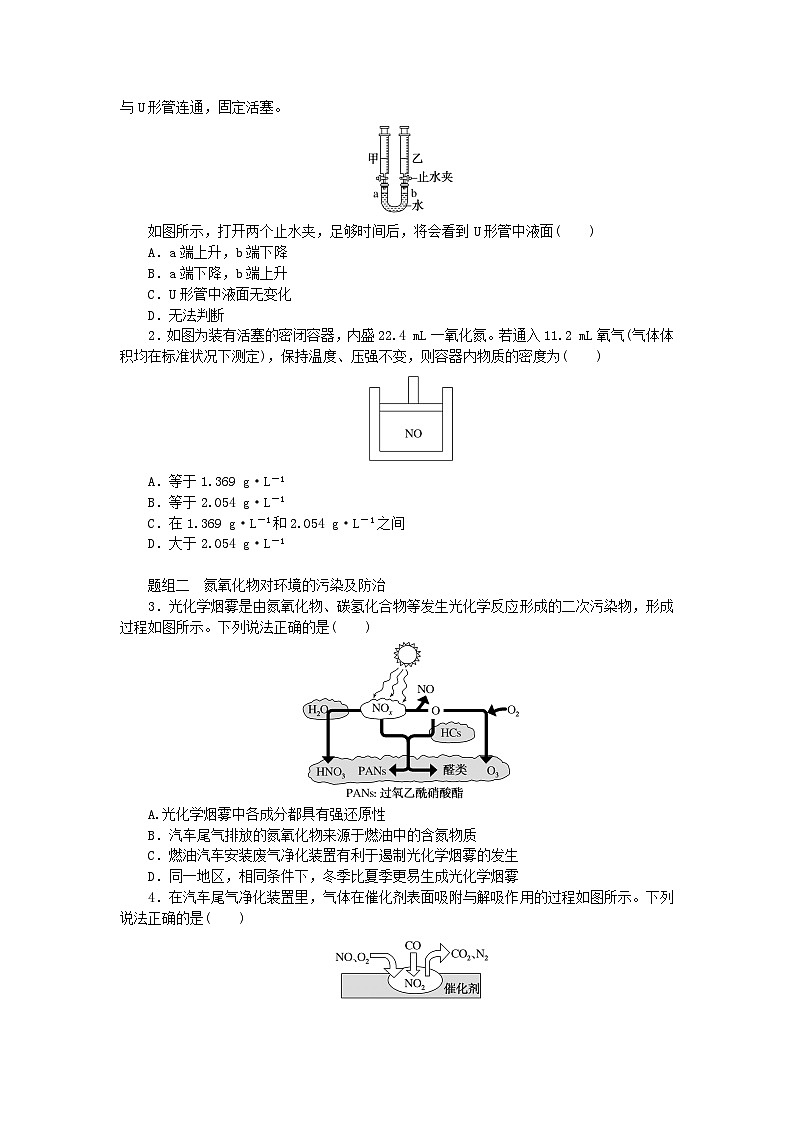
题组二 氮氧化物对环境的污染及防治3.光化学烟雾是由氮氧化物、碳氢化合物等发生光化学反应形成的二次污染物,形成过程如图所示。
下列说法正确的是( )A.光化学烟雾中各成分都具有强还原性B.汽车尾气排放的氮氧化物来源于燃油中的含氮物质C.燃油汽车安装废气净化装置有利于遏制光化学烟雾的发生D.同一地区,相同条件下,冬季比夏季更易生成光化学烟雾
解析:根据图示,光化学烟雾中含O3、HNO3等强氧化性物质,故A错误;汽车燃油一般是汽油,汽油来自石油的分馏和裂化,石油是多种碳氢化合物组成的混合物,不含N元素,故B错误;燃油汽车安装废气净化装置,可减少NO、碳氢化合物等污染物的排放,有利于遏制光化学烟雾的发生,故C正确;夏季日照强度大,是光化学烟雾的多发季节,故D错误。
题组三 NOx与H2O、O2反应的计算5.在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( )①1.2 mL ②2.4 mL ③3 mL ④4 mLA.①② B.②③C.③④ D.①④
6.如图所示,相同条件下,两个容积相同的试管分别装满NO2和NO气体,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液物质的量浓度之比为( )A.1∶1 B.5∶7C.7∶5 D.4∶3
解析:NO2、NO装满试管,则体积相同,根据阿伏加德罗定律:n(NO2)=n(NO),根据氮原子守恒所得硝酸的物质的量相同,溶液的体积相同,所以两个试管中溶液物质的量浓度之比为1∶1。
微点拨氮的氧化物的有关计算(1)NO和O2的混合气体通入水中,由2NO+O2===2NO2和3NO2+H2O===2HNO3+NO得总反应为4NO+3O2+2H2O===4HNO3。
(2)NO2和O2的混合气体通入水中,由3NO2+H2O===2HNO3+NO和2NO+O2===2NO2得总反应为4NO2+O2+2H2O===4HNO3。(3)NO、NO2和O2三种混合气体通入水中先按3NO2+H2O===2HNO3+NO计算出生成NO的体积,再加上原来混合气体中NO体积,再按(1)计算。
考点二 氨和铵盐必备知识整理一、氨(NH3)1.氨的物理性质【注意】 液氨汽化时要吸收大量的热,使周围温度急剧降低,因此,液氨可用作制冷剂。
(2)氨与酸的反应:蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,其现象为____________,将浓盐酸改为________,也会出现相同的现象。化学方程式:HCl+NH3===_________、NH3+HNO3===_________。(3)与盐溶液的反应如过量氨水与AlCl3反应的离子方程式:_________________________________。
(4)氨的催化氧化从化合价角度看,NH3中N元素显-3价,处于最低价,具有________性,在加热和有催化剂(如铂)的条件下,能被O2氧化生成NO和H2O,化学方程式为_______________________ (工业制硝酸的基础)。
4NH3+5O2 4NO+6H2O
3.氨的实验室制法(1)加热固态铵盐和碱的混合物
(2)实验室制取氨的其他方法
× 氨气溶于水,大部分与水反应生成NH3·H2O,故含氮微粒最多的是NH3·H2O
× 氨气遇到浓盐酸、浓硝酸等挥发性酸产生白烟,遇到浓硫酸无此现象
× 碳酸铵、碳酸氢铵水溶液呈碱性
× 铵盐的稀溶液与稀NaOH溶液混合,若不加热,生成的NH3较难逸出
× 原因是NH4Cl受热分解生成气体挥发
(6)现有1 ml·L-1的氨水,则该溶液中NH3·H2O的浓度是1 ml·L-1( )(7)液氨制冷、碘的升华、NH4Cl气化都不涉及化学变化( )
× NH4Cl气化是NH4Cl分解生成NH3与HCl,是化学变化
2.已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用如图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是( )A.C中氧化剂和还原剂的物质的量之比为2∶3B.B中加入的物质可以是碱石灰或无水氯化钙C.D中液体可以使干燥的红色石蕊试纸变蓝D.A中加入的固体,可以是NH4HCO3或NH4Cl
解析:C中氨可以与灼热的氧化铜反应得到氮气和金属铜,N元素的化合价由-3价升高为0价,铜元素的化合价由+2价降低为0价,根据得失电子守恒,氧化剂和还原剂的物质的量之比为3∶2,故A错误;无水氯化钙能与氨反应,所以B中加入的物质可以是碱石灰,不能是无水氯化钙,故B错误;D中液体是氨水,可以使干燥的红色石蕊试纸变蓝,故C正确;NH4Cl加热分解为氨和氯化氢,试管口温度较低,氯化氢和氨化合生成氯化铵,不能用加热氯化铵来制备氨,故D错误。
题组二 喷泉实验3.如图是课外活动小组的同学设计的4个喷泉实验方案,下列有关操作不可能引发喷泉的是( )A.挤压装置①的胶头滴管使CCl4全部进入烧瓶,片刻后打开止水夹B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹D.在装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
4.喷泉实验装置如图所示。应用下列各组气体-溶液,能出现喷泉现象的是( )
解析:本题喷泉实验的原理是使烧瓶内外在短时间内产生较大的压强差,利用大气压将烧瓶下面烧杯中的液体压入烧瓶内,在尖嘴导管口处形成喷泉。A项,H2S气体不易溶于稀盐酸,烧瓶内外不能形成压强差,故不能形成喷泉,错误;B项,HCl极易溶于水,能与稀氨水迅速反应,使烧瓶内外形成较大的压强差,故可以形成喷泉,正确;C项,NO难溶于水,不能与稀硫酸反应,烧瓶内外不能形成压强差,故不能形成喷泉,错误;D项,CO2不溶于饱和碳酸氢钠溶液且不能与饱和碳酸氢钠溶液反应,烧瓶内外不能形成压强差,故不能形成喷泉,错误。
微点拨喷泉实验的原理及应用(1)喷泉实验的原理使烧瓶内外在短时间内产生较大的压强差,利用大气压将烧瓶下面烧杯中的液体压入烧瓶内,在尖嘴导管口形成喷泉。(2)形成喷泉的类型下面是几种常见的能形成喷泉的气体和液体。(3)喷泉实验的引发,加入某种试剂;采取一定操作使烧瓶内的气体与烧杯中的液体接触。
题组三 铵盐的性质及应用5.“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( ) A.加热时,①中上部汇集了NH4Cl固体B.加热时,②中溶液变红,冷却后又都变为无色C.加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性D.三个“封管实验”中所发生的化学反应都是可逆反应
解析:加热时,①上部汇集了固体NH4Cl,是由于氯化铵不稳定,受热易分解,分解生成的氨气遇冷重新反应生成氯化铵,故A正确;加热时氨气逸出,②中颜色为无色,冷却后氨气溶解②中为红色,故B错误;二氧化硫与有机色素化合生成无色物质而具有漂白性,受热又分解,恢复颜色,所以加热时,③溶液变红,冷却后又变为无色,故C错误;可逆反应应在同一条件下进行,题中实验分别在加热条件下和冷却后进行,不是可逆反应,故D错误。
6.NH4ClO4可用作火箭燃料,130 ℃时会分解产生三种单质气体和水。实验室中通过NaClO4与NH4Cl反应来制取NH4ClO4,NH4ClO4与NaCl的溶解度如下图。
下列说法正确的是( )A.NH4ClO4分解后产生的气体通入紫色石蕊溶液中,溶液变红色B.NH4ClO4分解后产生的气体通过足量NaOH溶液,再通过足量灼烧的铜网,可得到纯净的单质气体C.NH4ClO4与NaCl的混合溶液分离时,应采取蒸发浓缩,冷却结晶,过滤,得到NH4ClO4固体粗产品D.在NH4ClO4固体粗产品中加入NaOH浓溶液,加热,收集所得NH3体积,可计算粗产品纯度
解析:NH4ClO4分解后产生的三种单质气体为氮气、氯气、氧气,将产生的气体通入紫色石蕊溶液中,氯气与水反应生成盐酸和次氯酸,使紫色石蕊溶液先变红后褪色,故A错误;NH4ClO4分解后产生的三种单质气体为氮气、氯气、氧气,还会携带一部分水蒸气,将气体通过足量NaOH溶液,氯气与氢氧化钠反应,剩余的气体为氮气、氧气和水蒸气,再通过足量灼烧的铜网,氧气与铜反应,剩余的气体为氮气和水蒸气,不会得到纯净的单质气体,故B错误;据图所示,NH4ClO4的溶解度随温度变化较大,而NaCl的溶解度随温度变化不大,故可用蒸发浓缩,冷却结晶,过滤,得到NH4ClO4固体粗产品,故C正确;在NH4ClO4固体粗产品中加入NaOH浓溶液,生成一水合氨,一水合氨不稳定,加热分解出氨气,NH3易溶于水,则根据收集所得NH3体积小,无法准确计算粗产品纯度,故D错误。
题组四 氨气性质与制备实验综合7.氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如图Ⅰ所示装置。
(1)某同学想用图Ⅱ装置及试剂方便快速地制取少量氨气。化学试剂:①NH4Cl固体、②浓氨水、③NaOH固体。
应选择的装置是 (填字母),选用的试剂是 (填序号)。选用上述试剂制氨气的理由是___________________________________________________________。实验过程中,制气时的实验操作是___________________________。(2)乙装置的作用是 ;写出受热时丙装置中发生反应的化学方程式:___________________________。(3)当戊中观察到 现象,则说明已制得硝酸。某同学按图Ⅰ组装仪器并检验装置气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因是______________________________。如何改进装置:___________________________________________________________。
将浓氨水逐滴滴加到NaOH固体上
干燥氧气和氨的混合气体
4NH3+5O2 4NO+6H2O
过量的氨致使戊中溶液不一定呈酸性
在丙和丁之间连接盛有无水氯化钙的干燥管或盛有浓硫酸的洗气瓶
解析:(1)不加热制取NH3是快速制取少量NH3的措施,具体操作方法是把浓氨水滴到NaOH固体上。(2)乙装置可干燥NH3和O2;NH3和O2在加热和Cr2O3的催化作用下发生催化氧化反应。(3)HNO3能使紫色石蕊溶液变红;由于NH3过量,可能会与HNO3反应,致使观察不到溶液变红的现象,故可在丙和丁之间连接一个能除去NH3的装置。
(4)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是___________________________________________________________。
试管丁内水面慢慢上升,上升到一定高度不再变化,试管内气体颜色由红棕色逐渐变淡至无色
考点三 硝酸必备知识整理1.物理性质:硝酸是无色易 的液体,有 气味。2.化学性质(1)不稳定性反应:________________________________。
(2)强氧化性浓、稀硝酸均具有强氧化性,浓度越大,氧化性越强,其还原产物的价态越高。还原产物一般为HNO3(浓)―→ ,HNO3(稀)―→ 。
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
微点拨 常温下,铁、铝遇浓硝酸能发生“钝化”,并非不反应,故浓硝酸可以用铁桶盛放。
(3)与有机物反应①硝化反应(与 反应):__________________________________;②显色反应:含有苯基的蛋白质遇到浓硝酸时变黄色。
3.工业制法(1)NH3在催化剂作用下与O2反应生成NO:___________________________________________________________。(2)NO进一步氧化生成NO2:___________________________________________________________。(3)用水吸收NO2生成HNO3:___________________________________________________________。
4NH3+5O2 NO+6H2O
2NO+O2===2NO2
3NO2+H2O===2HNO3+NO
[正误判断] (1)实验室也可用锌粒与稀硝酸制取氢气( )(2)常温下,铁、铝在浓硝酸中的钝化为化学变化( )(3)铜溶于稀硝酸不能体现硝酸的酸性( )(4)过量的铜与浓硝酸反应,产物中一定有NO( )(5)Fe与稀硝酸、稀硫酸反应均有气泡产生,说明Fe与两种酸均发生置换反应( )
× HNO3有强氧化性,与金属反应时不放出H2
× Cu与HNO3反应,生成Cu(NO3)2,体现HNO3的酸性
× Fe与稀硫酸反应为置换反应,Fe与稀硝酸不是置换反应
× 1 ml Fe与足量稀硝酸反应,转移3NA个电子
对点题组训练题组一 硝酸的性质及应用1.下述实验中均有红棕色气体产生,对比分析所得结论正确的是( )A.由①中的红棕色气体,可推知反应还有氧气产生B.红棕色气体表明②中木炭与浓硝酸发生了反应C.由③不能说明浓硝酸具有氧化性D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
2.某化学兴趣小组进行了有关Cu、稀硝酸、稀硫酸化学性质的实验,实验过程如图所示。下列有关说法正确的是( )A.实验①中溶液呈蓝色,试管口有红棕色气体产生,说明HNO3被Cu还原为NO2B.实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸的强C.实验③发生反应的化学方程式为3Cu+Cu(NO3)2+4H2SO4===4CuSO4+2NO↑+4H2OD.由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,又可以和稀硫酸反应
解析:稀硝酸被Cu还原为NO,故A错误;Cu与稀硫酸不反应,但硝酸铜在酸性条件下具有硝酸的强氧化性,继续与Cu反应,稀硫酸的氧化性比稀硝酸弱,故B错误;实验③发生反应的化学方程式为3Cu+Cu(NO3)2+4H2SO4===4CuSO4+2NO↑+4H2O,故C正确;由上述实验可得出结论:Cu在常温下可以和稀硝酸反应,故D错误。
题组二 硝酸反应产物综合实验探究3.某同学研究浓硝酸与KSCN溶液的反应,进行如图所示实验。已知:SCN-能被氧化为黄色的(SCN)2,(SCN)2可聚合为红色的(SCN)x。
4.某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。请回答有关问题:
(1)设计装置A的目的是_______________________________________________________。(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸并微热,观察到装置B中的现象是______________________________________________;B中反应的离子方程式为___________________________________。(3)装置E和F的作用是______________;为实现此作用,其操作方法是___________________________________________________________。(4)装置D的作用是吸收多余的氮氧化物,防止污染空气,兼有________的功能。
产生CO2,赶走装置中的空气,防止因NO与O2反应生成NO2而产生干扰
Cu丝表面产生气泡,稀硝酸液面上方仍为无色,溶液变蓝
将注射器中的空气推入E中,若气体变为红棕色则说明生成了NO
题组三 金属与硝酸反应的计算5.取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8 960 mL的NO2气体和672 mL的N2O4气体(都已折算到标准状况),在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀的质量为17.02 g。则x等于( ) B.9.20 C.9.00 D.9.44
6.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 ml·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )A.60 mL B.45 mLC.30 mL D.15 mL
微点拨 金属与硝酸反应计算的思维流程
考点四 氮及其化合物的相互转化必备知识整理1.氮在自然界中的循环
3.氮元素的“价—类二维图”氮元素有多种可变化合价,物质的种类较多,在复习时要从物质类别和价态变化理解这些物质之间的转化关系。
2.一定条件下,含氮元素的物质可发生如图所示的循环转化。
解析:(3)反应h的化学方程式为3NO2+H2O===2HNO3+NO,HNO3是氧化产物,NO是还原产物,因此氧化产物和还原产物的物质的量之比为2∶1。
题组二 氮及其化合物转化关系的综合应用3.依据下图中氮元素及其化合物的转化关系,判断下列说法不正确的是( )A.X是N2O5B.可用排空气法收集NO气体C.工业上以NH3、空气、水为原料生产硝酸D.从原理上看,NH3可与NO2反应实现NH3→N2的转化
解析:NO遇空气中的氧气被氧化为NO2,不可用排空气法收集NO气体,故B错误。
相关课件
这是一份2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第12讲氮及其化合物课件,共60页。PPT课件主要包含了答案B等内容,欢迎下载使用。
这是一份2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第10讲氯及其重要化合物课件,共60页。PPT课件主要包含了HOCl,NaClO,Cl2↑+H2O,CaClO2,答案B,答案D,实验装置,制取流程,饱和食盐水,浓硫酸等内容,欢迎下载使用。
这是一份2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第13讲无机非金属材料(课件+课时作业+学生用书)(3份),文件包含2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第13讲无机非金属材料课件pptx、2024版新教材高考化学全程一轮总复习第四章非金属及其化合物第13讲无机非金属材料学生用书doc、2024版新教材高考化学全程一轮总复习课时作业13无机非金属材料doc等3份课件配套教学资源,其中PPT共29页, 欢迎下载使用。












