

所属成套资源:人教版初中化学九年级上册同步训练(基础版+培优版)
初中化学人教版九年级上册课题 3 利用化学方程式的简单计算随堂练习题
展开
这是一份初中化学人教版九年级上册课题 3 利用化学方程式的简单计算随堂练习题,共5页。试卷主要包含了已知等内容,欢迎下载使用。
5.3 利用化学方程式的简单计算同步培优练习一.选择题(共11小题)1.等质量的下列物质在足量的氧气中燃烧,消耗氧气质量最多的是( )A.镁带 B.硫粉 C.铁丝 D.一氧化碳2.在反应X+2Y=R+2M中,已知R和M的相对原子质量比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则在反应中Y与M的质量比为( )A.12:9 B.23:9 C.32:9 D.16:93.有20g氢气和氧气的混合气体,点燃后充分反应,在室温下还剩余11g气体,则原混合气体中氧气的质量是( )A.9g B.1g C.12g D.19g4.在2A+3B=2C+4D中,3.2gA与9.6gB恰好完全反应生成5.6gC,已知D的相对分子质量为18,则C的相对分子质量为( )A.l6 B.28 C.44 D.645.取20.0g KMnO4固体制氧气,加热一段时间后,固体质量减少1.6g。已分解KMnO4的质量占取用KMnO4总质量的百分率为( )A.8% B.39.5% C.79% D.92%6.在反应2A+3B=2C+D中,当10g A完全反应,生成14g C,又知C与D的相对分子质量比为7:16,则B与D的质量比为( )A.5:6 B.6:5 C.5:4 D.4:57.质量相等的H2O2和KClO3在一定条件下完全分解,所制得氧气的质量( )A.H2O2产生的氧气多 B.KClO3产生的氧气多 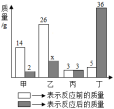 C.H2O2和KClO3产生的氧气一样多 D.无法确定8.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )A.参加反应的甲和乙质量比为2:7 B.丙可能是该反应的催化剂 C.丁一定是化合物 D.x的值是79.将20克H2、O2、N2的混合气体点燃,完全反应后生成18克水,则剩余气体不可能是( )A.N2和H2 B.O2 N2 C.2克N2 D.H2 O2 N210.已知:2Na2O2+2CO2═2Na2CO3+O2。在真空密闭容器中,将13.2gCO2与一定质量的Na2O2固体充分反应后,收集到气体M为xg。下列说法正确的是( )A.若x=4.8,气体M中含有CO2 B.若x=4.8,生成的Na2CO3的质量为15.9g C.若x=7.6,Na2O2反应后可能有剩余 D.若x=7.6,气体M中CO2与O2的质量比为11:811.已知碳酸钙高温分解为氧化钙和二氧化碳。某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将100g该混合物高温煅烧至固体质量不再改变。有关结论正确的是( )A.共生成16g二氧化碳 B.共生成56g氧化钙 C.煅烧后固体中氧元素的质量不变 D.煅烧后固体中钙元素的质量分数减少二.填空题(共10小题)12.已知A+3B2═2C+2D,现有7g A和24g B恰好完全反应生成9g D。已知C的相对分子质量为44,则B2的相对分子质量为 。13.水净化时需要运用科学的方法①净水过程中加入活性炭的作用是 。②过滤操作中用到的玻璃仪器有 。③日常生活中将硬水转化为软水的方法是 。14.把H2、O2混合气10克,点燃生成4.5克水蒸气,则反应前混合气体中氧气可能是 和 .15.碳粉和铜的混合物在空气中加热,充分反应后,发现质量未发生改变,请问原混合物中,碳粉和铜的质量比是 ;已知碳和浓硫酸在加热的条件下反应能生成二氧化碳、二氧化硫和一种氧化物,则该反应的化学方程式为 。16.①质量相同的H2O2和H2O,完全分解后所制得氧气的质量较多的是 ,②质量相同的二氧化碳和一氧化碳一氧化碳中氧原子的个数比为 。17.碱式碳酸铜[Cu2(OH)2CO3]受热分解生成氧化铜、水和二氧化碳,反应的化学方程式为 ;充分加热24g含氧化铜的碱式碳酸铜固体,若反应前后固体中铜元素的质量分数之比为3:4,则该反应生成水和二氧化碳的质量之和为 g。18.请回答下列问题。(1)黑火药是我国古代四大发明之一,黑火药爆炸的原理表示为S+2KNO3+3C═K2S+N2↑+3X↑,则X的化学式是 。(2)在2A+5B=4C+6D反应中,已知34gA与80gB完全反应生成54gD,若已知C的相对分子质量为30,则A的相对分子质量为 。19.一定条件下2A+B=2C的反应中,若8g物质A和一定质量的B恰好完全反应生成72gC,则物质B的质量为 g,上述反应所属的基本反应类型为 ;若B的相对分子质量为32,则A的相对分子质量为 。20.过氧化钠(Na2O2)可用作防毒面具和潜艇等的供氧剂,其反应的原理是过氧化钠与二氧化碳反应生成碳酸钠和氧气。为了模拟该过程,小丽将二氧化碳和氧气的混合气体34.4g通过足量的过氧化钠吸收后,固体质量增加了5.6g。(1)写出该反应的化学方程式 。(2)原混合气体中CO2和O2的质量比为 。21.在点燃条件下,一定质量的C2H2与7.2g O2恰好完全反应,生成6.6g CO2、1.8g H2O和xg CO。则x= ;化学方程式为 。要让这一定量的C2H2充分燃烧还需氧气的质量为 g。三.实验题(共4小题)22.2022年“世界水日”的主题是“珍惜地下水,珍惜隐藏的资源”,生活、生产中我们都离不开水。(1)为研究水的组成,某同学进行了电解水实验。①如图是电解水实验示意图,试管a、b中产生气体的体积比约为 (填最简比),试管a和b产生气体的质量比约为 ,电解水的化学方程式为 。②电解水的实验证明水是由 组成的。(2)小刚同学从海河中取一瓶河水,他在实验室模拟自来水厂的净水过程,最终制成自来水。其实验流程如图所示。请回答以下问题
C.H2O2和KClO3产生的氧气一样多 D.无法确定8.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )A.参加反应的甲和乙质量比为2:7 B.丙可能是该反应的催化剂 C.丁一定是化合物 D.x的值是79.将20克H2、O2、N2的混合气体点燃,完全反应后生成18克水,则剩余气体不可能是( )A.N2和H2 B.O2 N2 C.2克N2 D.H2 O2 N210.已知:2Na2O2+2CO2═2Na2CO3+O2。在真空密闭容器中,将13.2gCO2与一定质量的Na2O2固体充分反应后,收集到气体M为xg。下列说法正确的是( )A.若x=4.8,气体M中含有CO2 B.若x=4.8,生成的Na2CO3的质量为15.9g C.若x=7.6,Na2O2反应后可能有剩余 D.若x=7.6,气体M中CO2与O2的质量比为11:811.已知碳酸钙高温分解为氧化钙和二氧化碳。某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将100g该混合物高温煅烧至固体质量不再改变。有关结论正确的是( )A.共生成16g二氧化碳 B.共生成56g氧化钙 C.煅烧后固体中氧元素的质量不变 D.煅烧后固体中钙元素的质量分数减少二.填空题(共10小题)12.已知A+3B2═2C+2D,现有7g A和24g B恰好完全反应生成9g D。已知C的相对分子质量为44,则B2的相对分子质量为 。13.水净化时需要运用科学的方法①净水过程中加入活性炭的作用是 。②过滤操作中用到的玻璃仪器有 。③日常生活中将硬水转化为软水的方法是 。14.把H2、O2混合气10克,点燃生成4.5克水蒸气,则反应前混合气体中氧气可能是 和 .15.碳粉和铜的混合物在空气中加热,充分反应后,发现质量未发生改变,请问原混合物中,碳粉和铜的质量比是 ;已知碳和浓硫酸在加热的条件下反应能生成二氧化碳、二氧化硫和一种氧化物,则该反应的化学方程式为 。16.①质量相同的H2O2和H2O,完全分解后所制得氧气的质量较多的是 ,②质量相同的二氧化碳和一氧化碳一氧化碳中氧原子的个数比为 。17.碱式碳酸铜[Cu2(OH)2CO3]受热分解生成氧化铜、水和二氧化碳,反应的化学方程式为 ;充分加热24g含氧化铜的碱式碳酸铜固体,若反应前后固体中铜元素的质量分数之比为3:4,则该反应生成水和二氧化碳的质量之和为 g。18.请回答下列问题。(1)黑火药是我国古代四大发明之一,黑火药爆炸的原理表示为S+2KNO3+3C═K2S+N2↑+3X↑,则X的化学式是 。(2)在2A+5B=4C+6D反应中,已知34gA与80gB完全反应生成54gD,若已知C的相对分子质量为30,则A的相对分子质量为 。19.一定条件下2A+B=2C的反应中,若8g物质A和一定质量的B恰好完全反应生成72gC,则物质B的质量为 g,上述反应所属的基本反应类型为 ;若B的相对分子质量为32,则A的相对分子质量为 。20.过氧化钠(Na2O2)可用作防毒面具和潜艇等的供氧剂,其反应的原理是过氧化钠与二氧化碳反应生成碳酸钠和氧气。为了模拟该过程,小丽将二氧化碳和氧气的混合气体34.4g通过足量的过氧化钠吸收后,固体质量增加了5.6g。(1)写出该反应的化学方程式 。(2)原混合气体中CO2和O2的质量比为 。21.在点燃条件下,一定质量的C2H2与7.2g O2恰好完全反应,生成6.6g CO2、1.8g H2O和xg CO。则x= ;化学方程式为 。要让这一定量的C2H2充分燃烧还需氧气的质量为 g。三.实验题(共4小题)22.2022年“世界水日”的主题是“珍惜地下水,珍惜隐藏的资源”,生活、生产中我们都离不开水。(1)为研究水的组成,某同学进行了电解水实验。①如图是电解水实验示意图,试管a、b中产生气体的体积比约为 (填最简比),试管a和b产生气体的质量比约为 ,电解水的化学方程式为 。②电解水的实验证明水是由 组成的。(2)小刚同学从海河中取一瓶河水,他在实验室模拟自来水厂的净水过程,最终制成自来水。其实验流程如图所示。请回答以下问题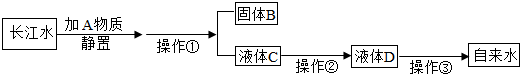 操作①的名称是 ;操作②加入活性炭,主要利用活性炭的 性。经过净化后的液体D是硬水,日常生活中常用 的方法使其软化后使用。(3)某工厂需要64kg氧气作为燃料。若用双氧水来制取这些氧气,则需要双氧水的质量是多少?
操作①的名称是 ;操作②加入活性炭,主要利用活性炭的 性。经过净化后的液体D是硬水,日常生活中常用 的方法使其软化后使用。(3)某工厂需要64kg氧气作为燃料。若用双氧水来制取这些氧气,则需要双氧水的质量是多少?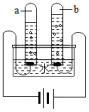 23.如图是实验室制取气体的几种发生装置和收集装置。请回答下列问题:
23.如图是实验室制取气体的几种发生装置和收集装置。请回答下列问题: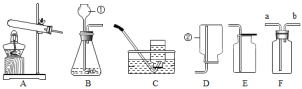 (1)实验室用氯酸钾制取氧气,所选用的装置是 (填序号),A装置中试管口略向下倾斜的原因是 。(2)若用C装置收集氧气,收集氧气的适宜时刻是 。(3)写出一条用B装置制取氧气时的注意事项 。(4)F装置在化学上被称为“万能瓶”,可用于排空气法收集氧气,应从 端通入;若用排水法收集,气体应从 端通入。(5)把干燥纯净的氯酸钾和二氧化锰的混合物18.55克,加热至不再产生气体为止,称量剩余物质量为13.75克,求参加反应的氯酸钾的质量。24.为验证质量守恒定律,小组同学设计了图所示的实验。
(1)实验室用氯酸钾制取氧气,所选用的装置是 (填序号),A装置中试管口略向下倾斜的原因是 。(2)若用C装置收集氧气,收集氧气的适宜时刻是 。(3)写出一条用B装置制取氧气时的注意事项 。(4)F装置在化学上被称为“万能瓶”,可用于排空气法收集氧气,应从 端通入;若用排水法收集,气体应从 端通入。(5)把干燥纯净的氯酸钾和二氧化锰的混合物18.55克,加热至不再产生气体为止,称量剩余物质量为13.75克,求参加反应的氯酸钾的质量。24.为验证质量守恒定律,小组同学设计了图所示的实验。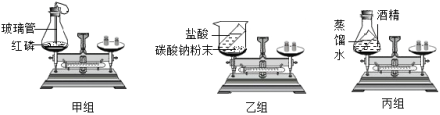 (1)甲组同学在实验过程中发现,化学反应前后天平平衡,锥形瓶内观察到的现象是 ,发生反应的化学方程式为 ,装置中气球的作用是 。(2)乙组同学在实验过程中发现天平指针向右倾斜,其原因是 ,此反应 (选填“遵守”或“不遵守”)质量守恒定律。(3)丙组同学的实验设计能否用来验证质量守恒定律 ,并说明理由 。(4)利用有气体生成或参与的化学反应来验证质量守恒定律,应让该反应在 容器中进行。(5)小组同学用68g过氧化氢溶液和2g二氧化锰混合制取氧气,充分反应后,称得剩余液体和固体的总质量为66.8g。参加反应的过氧化氢的质量是多少 。25.如图所示为实验室中常见的气体制备和收集装置。
(1)甲组同学在实验过程中发现,化学反应前后天平平衡,锥形瓶内观察到的现象是 ,发生反应的化学方程式为 ,装置中气球的作用是 。(2)乙组同学在实验过程中发现天平指针向右倾斜,其原因是 ,此反应 (选填“遵守”或“不遵守”)质量守恒定律。(3)丙组同学的实验设计能否用来验证质量守恒定律 ,并说明理由 。(4)利用有气体生成或参与的化学反应来验证质量守恒定律,应让该反应在 容器中进行。(5)小组同学用68g过氧化氢溶液和2g二氧化锰混合制取氧气,充分反应后,称得剩余液体和固体的总质量为66.8g。参加反应的过氧化氢的质量是多少 。25.如图所示为实验室中常见的气体制备和收集装置。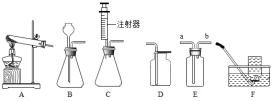 (1)实验室用加热氯酸钾和二氧化锰的混合物制纯净的氧气,应选用的制取装置是 (填字母序号),反应的化学方程式为 。(2)实验室用过氧化氢溶液和二氧化锰制取氧气,选用C做发生装置,选用C的优点是 ,反应的化学方程式为 。(3)实验室用高锰酸钾制取氧气时,试管炸裂了,原因可能是 (一种答案)。(4)欲使用装置E用排空气法收集氧气,则气体应从 (填“a”或“b”)端通入。(5)加热分解15.8g高锰酸钾,完全反应后得到氧气的质量是多少?四.解答题(共2小题)26.实验是学习和研究化学的重要途径。
(1)实验室用加热氯酸钾和二氧化锰的混合物制纯净的氧气,应选用的制取装置是 (填字母序号),反应的化学方程式为 。(2)实验室用过氧化氢溶液和二氧化锰制取氧气,选用C做发生装置,选用C的优点是 ,反应的化学方程式为 。(3)实验室用高锰酸钾制取氧气时,试管炸裂了,原因可能是 (一种答案)。(4)欲使用装置E用排空气法收集氧气,则气体应从 (填“a”或“b”)端通入。(5)加热分解15.8g高锰酸钾,完全反应后得到氧气的质量是多少?四.解答题(共2小题)26.实验是学习和研究化学的重要途径。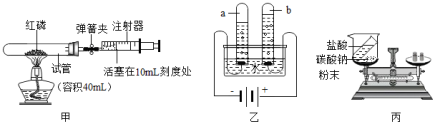 (1)装置甲的实验用到了足量红磷,其反应的化学方程式为 ;反应结束后,待装置冷却至室温后,打开弹簧夹,图甲中试管容积为40mL,注射器活塞从10mL刻度处缓慢移动至 mL刻度处停止(误差忽略不计)。(2)装置乙可进行电解水的实验。此实验可以得出水是由 组成的;在使用a试管内气体前,从实验安全的角度考虑,应该首先进行的操作是 ;b试管内气体的化学性质是 (写出一条即可)。(3)利用装置丙,我们可以探究化学反应前后物质的质量关系。①该装置不能验证质量守恒定律,请说明理由 。②用微粒的观点解释质量守恒定律 。(4)实验室常用加热高锰酸钾的方法制取氧气,若产生3.2g氧气,则需要高锰酸钾的质量是多少?27.化学是一门研究物质的组成、结构、性质和变化规律的科学。(1)不同种元素的本质区别是 不同;元素的化学性质,主要决定于原子的 。(2)一定条件下,下列物质在密闭容器中充分反应,某实验小组测得反应前后各物质的质量如表: ABCD反应前的质量/g1.77.90.10.2反应后的质量/gx04.52.0反应后x的值是 ;该反应的基本反应类型是 。(3)如图是实验室制取气体的装置:
(1)装置甲的实验用到了足量红磷,其反应的化学方程式为 ;反应结束后,待装置冷却至室温后,打开弹簧夹,图甲中试管容积为40mL,注射器活塞从10mL刻度处缓慢移动至 mL刻度处停止(误差忽略不计)。(2)装置乙可进行电解水的实验。此实验可以得出水是由 组成的;在使用a试管内气体前,从实验安全的角度考虑,应该首先进行的操作是 ;b试管内气体的化学性质是 (写出一条即可)。(3)利用装置丙,我们可以探究化学反应前后物质的质量关系。①该装置不能验证质量守恒定律,请说明理由 。②用微粒的观点解释质量守恒定律 。(4)实验室常用加热高锰酸钾的方法制取氧气,若产生3.2g氧气,则需要高锰酸钾的质量是多少?27.化学是一门研究物质的组成、结构、性质和变化规律的科学。(1)不同种元素的本质区别是 不同;元素的化学性质,主要决定于原子的 。(2)一定条件下,下列物质在密闭容器中充分反应,某实验小组测得反应前后各物质的质量如表: ABCD反应前的质量/g1.77.90.10.2反应后的质量/gx04.52.0反应后x的值是 ;该反应的基本反应类型是 。(3)如图是实验室制取气体的装置: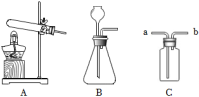 ①若选用A装置加热高锰酸钾制取氧气,其反应的化学方程式为 ;②写出选用B装置制取氧气的化学方程式 ;③若选用C装置排水法收集氧气,集气瓶中先装满水,气体从导管 端通入。(4)取24.5g氯酸钾,加入2g二氧化锰放入大试管中,加热完全分解,求:生成氧气的质量是多少?
①若选用A装置加热高锰酸钾制取氧气,其反应的化学方程式为 ;②写出选用B装置制取氧气的化学方程式 ;③若选用C装置排水法收集氧气,集气瓶中先装满水,气体从导管 端通入。(4)取24.5g氯酸钾,加入2g二氧化锰放入大试管中,加热完全分解,求:生成氧气的质量是多少?
参考答案一.选择题(共11小题)1.B; 2.D; 3.D; 4.B; 5.C; 6.C; 7.A; 8.A; 9.D; 10.D; 11.A;二.填空题(共10小题)12.32; 13.吸附水中色素和异味;烧杯、玻璃棒和 漏斗;加热煮沸; 14.4g;9.5g; 15.1:4;C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O; 16.H2O;14:11; 17.Cu2(OH)2CO3
CO2↑+2SO2↑+2H2O; 16.H2O;14:11; 17.Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑;6; 18.CO2;34; 19.64;化合反应;2; 20.2Na2O2+2CO2=2Na2CO3+O2;11:32; 21.1.4;4C2H2+9O2
2CuO+H2O+CO2↑;6; 18.CO2;34; 19.64;化合反应;2; 20.2Na2O2+2CO2=2Na2CO3+O2;11:32; 21.1.4;4C2H2+9O2![]() 6CO2+4H2O+2CO;0.8;三.实验题(共4小题)22.2:1;1:8;2H2O
6CO2+4H2O+2CO;0.8;三.实验题(共4小题)22.2:1;1:8;2H2O![]() 2H2↑+O2↑;氢元素和氧元素;过滤;吸附;煮沸; 23.AC或AE或AF;防止试管口产生的冷凝水倒流炸裂试管;气泡均匀连续冒出时;长颈漏斗下端要伸入液面以下;a;b; 24.红磷燃烧,产生大量的白烟,放热;4P+5O2
2H2↑+O2↑;氢元素和氧元素;过滤;吸附;煮沸; 23.AC或AE或AF;防止试管口产生的冷凝水倒流炸裂试管;气泡均匀连续冒出时;长颈漏斗下端要伸入液面以下;a;b; 24.红磷燃烧,产生大量的白烟,放热;4P+5O2![]() 2P2O5;平衡气压,防止气压过大冲开瓶塞;反应在烧杯中进行,生成的二氧化碳逸散到空气中使左盘质量减小;遵守;不能;质量守恒定律只适用于化学变化,丙组中蒸馏水和酒精混合是一个物理变化;密闭;6.8g; 25.AF;2KClO3
2P2O5;平衡气压,防止气压过大冲开瓶塞;反应在烧杯中进行,生成的二氧化碳逸散到空气中使左盘质量减小;遵守;不能;质量守恒定律只适用于化学变化,丙组中蒸馏水和酒精混合是一个物理变化;密闭;6.8g; 25.AF;2KClO3![]() 2KCl+3O2↑;可以控制反应速率;2H2O2
2KCl+3O2↑;可以控制反应速率;2H2O2![]() 2H2O+O2↑;试管口未略向下倾斜(或试管未预热或实验结束后先熄灭酒精灯再移出导管);a;四.解答题(共2小题)26.4P+5O2
2H2O+O2↑;试管口未略向下倾斜(或试管未预热或实验结束后先熄灭酒精灯再移出导管);a;四.解答题(共2小题)26.4P+5O2![]() 2P2O5;2;氢元素和氧元素;验纯;具有助燃性;碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,二氧化碳会逸散到空气中,不能称量生成的二氧化碳的质量;化学反应前后,原子的种类、数目和质量均不改变; 27.核内质子数;最外层电子数;3.4;分解反应;2KMnO4
2P2O5;2;氢元素和氧元素;验纯;具有助燃性;碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,二氧化碳会逸散到空气中,不能称量生成的二氧化碳的质量;化学反应前后,原子的种类、数目和质量均不改变; 27.核内质子数;最外层电子数;3.4;分解反应;2KMnO4![]() K2MnO4+MnO2+O2↑;2H2O2
K2MnO4+MnO2+O2↑;2H2O2![]() 2H2O+O2↑;b;声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2023/8/16 18:09:59;用户:初中化学;邮箱:xueshen03@xyh.com;学号:30236074
2H2O+O2↑;b;声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2023/8/16 18:09:59;用户:初中化学;邮箱:xueshen03@xyh.com;学号:30236074
相关试卷
这是一份人教版九年级上册课题 3 利用化学方程式的简单计算习题,共14页。试卷主要包含了选择题,判断题,综合应用题等内容,欢迎下载使用。
这是一份化学九年级上册课题 3 利用化学方程式的简单计算同步测试题,共16页。试卷主要包含了选择题,判断题,科学探究题,综合应用题等内容,欢迎下载使用。
这是一份初中人教版第五单元 化学方程式课题 3 利用化学方程式的简单计算课时训练,共7页。试卷主要包含了8g B.2,6gB.5,36g.,1%,2g等内容,欢迎下载使用。










