


高考化学一轮复习跟踪检测7钠及其化合物 含解析
展开
这是一份高考化学一轮复习跟踪检测7钠及其化合物 含解析,共7页。试卷主要包含了下列事实及其解释不正确的是等内容,欢迎下载使用。
![]() 钠及其化合物 1.关于钠元素的单质及其化合物的叙述不正确的是( )A.钠是银白色金属,质软,熔点相对较低,密度比水小B.Na2O2中阴阳离子个数比为1∶1C.金属钠在空气中长期放置,最终变为碳酸钠D.Na2O和Na2O2都能由金属钠和氧气化合生成,但Na2O和Na2O2中O的价态不同解析:选B B项,Na2O2中阳离子为
钠及其化合物 1.关于钠元素的单质及其化合物的叙述不正确的是( )A.钠是银白色金属,质软,熔点相对较低,密度比水小B.Na2O2中阴阳离子个数比为1∶1C.金属钠在空气中长期放置,最终变为碳酸钠D.Na2O和Na2O2都能由金属钠和氧气化合生成,但Na2O和Na2O2中O的价态不同解析:选B B项,Na2O2中阳离子为![]() 为阴离子,阴、阳离子个数比为1∶2,错误;C项,金属钠切开后置于空气中,发生反应:4Na+O2===2Na2O、Na2O+H2O===2NaOH、2NaOH+CO2===Na2CO3+H2O、Na2CO3+10H2O===Na2CO3·10H2O、Na2CO3·10H2O===Na2CO3+10H2O,正确;D项,Na2O2中O为-1价,Na2O中O为-2价,正确。2.下列各反应中,生成物不随反应条件或反应物的用量变化而变化的是( )A.Na和O2 B.NaOH和CO2C.NaHCO3和NaOH D.Na2CO3和HCl解析:选C A项反应条件不同,生成物不同;B项CO2的用量不同,生成物不同;D项,HCl的用量不同,生成物不同。3.下列事实及其解释不正确的是( )A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应解析:选A A项,对NaHCO3溶液微热,红色加深,是因为HCO的水解程度增大,溶液碱性增强。4.下列有关焰色反应实验操作注意事项的说法中正确的是( )①钾的火焰颜色要透过蓝色钴玻璃观察 ②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质 ③每次实验后,要将铂丝用盐酸洗净 ④实验时最好选择本身颜色较浅的火焰 ⑤没有铂丝时,也可以用光洁无锈的铁丝代替A.仅有③不正确 B.仅有④不正确C.仅有⑤不正确 D.全对解析:选D 由于焰色反应是通过观察火焰颜色来检验离子是否存在的方法,所以实验时所用火焰和所用金属丝在灼烧时都不应该有很明显的颜色,否则将无法观察到被检验离子的真实焰色反应情况;观察钾的火焰颜色时要透过蓝色钴玻璃,目的是滤去黄光,避免钠的干扰。5.测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案不合理的是( )A.取a g混合物充分加热,减重b gB.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体C.取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b gD.取a g混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b g固体解析:选C NaHCO3受热易分解生成Na2CO3、H2O和CO2,通过加热分解利用差量法即可计算出Na2CO3质量,A合理;Na2CO3和NaHCO3均可与盐酸反应生成H2O、CO2和NaCl,所以b g固体是NaCl,利用守恒法可计算出Na2CO3质量,B合理;混合物与足量稀硫酸充分反应,也会生成H2O和CO2,所以逸出的气体是CO2,但会混有水蒸气,即碱石灰增加的质量不是CO2的质量,不能测定其含量,故C不合理;Na2CO3和NaHCO3都与Ba(OH)2溶液反应,反应的离子方程式为CO+Ba2+===BaCO3↓、HCO+OH-+Ba2+===H2O+BaCO3↓,因此最后得到的固体是BaCO3,可以计算出Na2CO3质量,D合理。6.2 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )A.Na2CO3 B.Na2O2、Na2CO3C.NaOH、Na2CO3 D.Na2O2、NaOH、Na2CO3解析:选C 2NaHCO3Na2CO3+CO2↑+H2O 2 mol 1 mol 1 mol 1 mol2Na2O2+2CO2===2Na2CO3+O2 1 mol 1 mol 1 mol2Na2O2+2H2O===4NaOH+O2↑ 1 mol 1 mol 2 molNa2O2恰好与NaHCO3分解生成的CO2和H2O反应,排出气体物质后冷却,残留的固体物质为2 mol Na2CO3、2 mol NaOH。
为阴离子,阴、阳离子个数比为1∶2,错误;C项,金属钠切开后置于空气中,发生反应:4Na+O2===2Na2O、Na2O+H2O===2NaOH、2NaOH+CO2===Na2CO3+H2O、Na2CO3+10H2O===Na2CO3·10H2O、Na2CO3·10H2O===Na2CO3+10H2O,正确;D项,Na2O2中O为-1价,Na2O中O为-2价,正确。2.下列各反应中,生成物不随反应条件或反应物的用量变化而变化的是( )A.Na和O2 B.NaOH和CO2C.NaHCO3和NaOH D.Na2CO3和HCl解析:选C A项反应条件不同,生成物不同;B项CO2的用量不同,生成物不同;D项,HCl的用量不同,生成物不同。3.下列事实及其解释不正确的是( )A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应解析:选A A项,对NaHCO3溶液微热,红色加深,是因为HCO的水解程度增大,溶液碱性增强。4.下列有关焰色反应实验操作注意事项的说法中正确的是( )①钾的火焰颜色要透过蓝色钴玻璃观察 ②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质 ③每次实验后,要将铂丝用盐酸洗净 ④实验时最好选择本身颜色较浅的火焰 ⑤没有铂丝时,也可以用光洁无锈的铁丝代替A.仅有③不正确 B.仅有④不正确C.仅有⑤不正确 D.全对解析:选D 由于焰色反应是通过观察火焰颜色来检验离子是否存在的方法,所以实验时所用火焰和所用金属丝在灼烧时都不应该有很明显的颜色,否则将无法观察到被检验离子的真实焰色反应情况;观察钾的火焰颜色时要透过蓝色钴玻璃,目的是滤去黄光,避免钠的干扰。5.测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案不合理的是( )A.取a g混合物充分加热,减重b gB.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体C.取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b gD.取a g混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b g固体解析:选C NaHCO3受热易分解生成Na2CO3、H2O和CO2,通过加热分解利用差量法即可计算出Na2CO3质量,A合理;Na2CO3和NaHCO3均可与盐酸反应生成H2O、CO2和NaCl,所以b g固体是NaCl,利用守恒法可计算出Na2CO3质量,B合理;混合物与足量稀硫酸充分反应,也会生成H2O和CO2,所以逸出的气体是CO2,但会混有水蒸气,即碱石灰增加的质量不是CO2的质量,不能测定其含量,故C不合理;Na2CO3和NaHCO3都与Ba(OH)2溶液反应,反应的离子方程式为CO+Ba2+===BaCO3↓、HCO+OH-+Ba2+===H2O+BaCO3↓,因此最后得到的固体是BaCO3,可以计算出Na2CO3质量,D合理。6.2 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )A.Na2CO3 B.Na2O2、Na2CO3C.NaOH、Na2CO3 D.Na2O2、NaOH、Na2CO3解析:选C 2NaHCO3Na2CO3+CO2↑+H2O 2 mol 1 mol 1 mol 1 mol2Na2O2+2CO2===2Na2CO3+O2 1 mol 1 mol 1 mol2Na2O2+2H2O===4NaOH+O2↑ 1 mol 1 mol 2 molNa2O2恰好与NaHCO3分解生成的CO2和H2O反应,排出气体物质后冷却,残留的固体物质为2 mol Na2CO3、2 mol NaOH。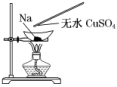 7.如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,据此判断下列说法中不正确的是( )A.上述反应是置换反应B.上述反应说明钠比铜活泼C.上述反应证明钠可以从CuSO4溶液中置换出铜D.加热且无水条件下,Na可以与CuSO4反应并生成Cu解析:选C 实验在无水条件下进行,有红色物质生成,说明熔融的钠将硫酸铜中的铜置换出来并且放出热量,属于置换反应,钠作还原剂,硫酸铜作氧化剂,说明钠比铜活泼,故A、B项正确;若钠与CuSO4溶液混合,则钠先与水反应生成氢氧化钠,氢氧化钠再与硫酸铜反应生成氢氧化铜,不会置换出铜单质,故C错误;根据以上分析,在无水且加热条件下,Na可以与CuSO4反应并生成Cu,故D正确。8.用如图所示实验装置进行相关实验探究,其中装置不合理的是( )
7.如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,据此判断下列说法中不正确的是( )A.上述反应是置换反应B.上述反应说明钠比铜活泼C.上述反应证明钠可以从CuSO4溶液中置换出铜D.加热且无水条件下,Na可以与CuSO4反应并生成Cu解析:选C 实验在无水条件下进行,有红色物质生成,说明熔融的钠将硫酸铜中的铜置换出来并且放出热量,属于置换反应,钠作还原剂,硫酸铜作氧化剂,说明钠比铜活泼,故A、B项正确;若钠与CuSO4溶液混合,则钠先与水反应生成氢氧化钠,氢氧化钠再与硫酸铜反应生成氢氧化铜,不会置换出铜单质,故C错误;根据以上分析,在无水且加热条件下,Na可以与CuSO4反应并生成Cu,故D正确。8.用如图所示实验装置进行相关实验探究,其中装置不合理的是( )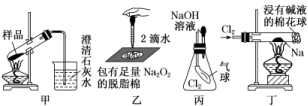 A.图甲装置鉴别纯碱与小苏打B.图乙装置证明Na2O2与水反应放热C.图丙装置证明Cl2能与烧碱溶液反应D.用图丁装置探究钠与Cl2的反应解析:选A 加热固体时,试管口不能向上倾斜,A项设计错误;B项中脱脂棉燃烧,能表明Na2O2与水反应放热;C项中气球变大,表明Cl2能被NaOH溶液吸收;D项能进行Na与Cl2反应的实验。9.
A.图甲装置鉴别纯碱与小苏打B.图乙装置证明Na2O2与水反应放热C.图丙装置证明Cl2能与烧碱溶液反应D.用图丁装置探究钠与Cl2的反应解析:选A 加热固体时,试管口不能向上倾斜,A项设计错误;B项中脱脂棉燃烧,能表明Na2O2与水反应放热;C项中气球变大,表明Cl2能被NaOH溶液吸收;D项能进行Na与Cl2反应的实验。9.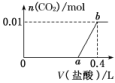 向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )A.在0~a范围内,只发生中和反应B.ab斜段发生反应的离子方程式为CO+2H+===H2O+CO2↑C.a=0.3D.原混合溶液中NaOH与Na2CO3的物质的量之比为 1∶2解析:选C 向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,发生的反应依次为OH-+H+===H2O,CO+H+===HCO,HCO+H+===CO2↑+H2O。在0~a范围内,发生的反应是OH-+H+===H2O,CO+H+===HCO,不只发生中和反应,A错误;ab段发生反应的离子方程式为HCO+H+===CO2↑+H2O,B错误;从图像知生成CO2 0.01 mol,根据HCO+H+===CO2↑+H2O知,消耗HCl的物质的量为0.01 mol,故a=0.3,C正确;根据CO+H+===HCO,HCO+H+===CO2+H2O和图像可知,Na2CO3的物质的量是0.01 mol,共计消耗HCl 0.02 mol,与NaOH反应的HCl是0.04 mol-0.02 mol=0.02 mol,NaOH的物质的量为0.02 mol,因此原混合液中,NaOH与Na2CO3的物质的量之比为2∶1,D错误。10.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W0 g样品进行实验,下列实验方法所对应的实验方案和测量数据最合理(除W0外)的是( )选项实验方法实验方案测量数据A滴定法将样品配成100 mL溶液,取10 mL,加入甲基橙,用标准盐酸滴定消耗盐酸的体积B量气法将样品与盐酸反应,生成的气体全部被碱石灰吸收碱石灰增重的质量C重量法样品放入烧瓶中,置于天平上,加入足量盐酸减轻的质量D量气法将样品与盐酸反应,气体通过排水量气装置量气排水体积解析:选A A项,用甲基橙作指示剂,发生反应Na2CO3+2HCl===2NaCl+H2O+CO2↑,根据消耗HCl的物质的量可确定Na2CO3的含量,正确;B项,CO2中含有水蒸气,导致结果偏大,错误;C项,CO2挥发带出水蒸气,导致结果偏大,错误;D项,CO2能溶于水,不能用排水法收集,可用排饱和NaHCO3溶液的方法收集,错误。
向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )A.在0~a范围内,只发生中和反应B.ab斜段发生反应的离子方程式为CO+2H+===H2O+CO2↑C.a=0.3D.原混合溶液中NaOH与Na2CO3的物质的量之比为 1∶2解析:选C 向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,发生的反应依次为OH-+H+===H2O,CO+H+===HCO,HCO+H+===CO2↑+H2O。在0~a范围内,发生的反应是OH-+H+===H2O,CO+H+===HCO,不只发生中和反应,A错误;ab段发生反应的离子方程式为HCO+H+===CO2↑+H2O,B错误;从图像知生成CO2 0.01 mol,根据HCO+H+===CO2↑+H2O知,消耗HCl的物质的量为0.01 mol,故a=0.3,C正确;根据CO+H+===HCO,HCO+H+===CO2+H2O和图像可知,Na2CO3的物质的量是0.01 mol,共计消耗HCl 0.02 mol,与NaOH反应的HCl是0.04 mol-0.02 mol=0.02 mol,NaOH的物质的量为0.02 mol,因此原混合液中,NaOH与Na2CO3的物质的量之比为2∶1,D错误。10.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W0 g样品进行实验,下列实验方法所对应的实验方案和测量数据最合理(除W0外)的是( )选项实验方法实验方案测量数据A滴定法将样品配成100 mL溶液,取10 mL,加入甲基橙,用标准盐酸滴定消耗盐酸的体积B量气法将样品与盐酸反应,生成的气体全部被碱石灰吸收碱石灰增重的质量C重量法样品放入烧瓶中,置于天平上,加入足量盐酸减轻的质量D量气法将样品与盐酸反应,气体通过排水量气装置量气排水体积解析:选A A项,用甲基橙作指示剂,发生反应Na2CO3+2HCl===2NaCl+H2O+CO2↑,根据消耗HCl的物质的量可确定Na2CO3的含量,正确;B项,CO2中含有水蒸气,导致结果偏大,错误;C项,CO2挥发带出水蒸气,导致结果偏大,错误;D项,CO2能溶于水,不能用排水法收集,可用排饱和NaHCO3溶液的方法收集,错误。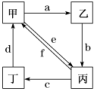 11.如图所示,甲、乙、丙、丁分别代表Na2CO3、NaOH、NaHCO3、CO2四种物质,a、b、c、d、e、f分别表示两种物质间的转化关系。对于图中两种物质间的转化,通过一步反应就能实现的有( )A.只有a、b、c、d B.只有b、c、d、eC.只有c、d、e、f D.a、b、c、d、e、f解析:选D a反应可以是Na2CO3与Ba(OH)2的反应;向NaOH溶液中通入过量的CO2,可以实现反应b;NaHCO3与酸反应可以生成CO2,c反应能够实现;CO2与NaOH反应可以生成Na2CO3,d反应能够实现;Na2CO3溶液中通入CO2能够实现反应e;NaHCO3受热分解或与NaOH反应,能够实现反应f。12.向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)(3)(4)图中分别有OA<AB,OA=AB,OA>AB,
11.如图所示,甲、乙、丙、丁分别代表Na2CO3、NaOH、NaHCO3、CO2四种物质,a、b、c、d、e、f分别表示两种物质间的转化关系。对于图中两种物质间的转化,通过一步反应就能实现的有( )A.只有a、b、c、d B.只有b、c、d、eC.只有c、d、e、f D.a、b、c、d、e、f解析:选D a反应可以是Na2CO3与Ba(OH)2的反应;向NaOH溶液中通入过量的CO2,可以实现反应b;NaHCO3与酸反应可以生成CO2,c反应能够实现;CO2与NaOH反应可以生成Na2CO3,d反应能够实现;Na2CO3溶液中通入CO2能够实现反应e;NaHCO3受热分解或与NaOH反应,能够实现反应f。12.向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)(3)(4)图中分别有OA<AB,OA=AB,OA>AB,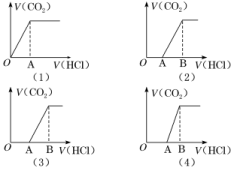 则下列分析与判断不正确的是( )A.M中只有一种溶质的有(1)和(3)B.M中有两种溶质的有(2)和(4)C.(2)图显示M中c(NaHCO3)<c(Na2CO3)D.(4)图显示M中的溶质为NaOH和Na2CO3解析:选C 发生的反应为NaOH+HCl===NaCl+H2O,Na2CO3+HCl===NaCl+NaHCO3,NaHCO3+HCl===NaCl+CO2↑+H2O,由方程式可知Na2CO3转化为NaHCO3消耗盐酸与NaHCO3反应消耗盐酸体积相等。A项,图(1)中加入盐酸即有CO2生成,说明溶质只有一种,为NaHCO3,图(3)中OA=AB,说明溶质只有Na2CO3,正确;图(2)中OA<AB,说明含有Na2CO3和NaHCO3两种溶质,图(4)中OA>AB,说明含有NaOH和Na2CO3两种溶质,B、D项正确;C项,图(2)中OA<AB,说明含有Na2CO3和NaHCO3两种溶质,当AB<2OA时,M中c(NaHCO3)<c(Na2CO3),当AB>2OA时,M中c(NaHCO3)>c(Na2CO3),错误。13.某化学小组在实验室制取Na2O2。查阅资料可知,钠与空气在453~473 K之间可生成Na2O,迅速提高温度到573~673 K之间可生成Na2O2,若温度提高到733~873 K之间Na2O2可分解。除Li外其他碱金属不与N2反应。
则下列分析与判断不正确的是( )A.M中只有一种溶质的有(1)和(3)B.M中有两种溶质的有(2)和(4)C.(2)图显示M中c(NaHCO3)<c(Na2CO3)D.(4)图显示M中的溶质为NaOH和Na2CO3解析:选C 发生的反应为NaOH+HCl===NaCl+H2O,Na2CO3+HCl===NaCl+NaHCO3,NaHCO3+HCl===NaCl+CO2↑+H2O,由方程式可知Na2CO3转化为NaHCO3消耗盐酸与NaHCO3反应消耗盐酸体积相等。A项,图(1)中加入盐酸即有CO2生成,说明溶质只有一种,为NaHCO3,图(3)中OA=AB,说明溶质只有Na2CO3,正确;图(2)中OA<AB,说明含有Na2CO3和NaHCO3两种溶质,图(4)中OA>AB,说明含有NaOH和Na2CO3两种溶质,B、D项正确;C项,图(2)中OA<AB,说明含有Na2CO3和NaHCO3两种溶质,当AB<2OA时,M中c(NaHCO3)<c(Na2CO3),当AB>2OA时,M中c(NaHCO3)>c(Na2CO3),错误。13.某化学小组在实验室制取Na2O2。查阅资料可知,钠与空气在453~473 K之间可生成Na2O,迅速提高温度到573~673 K之间可生成Na2O2,若温度提高到733~873 K之间Na2O2可分解。除Li外其他碱金属不与N2反应。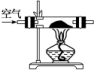 (1)甲组设计制取Na2O2装置如图。①使用该装置制取的Na2O2中可能含有的杂质为________。A.Na3N B.Na2CO3C.Na2O D.NaOHE.NaHCO3②该小组为测定制得的Na2O2样品的纯度,设计装置如下:
(1)甲组设计制取Na2O2装置如图。①使用该装置制取的Na2O2中可能含有的杂质为________。A.Na3N B.Na2CO3C.Na2O D.NaOHE.NaHCO3②该小组为测定制得的Na2O2样品的纯度,设计装置如下: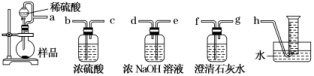 烧瓶中发生的主要反应的化学方程式是____________________。分液漏斗和烧瓶用导管连接可使稀硫酸顺利流下,也可防止产生实验误差,若没有该导管将导致测定结果________(填“偏大”“偏小”或“无影响”)。测定装置的接口从左至右正确的连接顺序是________________________________________________________________。(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果________(填“偏大”或“偏小”)。为证明其分析的正确性,设计实验方案如下:实验方案产生的现象Ⅰ.取烧瓶中的反应液加入少量MnO2粉末有大量气泡逸出Ⅱ.向NaOH稀溶液中加入2~3滴酚酞溶液,然后加入少量的反应液溶液先变红后褪色Ⅲ.向反应液中加入2~3滴酚酞溶液,充分振荡,然后逐滴加入过量的NaOH稀溶液开始无明显现象,加NaOH溶液先变红后褪色 在上述实验中,能够证明乙组分析正确的最佳方案是____(填实验序号)。根据上述实验可知,反应溶液中存在的中间产物与酚酞作用的条件是______________。(3)丙组根据上述提供的有关信息,设计了一个方案可准确的测定样品的纯度。请简述实验操作和需要测定的有关数据__________________________________________________。解析:(1)①由于空气中含有少量的CO2和水蒸气,因此钠与空气反应时产物中可能含有Na2CO3和NaOH,当反应温度在453~473 K之间还有Na2O生成,故选BCD。②烧瓶中发生的主要反应的化学方程式为2Na2O2+2H2SO4===2Na2SO4+O2↑+2H2O;若没有该导管,由于硫酸的流入,会使得收集的气体(含有部分空气)体积偏大,导致测定结果偏大;根据①的分析,需要将生成的CO2除去后再收集O2,从左至右的连接顺序为aedfgh,增加澄清石灰水是检验CO2是否除净。(2)从反应历程上看,Na2O2与水反应生成H2O2,如果H2O2没有完全分解,将会导致放出的氧气偏少,测定结果偏小;为了使H2O2分解,可以加入少量MnO2粉末作为催化剂,故选Ⅰ;根据实验Ⅲ可知,H2O2与酚酞作用的条件是碱性条件。(3)根据钠与空气在453~473 K之间可生成Na2O,迅速提高温度到573~673 K之间可生成Na2O2,若温度提高到733~873 K之间Na2O2可分解,可以称取一定质量的样品(m),加热到733~873 K使之分解,使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算,也可以称取一定质量的样品(m),加入少量MnO2固体,再加入足量水并使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算。答案:(1)①BCD ②2Na2O2+2H2SO4===2Na2SO4+O2↑+2H2O 偏大 aedfgh(2)偏小 Ⅰ 碱性条件(3)称取一定质量的样品(m),加热到733~873 K使之分解,使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算[或称取一定质量的样品(m),加入少量MnO2固体,再加入足量水并使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算]14.我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献。以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为NH3+CO2+H2O===NH4HCO3;NH4HCO3+NaCl===NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。(1)利用上述反应原理,设计如下图所示装置,制取碳酸氢钠晶体,B中盛有饱和碳酸氢钠溶液,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。制取碳酸氢钠晶体可供选用的药品有:a.石灰石 b.生石灰 c.6 mol·L-1盐酸 d.稀盐酸e.浓氨水 f.饱和氯化钠溶液
烧瓶中发生的主要反应的化学方程式是____________________。分液漏斗和烧瓶用导管连接可使稀硫酸顺利流下,也可防止产生实验误差,若没有该导管将导致测定结果________(填“偏大”“偏小”或“无影响”)。测定装置的接口从左至右正确的连接顺序是________________________________________________________________。(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果________(填“偏大”或“偏小”)。为证明其分析的正确性,设计实验方案如下:实验方案产生的现象Ⅰ.取烧瓶中的反应液加入少量MnO2粉末有大量气泡逸出Ⅱ.向NaOH稀溶液中加入2~3滴酚酞溶液,然后加入少量的反应液溶液先变红后褪色Ⅲ.向反应液中加入2~3滴酚酞溶液,充分振荡,然后逐滴加入过量的NaOH稀溶液开始无明显现象,加NaOH溶液先变红后褪色 在上述实验中,能够证明乙组分析正确的最佳方案是____(填实验序号)。根据上述实验可知,反应溶液中存在的中间产物与酚酞作用的条件是______________。(3)丙组根据上述提供的有关信息,设计了一个方案可准确的测定样品的纯度。请简述实验操作和需要测定的有关数据__________________________________________________。解析:(1)①由于空气中含有少量的CO2和水蒸气,因此钠与空气反应时产物中可能含有Na2CO3和NaOH,当反应温度在453~473 K之间还有Na2O生成,故选BCD。②烧瓶中发生的主要反应的化学方程式为2Na2O2+2H2SO4===2Na2SO4+O2↑+2H2O;若没有该导管,由于硫酸的流入,会使得收集的气体(含有部分空气)体积偏大,导致测定结果偏大;根据①的分析,需要将生成的CO2除去后再收集O2,从左至右的连接顺序为aedfgh,增加澄清石灰水是检验CO2是否除净。(2)从反应历程上看,Na2O2与水反应生成H2O2,如果H2O2没有完全分解,将会导致放出的氧气偏少,测定结果偏小;为了使H2O2分解,可以加入少量MnO2粉末作为催化剂,故选Ⅰ;根据实验Ⅲ可知,H2O2与酚酞作用的条件是碱性条件。(3)根据钠与空气在453~473 K之间可生成Na2O,迅速提高温度到573~673 K之间可生成Na2O2,若温度提高到733~873 K之间Na2O2可分解,可以称取一定质量的样品(m),加热到733~873 K使之分解,使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算,也可以称取一定质量的样品(m),加入少量MnO2固体,再加入足量水并使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算。答案:(1)①BCD ②2Na2O2+2H2SO4===2Na2SO4+O2↑+2H2O 偏大 aedfgh(2)偏小 Ⅰ 碱性条件(3)称取一定质量的样品(m),加热到733~873 K使之分解,使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算[或称取一定质量的样品(m),加入少量MnO2固体,再加入足量水并使用量气装置测定常温常压下生成O2体积(V),然后进行有关计算]14.我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献。以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为NH3+CO2+H2O===NH4HCO3;NH4HCO3+NaCl===NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。(1)利用上述反应原理,设计如下图所示装置,制取碳酸氢钠晶体,B中盛有饱和碳酸氢钠溶液,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。制取碳酸氢钠晶体可供选用的药品有:a.石灰石 b.生石灰 c.6 mol·L-1盐酸 d.稀盐酸e.浓氨水 f.饱和氯化钠溶液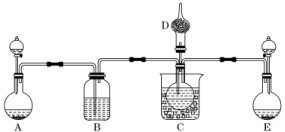 ①A中制备气体时,所需药品是____________(填字母);②B中盛有饱和碳酸氢钠溶液,其作用是______________________________________;③在实验过程中,向C中依次通入足量的NH3、CO2(氨碱法),而不先通CO2再通NH3的原因是____________________________________________________________;④E装置向C中通气的导管不能插入液面下的原因是_________________________。(2)该小组同学为了测定C中所得晶体碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:
①A中制备气体时,所需药品是____________(填字母);②B中盛有饱和碳酸氢钠溶液,其作用是______________________________________;③在实验过程中,向C中依次通入足量的NH3、CO2(氨碱法),而不先通CO2再通NH3的原因是____________________________________________________________;④E装置向C中通气的导管不能插入液面下的原因是_________________________。(2)该小组同学为了测定C中所得晶体碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:![]() ①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是________(填字母);a.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液b.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液②操作Ⅲ的方法为______________、________________、________________;③所得晶体中碳酸氢钠的纯度为__________________________________________。解析:(1)①制取CO2是用石灰石和盐酸在烧瓶中发生反应产生的,由于CO2在水中溶解度不大,所以导气管要伸入到液面以下,而制取氨气是将e浓氨水滴入到盛有b生石灰的烧瓶中反应制取的,氨气在水中非常容易溶解,所以导气管要在液面以上,根据在C中导气管的长短可知:在A中制备CO2气体,所需药品是ac;②用盐酸制取CO2气体时,由于盐酸有挥发性,所以其中含有杂质HCl,在B中盛有饱和碳酸氢钠溶液,其作用就是除去CO2中的杂质HCl;③CO2在水中的溶解度小,产生的HCO的浓度也就小,不容易形成NaHCO3的饱和溶液,所以难形成沉淀,因此在实验过程中,向C中先通入NH3使溶液呈碱性,能吸收大量CO2气体产生较高浓度的HCO,才能析出NaHCO3晶体;④E装置向C中通气的导管不能插入液面下是为了防止倒吸现象的发生。(2)①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是a。在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液,若不出现白色沉淀,就证明氯化钙溶液过量,若产生白色沉淀,就证明氯化钙溶液不足量。因此选项是a;②操作Ⅲ的方法是过滤、洗涤、干燥;③方法一、2NaHCO3Na2CO3+H2O+CO2↑,根据方程式可知2×84 g=168 g NaHCO3完全分解,会产生106 g Na2CO3,固体质量会减轻2×84 g-106 g=62 g;现在固体质量减轻(w-m)g,所以其中含有的NaHCO3的质量是[2×84(w-m)÷62] g=,所以所得晶体中碳酸氢钠的纯度为;方法二、2NaHCO3Na2CO3+H2O+CO2↑,Na2CO3+CaCl2===CaCO3↓+2NaCl。根据方程式可得关系式:2NaHCO3~Na2CO3~CaCO3;若含有168 g NaHCO3,发生反应会产生CaCO3沉淀100 g,现在产生沉淀n g,所以原固体中含有NaHCO3的质量是(168n÷100)g,所以NaHCO3的质量分数是[(168n÷100)g÷w g]×100%=×100%。答案:(1)①ac ②除去CO2中的HCl ③由于CO2在NaCl溶液中的溶解度很小,先通入NH3使食盐水呈碱性,能够吸收大量CO2气体,产生较高浓度的HCO,才能析出NaHCO3晶体 ④防倒吸(2)①a ②过滤 洗涤 干燥 ③×100%
①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是________(填字母);a.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液b.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液②操作Ⅲ的方法为______________、________________、________________;③所得晶体中碳酸氢钠的纯度为__________________________________________。解析:(1)①制取CO2是用石灰石和盐酸在烧瓶中发生反应产生的,由于CO2在水中溶解度不大,所以导气管要伸入到液面以下,而制取氨气是将e浓氨水滴入到盛有b生石灰的烧瓶中反应制取的,氨气在水中非常容易溶解,所以导气管要在液面以上,根据在C中导气管的长短可知:在A中制备CO2气体,所需药品是ac;②用盐酸制取CO2气体时,由于盐酸有挥发性,所以其中含有杂质HCl,在B中盛有饱和碳酸氢钠溶液,其作用就是除去CO2中的杂质HCl;③CO2在水中的溶解度小,产生的HCO的浓度也就小,不容易形成NaHCO3的饱和溶液,所以难形成沉淀,因此在实验过程中,向C中先通入NH3使溶液呈碱性,能吸收大量CO2气体产生较高浓度的HCO,才能析出NaHCO3晶体;④E装置向C中通气的导管不能插入液面下是为了防止倒吸现象的发生。(2)①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是a。在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液,若不出现白色沉淀,就证明氯化钙溶液过量,若产生白色沉淀,就证明氯化钙溶液不足量。因此选项是a;②操作Ⅲ的方法是过滤、洗涤、干燥;③方法一、2NaHCO3Na2CO3+H2O+CO2↑,根据方程式可知2×84 g=168 g NaHCO3完全分解,会产生106 g Na2CO3,固体质量会减轻2×84 g-106 g=62 g;现在固体质量减轻(w-m)g,所以其中含有的NaHCO3的质量是[2×84(w-m)÷62] g=,所以所得晶体中碳酸氢钠的纯度为;方法二、2NaHCO3Na2CO3+H2O+CO2↑,Na2CO3+CaCl2===CaCO3↓+2NaCl。根据方程式可得关系式:2NaHCO3~Na2CO3~CaCO3;若含有168 g NaHCO3,发生反应会产生CaCO3沉淀100 g,现在产生沉淀n g,所以原固体中含有NaHCO3的质量是(168n÷100)g,所以NaHCO3的质量分数是[(168n÷100)g÷w g]×100%=×100%。答案:(1)①ac ②除去CO2中的HCl ③由于CO2在NaCl溶液中的溶解度很小,先通入NH3使食盐水呈碱性,能够吸收大量CO2气体,产生较高浓度的HCO,才能析出NaHCO3晶体 ④防倒吸(2)①a ②过滤 洗涤 干燥 ③×100%
相关试卷
这是一份2024届高考化学一轮复习 课时跟踪检测(十) 钠及其化合物(含答案),共15页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份高考化学一轮复习跟踪检测4氧化还原反应 含解析,共7页。试卷主要包含了下列说法正确的是,已知下列实验事实等内容,欢迎下载使用。
这是一份高考化学一轮复习跟踪检测2物质的量 含解析,共6页。试卷主要包含了NA表示阿伏加德罗常数的数值,设NA表示阿伏加德罗常数的值,NA代表阿伏加德罗常数的数值,下列有关溶液配制的说法正确的是等内容,欢迎下载使用。








