


(通用版)高考化学一轮复习检测02 物质的分类(含答案解析)
展开高考化学复习检测:02
物质的分类
A.2.4g镁在足量的O2中燃烧,转移的电子数为0.1NA
B.标准状况下,5.6 L CO2气体中含有的氧原子数为0.5NA
C.氢原子数为0.4NA的CH3OH分子中含有的σ键数为0.4NA
D.0.1 L 0.5 mol/L CH3COOH溶液中含有的H+数为0.05NA
A.200 mL 2.5 mol·L-1 MgCl2溶液
B.1 000 mL 2.5 mol·L-1 NaCl溶液
C.250 mL 1 mol·L-1 AlCl3溶液
D.300 mL 5 mol·L-1 KClO3溶液
A.1 mol Na2O2与水完全反应时转移电子数为2NA
B.常温下,4 g CH4含有NA个C-H共价键
C.标况下,22.4L氨水含有NA个NH3分子
D.1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
A.摩尔是物质的量的单位,每摩尔物质约含有6.02×1023个分子
B.1 mol氧的质量为16 g
C.0.5 mol He约含有6.02×1023个电子
D.2H既可表示2个氢原子又可表示2 mol氢分子
5.食品干燥剂应无毒、无味、无腐蚀性及环境友好。下列说法错误的是( )
A.硅胶可用作食品干燥剂
B.P2O5不可用作食品干燥剂
C.六水氯化钙可用作食品干燥剂
D.加工后具有吸水性的植物纤维可用作食品干燥剂
A.18 g H2O中含有10NA个质子
B.1 mol甲苯中含有6NA个C—H键
C.标准状况下,22.4 L氨水中含有NA个NH3分子
D.将56 g铁片投入足量浓H2SO4中生成NA个SO2分子

8.按照混合物、纯净物、强电解质、弱电解质、非电解质的顺序排列正确的一组是( )
A.盐酸、氯气、BaSO4、CO2、SO2
B.硫酸、氨水、醋酸、乙醇、NO2
C.漂白粉、胆矾、NH4Cl、CH3COOH、CO2
D.干冰、氯水、HCl、HClO、CO
A.标况下,22.4L 的H2O 含有的水分子数为NA
B.标况下,11.2LCCl4 中含有的Cl 原子数为2NA.
C. 17gNH3中含有的电子总数为l0NA
D. 0.5mol/L的H2SO4溶液中含有的H+数为NA
A.二者的碳元素的质量分数相同
B.在标准状况下,等体积的两种物质含有的分子数相等
C.等物质的量时,二者质量之比为=
D.等质量时,二者完全燃烧消耗相同状况下的氧气体积相等
11.下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是( )
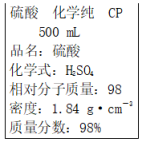
A.该硫酸的物质的量浓度为9.2 mol·L-1
B.1 mol Zn与足量该硫酸反应产生2 g氢气
C.配制200 mL 4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D.该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol·L-1
A.漂白粉、盐酸、碘酒和液氯都属于混合物
B.向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液,可制备Fe(OH)3胶体
C.熔融氯化钠,盐酸和铜都能导电,所以都属于电解质
D.一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路
A.1 mol二甲醚中含有的C—O键的数目为2NA
B.0.1 mol·L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA
C.200 g质量分数为23%的HCOOH水溶液中含氧原子的总数目为2NA
D.在反应Cu2S+O2高温,2Cu+SO2中,每生成1 mol Cu,转移电子的数目为2NA
14.Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的是( )
①化合物 ②能与硝酸反应 ③钠盐 ④电解质 ⑤离子化合物 ⑥氧化物
A.②⑤⑥ B.①②⑥ C.①③④ D.①④⑤
A.含有NA个氦原子的氦气在标准状况下的体积为11.2 L
B.298 K、1.01×105Pa时64 g SO2中含有的原子数为3NA
C.11.2 L Cl2含有的分子数为0.5NA
D.标准状况下,11.2 L乙醇中含有的分子数为0.5NA
16.如图所示,①和②为两个体积相同的固定容器,图中“![]() ”和“
”和“![]() ”分别表示氢原子和氧原子,则下列说法正确的是( )
”分别表示氢原子和氧原子,则下列说法正确的是( )
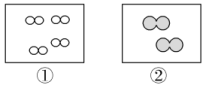
A.若①中的H2为1 mol,则②中所含原子总数为3.01×1023个
B.①和②中气体的质量之比为1∶8
C.H2、O2均能发生化合反应,但不能发生置换反应
D.两容器的温度和压强均相同
17.已知A是单质,E有强酸性和强氧化性。A、B、C、D、E是含有一种相同元素的五种物质,在一定条件下可发生如图所示的变化。则A可能是( )
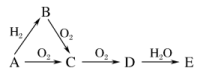
A.Cl2 B.C C.N2 D.Si
18.取m g相对原子质量为M的某金属与足量稀硫酸反应,在标准状况下产生a L氢气,该反应生成的硫酸盐中金属元素的化合价为( )
A.+ B.+ C.+ D.+
19.在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-1,质量分数为w,其中含有NH的物质的量是b mol,下列叙述正确的是( )
A.溶质的质量分数w=×100%
B.溶质的物质的量浓度c= mol·L-1
C.溶液中c(OH-)= mol·L-1+c(H+)
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
20.胞嘧啶是DNA水解产物之一,是精细化工的重要中间体。胞嘧啶可由5-巯基甲脲嘧啶、浓氨水和氯乙酸在一定条件下合成,则反应时NH3和5-巯基甲脲嘧啶的物质的量之比为( )
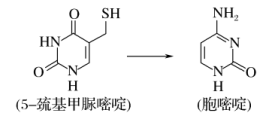
A.1∶1 B.2∶3 C.3∶1 D.2∶1
21.FeCl3是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的a L氯化氢气体溶于100 g水中,得到盐酸的密度为b g·mL-1,则该盐酸的物质的量浓度是________。
(2)向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为________。
(3)FeCl3溶液可以用来净水,其净水的原理为___________________(用离子方程式表示)。用100 mL 2 mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________(填“大于”“等于”或“小于”)0.2NA。
(1)0.2 g H2含有________个H原子。
(2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为________。
(3)100 mL硫酸铝溶液中n(Al3+)=0.20 mol(不考虑水解因素),则其中c(SO)=________。
(4)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为________,该金属元素的相对原子质量为________。
(5)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为________g。
23.A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
(1)分别写出三只烧杯中形成分散系的名称:
A________,B________,C________。
(2)写出C中形成分散系的化学方程式:___________________________________________。
(3)若不用化学试剂鉴别,写出鉴别B、C分散系的两种简单方法:
①______________________________________________,
②______________________________________________。
(4)向C中逐滴加入稀H2SO4,现象为_________________________________________。
解析:A、2.4 g镁的物质的量为2.4/24=0.1 mol,反应中失去0.2 mol电子,故错误;
B、标准状况下5.6 L二氧化碳的物质的量为5.6/22.4=0.25 mol,含有的氧原子为0.5 mol,故正确;
C、甲醇的结构为CH3OH,氢原子数为0.4NA的甲醇分子为0.1 mol,含有5molσ键,故错误;
D、醋酸是弱酸,不能完全电离,故错误。
解析:A.1 mol Na2O2与水完全反应时氧元素的化合价部分升高到0价,部分降低到-2价,转移电子数为NA,A错误;
B.常温下,4 g CH4即0.5mol甲烷含有NA个C-H共价键,B正确;
C.标况下氨水是液体,且是混合物,不能利用气体摩尔体积计算,C错误;
D.1 mol SO2与足量O2在一定条件下反应生成SO3,转移的电子数小于2NA个,因为![]() 是可逆反应,D错误。
是可逆反应,D错误。
解析:作为物质的量的单位,mol可以计量微观粒子(包括原子、分子、离子、原子团等),每摩尔物质约含有6.02×1023个“粒子”,这里的“粒子”并不一定是分子,A项错误;使用“mol”作单位时,所指粒子必须明确,且粒子种类要用适当的符号或化学式表示,“1 mol氧”的说法错误,B项错误;2H只表示2个氢原子,D项错误。
解析:A项,硅胶疏松多孔,吸附水分能力强,且无毒、无味、无腐蚀性,可用作食品干燥剂,正确;B项,P2O5具有吸水性,吸水生成对人体有一定危害的磷酸或偏磷酸,因此不可用作食品干燥剂,正确;C项,六水氯化钙没有吸水性,不可用作食品干燥剂,错误;D项,吸水性的植物纤维无毒、无味、无腐蚀性,可用作食品干燥剂,正确。
解析:每个水分子中含有10个质子,18 g H2O的物质的量为1 mol,1 mol H2O中含有10 mol质子,A项正确;1 mol甲苯中含有8NA个C—H键,B项错误;标准状况下,氨水为液体,不能用气体摩尔体积计算,C项错误;Fe在浓H2SO4中会发生钝化,不能生成SO2,D项错误。
解析:CO2是非电解质,故A错误;
硫酸、氨水、醋酸、乙醇、NO2分别属于纯净物、混合物、弱电解质、非电解质、非电解质,故B错误;
漂白粉、胆矾、NH4Cl、CH3COOH、CO2依次属于混合物、纯净物、强电解质、弱电解质、非电解质,故C正确;
干冰、氯水、HCl、HCl![]() O、CO依次属于纯净物、混合物、强电解质、弱电解质、非电解质,故D错误。
O、CO依次属于纯净物、混合物、强电解质、弱电解质、非电解质,故D错误。
解析:A.标况下,水不是气体,22.4L 的H2O的物质的量不是1mol,故A错误;
B.标况下,CCl4不是气体,11.2LCCl4的物质的量不是0.5mol,故B错误;
C. 17gNH3的物质的量为![]() =1mol,含有的电子总数为l0NA,故C正确;
=1mol,含有的电子总数为l0NA,故C正确;
D. 为告知溶液的体积,无法计算0.5mol/L的H2SO4溶液中含有的H+数,故D错误。
解析:C2H2与C6H6的最简式均为CH,故二者的碳元素的质量分数相同,A项正确;标准状况下,C6H6为非气体,等体积的两种物质的物质的量不相等,所以含有的分子数也不相等,B项错误;假设二者均为1 mol,则C2H2的质量为26 g,C6H6的质量为78 g,质量之比==,C项正确;假设二者质量均为78 g,则C2H2为3 mol,C6H6为1 mol,3 mol C2H2完全燃烧消耗7.5 mol O2,1 mol C6H6完全燃烧也消耗7.5 mol O2,D项正确。
解析:A项,c==18.4 mol·L-1;B项,Zn与浓H2SO4反应放出SO2气体;C项,200 mL×4.6 mol·L-1=x·18.4 mol·L-1,x=50 mL;D项,由于水的密度小于H2SO4的密度,所以当浓H2SO4与水等质量混合时,其体积大于浓H2SO4体积的2倍,所以其物质的量浓度小于9.2 mol·L-1。
解析:A.漂白粉、盐酸、碘酒都属于混合物,液氯是氯气分子构成的,属于纯净物,A错误;
B.向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液生成氢氧化铁和红褐色沉淀,不能制备Fe(OH)3胶体,B错误;
C.熔融氯化钠,盐酸和铜都能导电,其中氯化钠属于电解质,盐酸是混合物,铜是金属,均既不是电解质,也不是非电解质,C错误;
D.蛋白质形成的分散系是胶体,则一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路,D正确。
解析:二甲醚的结构简式为CH3—O—CH3,1 mol二甲醚中含有的C—O键的数目为2NA,A对;B项没有给出溶液的体积,错误;C项溶液中还有大量水,水中也含有氧原子,错误;D项每生成1 mol Cu,转移电子的数目为3NA,错误。
解析:①Na2O、NaOH、Na2CO3、NaCl、Na2SO4都是由两种或两种以上元素构成的纯净物,属于化合物,①正确。②Na2O、NaOH与硝酸反应均生成NaNO3和H2O,Na2CO3和硝酸反应可生成NaNO3、CO2和H2O,NaCl、Na2SO4与硝酸不反应,②错误。Na2CO3、NaCl、Na2SO4是钠盐,Na2O属于钠的氧化物,NaOH属于碱,故③⑥错误。④Na2O、NaOH、Na2CO3、NaCl、Na2SO4在水溶液中或熔融状态下能导电,属于电解质,④正确。⑤Na2O、NaOH、Na2CO3、NaCl、Na2SO4都属于离子化合物,⑤正确。即分类标准正确的是①④⑤,故本题选D。
解析:含有NA个氦原子的氦气的物质的量为1 mol,其在标准状况下的体积为22.4 L,A项错误;64 g SO2的物质的量为1 mol,其中含有1 mol S原子和2 mol O原子,B项正确;未指明温度和压强,不能根据标准状况下的气体摩尔体积进行计算,C项错误;乙醇在标准状况下不是气体,不能根据标准状况下的气体摩尔体积进行计算,D项错误。
解析:根据图示可知,①和②中H2与O2的分子个数之比为2∶1,若H2为1 mol,则O2为0.5 mol,故O原子数目为6.02×1023个,A项错误;①和②中H2与O2的分子个数之比为2∶1,所以其物质的量之比为2∶1,质量之比为1∶8,B项正确;H2能发生置换反应,如H2与CuO反应,O2也能发生置换反应,如O2与H2S反应,C项错误;根据阿伏加德罗定律,①和②两容器体积相同,但气体分子个数不同,所以两容器的温度和压强不可能均相同,D错误。
解析:A是单质,能和氢气反应,则A是非金属单质,A能被氧气氧化生成C,C能被氧化生成D,则A在氧化物中是显不同价态,E有强酸性和强氧化性,则A中元素是非金属性较强的元素。A项,氯气和氢气反应生成氯化氢,氯化氢和氧气不反应,错误;B项,碳和氧气反应生成一氧化碳,CO和O2反应生成二氧化碳,CO2和H2O反应生成碳酸,但碳酸是弱酸,错误;C项,N2和H2反应生成NH3,NH3和O2反应生成一氧化氮,氮气和氧气反应生成一氧化氮,NO和O2反应生成NO2,NO2和H2O反应生成硝酸,硝酸是强酸且是强氧化性酸,正确;D项,硅和氧气反应时,无论氧气是否过量都生成SiO2,且SiO2和H2O不反应,硅酸是弱酸,错误。
解析:设生成的硫酸盐中金属元素的化合价为+x,根据得失电子守恒,
mol×x=×2,解得:x=,则金属元素的化合价为+。
解析:氨水中溶质为氨气,该溶液的密度为ρ g·mL-1,体积为V mL,所以溶液质量为ρV g,溶质氨气的质量为a g,溶质的质量分数×100%=×100%,故A不正确;
a g NH3的物质的量为 mol,溶液体积为V mL,所以溶质的物质的量浓度为= mol·L-1,故B不正确;
V mL溶液中c(OH-)=c(H+)+c(NH)=c(H+)+ mol·L-1,C正确;
混合前后溶质的质量不变,仍为a g,因水的密度比氨水的密度大,等体积的水的质量比氨水的大,混合后溶液的质量大于2ρV g,所以混合后溶质的质量分数小于0.5w,故D不正确。
解析:对比5-巯基甲脲嘧啶和胞嘧啶的分子式,不难看出胞嘧啶比5-巯基甲脲嘧啶多了一个N原子,多出的N原子一定来自于氨,所以反应时NH3和5-巯基甲脲嘧啶的物质的量之比为1∶1。
(1) mol·L-1
(2)2 mol·L-1
(3)Fe3++3H2OFe(OH)3(胶体)+3H+ 小于;
解析:
(1)注意盐酸的体积不是100 g水的体积,要用所得盐酸的质量和密度计算,还应注意单位换算。
(2)根据氧化还原反应的规律,氯气先氧化Fe2+,反应后溶液中Cl-和Br-的物质的量浓度相等,表明溶液中无Fe2+,有FeBr3、FeCl3,n(Cl-)=×2=0.3 mol=n(Br-),根据电荷守恒及原子守恒知,n(Fe3+)=0.2 mol=n(Fe2+),则c(FeBr2)==2 mol·L-1。
(3)Fe3+在水中发生水解:Fe3++3H2OFe(OH)3(胶体)+3H+,生成的Fe(OH)3胶体具有吸附作用,可吸附溶液中的杂质离子。Fe3+的水解是可逆反应,且Fe(OH)3胶体中的胶体粒子是由多个Fe(OH)3组成的集合体,所以生成的Fe(OH)3胶体粒子数目小于0.2NA。
(1)0.2NA;
(2)2∶1;
(3)3.0 mol·L-1
(4)95 g·mol-1 24;
(5)11.2;
解析:
(1)0.2 g H2的物质的量为0.1 mol,含有0.2 mol H原子,即0.2NA个。
(2)含有相同氧原子数的CO与CO2的物质的量之比为2∶1,标准状况下,体积之比为2∶1。
(3)100 mL硫酸铝溶液中,n(Al3+)=0.20 mol,则其中n(SO)=0.30 mol,c(SO)=3.0 mol·L-1。(4)二价金属的氯化物可表示为MCl2,在9.5 g某二价金属的氯化物中含0.2 mol Cl-,
则该氯化物的物质的量为0.1 mol,摩尔质量为95 g·mol-1;
该金属元素的相对原子质量为95-71=24。
(5)CO与Fe2O3反应的化学方程式为3CO+Fe2O3△,2Fe+3CO2,
标准状况下6.72 L CO的物质的量为0.3 mol,完全反应后生成0.2 mol铁,即11.2 g。
(1)悬浊液 溶液 胶体
(2)FeCl3+3H2O△,Fe(OH)3(胶体)+3HCl
(3)①观察颜色,红色的液体为B,红褐色的液体为C
②用一束光照射两液体,有光亮通路的液体为C,另一液体为B
(4)先生成红褐色沉淀,然后沉淀逐渐溶解至沉淀消失形成棕黄色溶液
(通用版)高考化学一轮复习检测19 化学实验(含答案解析): 这是一份(通用版)高考化学一轮复习检测19 化学实验(含答案解析),共12页。试卷主要包含了2 g Na2O与7,82 mL浓盐酸等内容,欢迎下载使用。
(通用版)高考化学一轮复习检测17 电化学基础(含答案解析): 这是一份(通用版)高考化学一轮复习检测17 电化学基础(含答案解析),共15页。试卷主要包含了4 g时,用电器流过2,24 L气体,则溶液中转移0等内容,欢迎下载使用。
(通用版)高考化学一轮复习检测14 化学能与热能(含答案解析): 这是一份(通用版)高考化学一轮复习检测14 化学能与热能(含答案解析),共11页。试卷主要包含了92 kJ·ml-1,4 kJ·ml-1,2 kJ·ml-1;,3 kJ·ml-1,1 kJ·ml-1,5 kJ·ml-1,45 kJ·ml-1等内容,欢迎下载使用。












