


(通用版)高考化学一轮复习检测06 镁铝及其化合物(含答案解析)
展开高考化学复习检测:06
镁铝及其化合物
1.多年前,世界卫生组织把铝确定为食品的污染源之一而加以控制使用。铝在下列应用中应加以控制的是( )
①制铝合金 ②制电线 ③制炊具 ④制银色漆颜料 ⑤用明矾净水 ⑥用明矾与苏打作食品膨松剂 ⑦制易拉罐 ⑧用氢氧化铝凝胶制胃舒平药品 ⑨包装糖果和食品
A.③⑤⑧⑨ B.②⑥⑧⑨ C.③④⑤⑨ D.③⑤⑥⑦⑧⑨
2.某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。

下列说法正确的是( )
A.NaOH溶液可以用氨水来代替
B.溶液a中含有Al3+、K+、Cl-、Na+、OH-
C.溶液b中只含有NaCl
D.向溶液a中滴加盐酸需控制溶液的pH
3.镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如图所示。下列判断不合理的是( )

A.Al、Ga均处于第ⅢA族
B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可与NaOH溶液反应生成NaGaO2
D.由流程图可知酸性:Al(OH)3>Ga(OH)3
4.向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的物质的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )

A.a点对应的溶液中:Na+、Mg2+、SO、HCO
B.b点对应的溶液中:Na+、NH、SO、Cl-
C.c点对应的溶液中:Ag+、Ca2+、NO、Cl-
D.d点对应的溶液中:K+、NH、I-、SO
5.铝自然形成的氧化膜易脱落。以硫酸为电解液,分别以石墨和铝材作阴、阳极材料,经过电解处理形成氧化铝膜,抗蚀能力强。其制备的简要流程如图所示。下列用来解释流程中反应的方程式不正确的是( )

A.碱洗目的是除去铝材表面的自然氧化膜:2OH-+Al2O3===2AlO+H2O
B.碱洗时铝材表面会出现气泡:2Al+2OH-+2H2O===2AlO+3H2↑
C.获得耐蚀铝材的电极反应:4Al-12e-+3O2===2Al2O3
D.用稀氨水洗去耐蚀铝材表面的酸:NH3·H2O+H+===NH+H2O
6.下列物质组合中,既能和酸反应又能和碱反应的化合物共有( )
①(NH4)2CO3 ②Al2O3 ③Al2(SO4)3 ④Al ⑤NaHSO3 ⑥Al(OH)3
A.3种 B.4种 C.5种 D.6种
7.a g镁铝合金投入x mL 2 mol·L-1的盐酸中,金属完全溶解,再加入y mL 1 mol·L-1 NaOH溶液,沉淀达到最大值,质量为(a+1.7) g,则下列说法不正确的是( )
A.镁铝合金与盐酸反应转移电子数为0.1NA
B.沉淀为Mg(OH)2和Al(OH)3的混合物
C.x=2y
D.a的取值范围为0.9<a<1.2
8.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间因果关系的判断,完全正确的是( )

A.铝罐可久盛食醋
B.焰火的五彩缤纷是某些金属元素化学性质的展现
C.氧化铝熔点很高,可作耐火材料
D.明矾作净水剂,可以除去废水中的铜离子
10.现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断中不合理的是( )

A.N一定是HCl(aq)
B.X可能为Al或Cl2
C.Y一定为NaOH(aq)
D.Q、Z中的一种必定为Al2O3

12.工业上用铝土矿(主要成分为Al2O3,含SiO2、Fe2O3等杂质)为原料冶炼铝的工艺流程如图所示。

对上述流程中的判断正确的是( )
①试剂X为稀硫酸,沉淀中含有硅的化合物
②反应Ⅱ中生成Al(OH)3的反应为CO2+AlO+2H2O===Al(OH)3↓+HCO
③结合质子(H+)的能力由强到弱的顺序是OH->AlO>CO
④Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
A.①② B.②③ C.①④ D.③④
A.向氯化铝溶液中加入过量氨水反应的实质是Al3++3NH3·3H2O=== Al(OH)3↓+3NH
B.存在于污水中的重金属离子,常用加入明矾等电解质的方法进行处理
C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液
D.依据铝热反应原理,能发生反应2Al+3MgO高温,3Mg+Al2O3
14.某无色溶液含有下列离子中的若干种:H+、NH、Cu2+、Ba2+、Al3+、CO、Cl-、OH-、NO。向该溶液中加入铝粉,只放出H2,则溶液中能大量存在的离子最多有( )
A.3种 B.4种 C.5种 D.6种

A.Al跟NaOH溶液共热
B.Al(NO3)3跟过量的NaOH溶液反应
C.Al2O3和水共热
D.Al2(SO4)3和过量的氨水反应
17.有一块镁铝合金,其中镁与铝的质量比是8∶9。加入足量稀H2SO4使其完全溶解后,再加入NaOH溶液,生成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是( )

18.向等物质的量浓度的HCl、AlCl3、NH4Cl、MgCl2混合溶液中逐滴加入1 mol·L-1的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。下列有关说法正确的是( )

A.在0~a段加入的NaOH溶液与NH4Cl反应
B.在b~c段加入NaOH溶液发生反应的离子方程式为Al3++3OH-=== Al(OH)3↓
C.在d~e段加入NaOH溶液发生反应的离子方程式为Al3++4OH-===AlO+2H2O
D.在滴加NaOH溶液全过程中主要粒子参与反应的先后顺序是H+、Al3+、Mg2+、NH、Al(OH)3
19.铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼金属铝。下列说法错误的是( )
![]()
A.①中还需要进行过滤操作,滤渣为二氧化硅
B.a、b中铝元素的存在形式不同
C.③中需要通入过量的氨气
D.④进行的操作是加热,而且d一定是氧化铝
20.有关NaHCO3和Na2CO3的性质,以下叙述错误的是( )
A.等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积小
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍
C.等质量NaHCO3和Na2CO3与盐酸完全反应,前者消耗盐酸较多
D.等物质的量的NaHCO3和Na2CO3与足量盐酸反应产生CO2一样多
21.利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:

(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式
为____________。
“水解”采用90 ℃而不在室温下进行的原因是____________________。
(2)“酸溶”时,Al2O3发生反应的离子方程式为
____________________________________。
(3)“氧化”时,发生反应的离子方程式为__________________________________。
(4)“废渣”成分为________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是_______________________________________。
22.某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应。资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。该兴趣小组设计了如下实验方案验证产物并探究反应原理。
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红色变为红色。
(1)该小组对反应中产生的白色不溶物作出如下假设:
假设1:可能为_______________________________________。
假设2:可能为MgCO3。
假设3:可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证假设:

(3)设计定量实验确定实验Ⅰ的产物:称取实验Ⅰ中所得干燥、纯净的白色不溶物6.20 g,充分加热灼烧至不再产生气体为止,并使分解产生的气体全部进入装置A(盛足量浓硫酸)和B(盛足量碱石灰)中,装置A增重0.36 g,装置B增重2.64 g,则白色不溶物的化学式为________。
23.如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
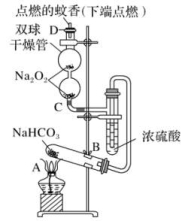
(1)在A试管内发生反应的化学方程式是__________________________________________。
(2)B装置的作用是______________________________。
(3)在双球干燥管内发生反应的化学方程式为________________________________________。
(4)双球干燥管内观察到的实验现象是___________________________________________。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是________________。
24.铝(熔点660 ℃)是一种应用广泛的金属,工业上用Al2O3(熔点2045 ℃)和冰晶石(Na3AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(1)冶金工业上常用金属铝作还原剂冶炼钒、铬、锰,铝与V2O5在高温下反应的化学方程式
为_________________________________________________。
(2)将打磨过的铝片在酒精灯火焰上加热,可观察到铝熔化而不滴落,
原因是____________________________________________;铝是活泼金属,但打磨过的铝片投入沸水中不易观察到有气泡产生。若将铝片用饱和Hg(NO3)2溶液浸泡数分钟,取出后迅速洗净,可制得俗称“铝汞齐”的铝汞合金。铝汞齐露置在空气中,表面会快速生长出蓬松的白毛(Al2O3)。若将新制的铝汞齐放入水中,可迅速反应产生气泡,该反应的化学方程式
为________________________________;
铝汞齐的化学性质变得“活泼”的原因可能是_________________________。
(3)饮用水中的NO对人体健康会产生危害。为了降低饮用水中NO的浓度,有研究人员建议在碱性条件下用铝粉将NO还原为N2,该反应的离子方程式为____________________________。
(4)将0.1 mol·L-1 AlCl3溶液和10% NH4F溶液等体积混合,充分反应后滴加氨水,无沉淀析出。
则AlCl3与NH4F反应的化学方程式为_______________________________________。
解析:解答本题时,要抓住题中的“把铝确定为食品的污染源之一”与“控制使用”。D项符合题意。
解析:A项,氨水也沉淀Al3+,不能代替NaOH溶液;B项,a中不含Al3+;C项,b也含有KCl。
解析:镓(Ga)与铝同主族,均位于第ⅢA族,A正确;
Ga2O3与Al2O3的性质具有相似性,可与盐酸反应生成GaCl3,B正确;
Ga(OH)3与Al(OH)3的性质相似,属于两性氢氧化物,能与NaOH溶液反应生成NaGaO2,C正确;
化学反应遵循强酸制弱酸原理,在NaAlO2和NaGaO2的混合溶液中通入CO2,有Al(OH)3生成,而无Ga(OH)3生成,可能是Ga(OH)3酸性强于碳酸,则酸性:Al(OH)3<Ga(OH)3,D错误。
解析:向NaOH溶液中逐滴加入AlCl3溶液,依次发生反应:Al3++4OH-===AlO+2H2O、3AlO+6H2O+Al3+===4Al(OH)3↓。a点时溶液中有大量OH-,与Mg2+、HCO不能大量共存,A错误;
b点时溶质为NaCl和NaAlO2,AlO与NH不能大量共存,B错误;
c点时溶质为NaCl,Cl-与Ag+不能大量共存,C错误;
d点时溶质为NaCl和AlCl3,所有离子可以大量共存,D正确。
解析:A.氧化铝能够溶于氢氧化钠,离子方程式为2OH-+Al2O3===2AlO+H2O,正确;B.铝能够与氢氧化钠反应放出氢气,离子方程式为:2Al+2OH-+2H2O===2AlO+3H2↑,正确;C.电极反应方程式也要满足电荷守恒,4Al-12e-+3O2===2Al2O3,电荷不守恒,错误;D.氨水是弱电解质,用化学式表示,离子方程式为NH3·H2O+H+===NH+H2O,D正确;故选C。
解析:Al为单质,排除④;(NH4)2CO3与酸反应生成CO2,与碱反应生成NH3;Al2O3、Al(OH)3为两性物质,均能与强酸、强碱反应;NaHSO3与酸反应生成SO2,与碱反应生成Na2SO3;Al2(SO4)3只能与碱反应,不能与酸反应。故既能与酸反应也能与碱反应的化合物是①②⑤⑥,B正确。
解析:Mg、Al失去电子变为离子,离子再结合OH-生成沉淀,则镁铝合金与盐酸反应转移电子的物质的量等于其生成沉淀时结合的OH-的物质的量,沉淀量最大时得到Mg(OH)2和Al(OH)3的混合物,则m(OH-)=(a+1.7) g-a g=1.7 g,n(OH-)=0.1 mol,电子转移总数是0.1NA,A、B正确;
沉淀量最大时,溶液中n(Na+)=n(Cl-),此时HCl和氢氧化钠的物质的量相等,即2x=y,C错误;
电子转移总数是0.1NA,若金属全部是镁,则镁的质量是1.2 g,若金属全部是铝,则铝的质量是0.9 g,D正确。
解析:铝箔在酒精灯火焰上加热熔化但不滴落是因为Al2O3的熔点高于金属Al,故B错;
明矾水解产生Al(OH)3胶体,可净化水,但不能进行消毒,故C错;
铁、铝遇浓硫酸、浓硝酸钝化,并不是不反应,故D错。
解析:铝罐的主要成分铝可与醋酸反应,故铝罐不能久盛食醋,A项错误;焰火的五彩缤纷是因为某些金属元素的焰色反应,焰色反应是金属元素的物理性质,B项错误;氧化铝熔点很高,可用于制耐火砖、耐火坩埚、耐火管、耐高温实验仪器,C项正确;明矾净水利用的是Al(OH)3胶体的吸附性,其可吸附水中不溶于水的杂质形成沉淀,从而起到净水的作用,D项错误。
解析:在Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)中,只有NaOH(aq)能与Al、Cl2、Al2O3、HCl(aq)、Al(OH)3五种物质反应,对照图示转化关系,可知Y为NaOH(aq)。只有HCl(aq)能与Al、Al2O3、Al(OH)3、NaOH(aq)四种物质反应,对照图示转化关系可知N为HCl(aq),故选项A、C正确;选项B,若X为Al,Al能与Cl2、HCl(aq)、NaOH(aq)三种物质反应,而图示给出的是与两种物质反应,所以X不可能是Al,但可能是Cl2;选项D,Al2O3既能与HCl(aq)反应,也能与NaOH(aq)反应,故Q、Z中的一种必定为Al2O3。
解析:金属性的强弱可根据金属与酸反应时金属失电子的能力强弱判断,而不是与碱反应,故A错误;没有脱落表明氧化铝的熔点高,故B错误;氯化铵溶液显酸性,与铝反应时放出氢气,故C错误;氯化铝和氢氧化钠溶液反应先生成氢氧化铝白色沉淀,氢氧化铝再和氢氧化钠溶液反应生成可溶性的偏铝酸钠,故D正确。
解析:由溶液乙通入过量的Y生成氢氧化铝沉淀和碳酸氢钠可知,溶液乙中含有AlO,气体Y为二氧化碳,故试剂X为氢氧化钠溶液,不可能为硫酸,故①错误;
过量的二氧化碳与偏铝酸钠反应生成氢氧化铝沉淀与碳酸氢钠,反应离子方程式为CO2+AlO+2H2O===Al(OH)3↓+HCO,故②正确;
结合质子的能力就是指碱性强弱,碱性:OH->AlO>CO,所以结合质子的能力:OH->AlO>CO,故③正确;
AlCl3是共价化合物,熔融时不能电离出Al3+,电解熔融的AlCl3不能获得金属铝,故④错误。
解析:B项中明矾只能使污水中的悬浮物沉降,不能除去重金属离子;C项中Mg不能溶于NaOH溶液;D项中Mg的金属性比Al强,故Al与MgO不能发生铝热反应。
解析:Cu2+在溶液中为蓝色,则溶液中一定不含有Cu2+。能与铝粉反应放出H2,则溶液中含有H+或OH-。若溶液中含有H+,则不含CO、OH-、NO,一定含有Cl-,可能含有NH、Ba2+、Al3+。若溶液中含有OH-,则不含H+、NH、Al3+,结合溶液呈电中性知,一定含有Ba2+,一定不含CO,可能含有Cl-、NO。综上所述,溶液中能大量存在的离子最多有5种。
解析:Al跟NaOH溶液共热生成NaAlO2,得不到氢氧化铝,故A错误;
氢氧化铝是两性氢氧化物,溶于强酸或强碱,Al(NO3)3跟过量的NaOH溶液反应生成NaAlO2,得不到氢氧化铝,故B错误;
氧化铝不溶于水,不能与水反应生成氢氧化铝,故C错误;
Al2(SO4)3和过量的氨水反应可以得到氢氧化铝,氢氧化铝不溶于弱碱,故D正确。
解析:镁与铝的质量比是8∶9,则物质的量之比是1∶1,NaOH溶液过量后Al(OH)3完全溶解,只有Mg(OH)2,B错误;等物质的量的Mg(OH)2与Al(OH)3的质量之比是58∶78,即剩余的Mg(OH)2的质量小于沉淀最大质量的,排除C、D,故选A。
解析:A项错误,加入的NaOH溶液应先与H+反应;B项错误,由图像中耗用NaOH溶液的体积可知,在b~c段加入NaOH溶液发生反应的离子方程式为Mg2++2OH-===Mg(OH)2↓;C项错误,在d~e段加入NaOH溶液发生反应的离子方程式为Al(OH)3+OH-===AlO+2H2O;D项正确。
解析:铝土矿加盐酸生成Al3+和Fe3+,二氧化硅不溶于盐酸,所以要过滤、分离出二氧化硅;滤液中加过量NaOH,Al3+转化为AlO、Fe3+转化为Fe(OH)3沉淀,过滤除去Fe(OH)3沉淀,向滤液中通入过量的二氧化碳,生成Al(OH)3沉淀,Al(OH)3分解生成Al2O3,最后电解熔融的Al2O3生成Al。由以上分析可知①、②中除加试剂外,还需要进行过滤操作,故A正确;a中为Al3+,b中为AlO,故B正确;③中需要把AlO转化为Al(OH)3沉淀,要通入过量的二氧化碳,AlO+CO2+2H2O===Al(OH)3↓+HCO,故C错误;根据上面分析可知④是Al(OH)3受热分解生成Al2O3,故D正确。
解析:Na2CO3+2HCl===2NaCl+CO2↑+H2O
NaHCO3+HCl===NaCl+CO2↑+H2O
解答此类题目用归“1”法,
A项,假设二者都是1 g,则n(NaHCO3)=n(CO2)= mol,n(Na2CO3)=n(CO2)= mol,故A正确;
B项,假设二者均为1 mol,则消耗的盐酸Na2CO3为2 mol,NaHCO3为1 mol,故B正确;
C项,假设二者均为1 g,Na2CO3需盐酸为2× mol= mol,NaHCO3需盐酸 mol,故C错。
(1)AlN+3H2OAl(OH)3+NH3↑ 加快AlN水解反应速率;
降低NH3在水中的溶解度,促使NH3逸出
(2)Al2O3+6H+===2Al3++3H2O
(3)2Fe2++2H++ClO-===2Fe3++Cl-+H2O
(4)Fe(OH)3
(5)防止Al(OH)2Cl水解生成Al(OH)3
(1)Mg(OH)2
(2)①能安静燃烧、产生淡蓝色火焰,证明该气体为氢气 ②稀盐酸(或稀硫酸) ③CO
(3)3MgCO3·Mg(OH)2[或Mg(OH)2·3MgCO3或Mg4(OH)2(CO3)3]
解析:
(1)根据假设2和3,推出假设1:白色不溶物可能为Mg(OH)2。
(2)①HCO在水中存在水解平衡和电离平衡:HCO+H2OH2CO3+OH-、HCOH++CO,
Mg和OH-不反应,Mg和H+反应产生氢气,因此气体可能为氢气,若气体点燃后能安静燃烧、产生淡蓝色火焰,则该气体为氢气。②根据假设,应加入足量的稀盐酸或稀硫酸,沉淀全部消失,且产生气体,说明沉淀中含有碳酸镁。③加入CaCl2溶液,出现沉淀,说明溶液中含有CO。
(3)浓硫酸的作用是吸收水蒸气,根据H元素守恒,可得n[Mg(OH)2]=n(H2O)==0.02 mol,
碱石灰的作用是吸收CO2,根据C元素守恒,可得n(MgCO3)=n(CO2)==0.06 mol,
因此MgCO3∶Mg(OH)2=0.06∶0.02=3∶1,
化学式为3MgCO3·Mg(OH)2或Mg(OH)2·3MgCO3或Mg4(OH)2(CO3)3。
(1)2NaHCO3Na2CO3+H2O+CO2↑
(2)吸收气体中的水蒸气(干燥CO2)
(3)2Na2O2+2CO2===2Na2CO3+O2
(4)淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈
(5)点燃的蚊香逐渐熄灭
解析:NaHCO3受热发生分解反应产生的CO2经浓硫酸干燥后,与双球干燥管中Na2O2发生反应:2CO2+2Na2O2===2Na2CO3+O2,淡黄色的Na2O2固体逐渐变为白色粉末,同时由于O2的产生,使点燃的蚊香燃烧更加剧烈;若换为Na2O,则只发生反应CO2+Na2O===Na2CO3,点燃的蚊香逐渐熄灭。
(1)10Al+3V2O55Al2O3+6V
(2)铝表面很快形成致密氧化膜,其熔点高于铝 2Al+6H2O===2Al(OH)3+3H2↑
其表面不易形成致密的氧化膜(合理即可)
(3)10Al+6NO+4OH-===3N2↑+10AlO+2H2O
(4)AlCl3+6NH4F===(NH4)3AlF6+3NH4Cl
解析:
(1)金属铝作还原剂化合价升高生成Al2O3,V2O5作氧化剂化合价降低生成V。
(2)Al2O3的熔点高于金属铝,所以铝熔化而不滴落;金属铝与水发生置换反应:2Al+6H2O===2Al(OH)3+3H2↑;单质铝的化学性质活泼,会与O2迅速反应生成Al2O3致密氧化膜,阻碍Al与H2O发生反应,当制成铝汞齐后,Al与O2反应生成蓬松的Al2O3,此时将其放入水中,Al与H2O接触发生反应生成H2。
(3)金属铝作还原剂在碱性条件下生成AlO,硝酸根离子作氧化剂被还原为N2,再根据氧化还原方程式配平原则配平离子方程式。
(4)加入氨水后,无沉淀生成,说明溶液中不存在Al3+,依据元素守恒和冰晶石的化学式,可写出反应的化学方程式。
(通用版)高考化学一轮复习一遍过专题09镁铝及其重要化合物(含解析): 这是一份(通用版)高考化学一轮复习一遍过专题09镁铝及其重要化合物(含解析),共19页。试卷主要包含了以下说法正确的是,下列实验现象的描述中不正确的是,铝热反应的实验装置如图等内容,欢迎下载使用。
(通用版)高考化学一轮复习课时分层提升练七3.2镁铝及其重要化合物(含解析): 这是一份(通用版)高考化学一轮复习课时分层提升练七3.2镁铝及其重要化合物(含解析),共11页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
通用版高考化学考点复习训练五钠镁铝及其化合物含答案: 这是一份通用版高考化学考点复习训练五钠镁铝及其化合物含答案,共18页。












