


人教版九年级化学上册单元检测 第三单元综合素质评价
展开
这是一份人教版九年级化学上册单元检测 第三单元综合素质评价,共14页。
第三单元综合素质评价限时:45分钟 满分:100分一、选择题 (本题包括12小题,1~ 8题每题2分,9~ 12题每题3分,共28分)1. 济阳仁风镇是“中国西瓜之乡”,种植的西瓜,硒的含量高,色泽好,糖分高,口感好,被农业部认证为国家级“无公害农产品”和“绿色食品”。这里的“硒”指的是( )A. 原子 B. 离子 C. 分子 D. 元素2. 下列物质中含氧分子的是( )A. 空气 B. 氯酸钾 C. 过氧化氢 D. 高锰酸钾3. 水蒸发的过程中发生改变的是( )A. 分子种类 B. 分子间间隔 C. 分子数目 D. 原子大小4. 【2023·南昌模拟】制造“北斗三号”卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )A. 22 B. 48 C. 70 D. 265. 下列说法中正确的是( )A. 原子的质量主要集中在原子核上 B. 原子核中的质子数与中子数一定相等C. 元素的种类由相对原子质量来决定 D. 元素的化学性质取决于原子的核外电子数6. 宏微结合是化学学科特有的思维方式。下列事实的微观解释不正确的是( )A. 端午时节粽飘香——分子在不停地运动B. 氧气压缩为液氧——氧分子的体积变小C. 过氧化氢分解产生水和氧气——化学变化中分子的种类发生了改变D. 氧气能支持燃烧,二氧化碳不能支持燃烧——不同种分子化学性质不同7. 下列对分子、原子、离子的认识,不正确的是( )A. 分子、原子、离子都能构成物质 B. 水结冰后分子不再运动C. 温度越高,分子运动越快 D. 钠原子和钠离子的化学性质不同8. 【2023·龙岩模拟】据报道,一种新型铝离子电池,比现今普遍使用的锂离子电池具有更加优良的性能,未来,该铝离子电池或将成为下一代高性价比电池的理想选择,下图是元素周期表中锂、铝两种元素的有关信息,下列说法不正确的是( ) A. 锂、铝元素在周期表中分别位于第二、三周期
A. 锂、铝元素在周期表中分别位于第二、三周期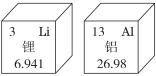 B. 相对原子质量铝比锂多20. 039 gC. 锂、铝两种元素都是金属元素D. 核外电子数Al3+比Li+多89. 【2023·宜昌模拟】如图是五种微粒的结构示意图,下列说法正确的是( )
B. 相对原子质量铝比锂多20. 039 gC. 锂、铝两种元素都是金属元素D. 核外电子数Al3+比Li+多89. 【2023·宜昌模拟】如图是五种微粒的结构示意图,下列说法正确的是( )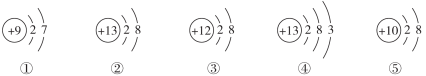
 A. ①④属于金属元素 B. ②的微粒符号是Al3+C. ②③⑤属于阳离子 D. ②③属于同种元素10. 下列说法正确的是( )A. 铁离子:Fe+3 B.
A. ①④属于金属元素 B. ②的微粒符号是Al3+C. ②③⑤属于阳离子 D. ②③属于同种元素10. 下列说法正确的是( )A. 铁离子:Fe+3 B. 
 硅的相对原子质量是14C. 镁离子结构示意图:
硅的相对原子质量是14C. 镁离子结构示意图: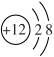
 D. 2个氮原子:N211. 【2023·桐城模拟】1911年,英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。根据实验,不能获得的结论是( )A. 金原子核带正电 B. 金原子核外电子带负电C. 金原子核体积很小 D. 金原子核的质量比α粒子大得多
D. 2个氮原子:N211. 【2023·桐城模拟】1911年,英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。根据实验,不能获得的结论是( )A. 金原子核带正电 B. 金原子核外电子带负电C. 金原子核体积很小 D. 金原子核的质量比α粒子大得多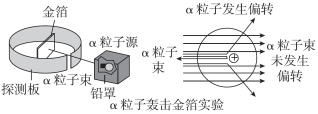
 (第11题)
(第11题)
 (第12题)12. 如图是工业上生产尿素[CO(NH2)2]肥料的反应微观示意图,下列有关分析正确的是( )A. 反应后,原子总数增加 B. 化学变化中,原子、分子都可再分C. 尿素中含有4个氢原子 D. 在一定条件下,物质间可以相互转化二、填空题 (本题包括4小题,共39分)13. (9分)建立“宏观—微观—符号”之间的联系是化学学科的重要特点。(1)用化学符号和数字表示下列微粒。两个氢原子_______________;两个铝离子_______________;两个硝酸根离子_____________;(2)说出下列符号中数字的意义。2Mg2+中前一个“2”表示____________,右上角的“2”表示_______________________________。(3)“水循环”和“碳循环”是自然界中存在的两大重要循环。①从微观的角度看:水分子是由______________________构成的;②从宏观的角度看:二氧化碳是由____________________组成的。14. (12分)回答下列问题:(1)分子、原子、离子都是构成物质的微观粒子,例如氢气是由________(填具体粒子的名称)构成的,氯化钠是由___________________(填具体粒子的名称)构成的。图1中B处应填入________(填“原子”“分子”或“离子”)。
(第12题)12. 如图是工业上生产尿素[CO(NH2)2]肥料的反应微观示意图,下列有关分析正确的是( )A. 反应后,原子总数增加 B. 化学变化中,原子、分子都可再分C. 尿素中含有4个氢原子 D. 在一定条件下,物质间可以相互转化二、填空题 (本题包括4小题,共39分)13. (9分)建立“宏观—微观—符号”之间的联系是化学学科的重要特点。(1)用化学符号和数字表示下列微粒。两个氢原子_______________;两个铝离子_______________;两个硝酸根离子_____________;(2)说出下列符号中数字的意义。2Mg2+中前一个“2”表示____________,右上角的“2”表示_______________________________。(3)“水循环”和“碳循环”是自然界中存在的两大重要循环。①从微观的角度看:水分子是由______________________构成的;②从宏观的角度看:二氧化碳是由____________________组成的。14. (12分)回答下列问题:(1)分子、原子、离子都是构成物质的微观粒子,例如氢气是由________(填具体粒子的名称)构成的,氯化钠是由___________________(填具体粒子的名称)构成的。图1中B处应填入________(填“原子”“分子”或“离子”)。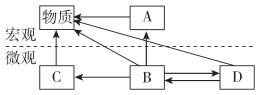
 图1
图1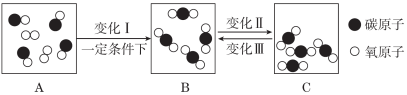
 图2(2)如图2是某密闭容器中物质变化过程的微观示意图:①A、B、C中表示混合物的是________;②上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是________,该化学变化中一定不变的粒子是________________(填粒子名称)。15. (8分)氮化镓(GaN)是“蓝色发光二极管”研发技术中的重要材料。(1)镓元素(Ga)的原子结构示意图为
图2(2)如图2是某密闭容器中物质变化过程的微观示意图:①A、B、C中表示混合物的是________;②上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是________,该化学变化中一定不变的粒子是________________(填粒子名称)。15. (8分)氮化镓(GaN)是“蓝色发光二极管”研发技术中的重要材料。(1)镓元素(Ga)的原子结构示意图为
 ,其中x=______;镓元素的原子序数为________,在元素周期表中位于第______周期;在化学变化中易________(填“得到”或“失去”)电子,形成离子的符号是________,镓原子失去电子后核内质子数为________,核外电子数为________。(2)下列原子结构示意图所对应的元素与镓元素的化学性质相似的是_____。
,其中x=______;镓元素的原子序数为________,在元素周期表中位于第______周期;在化学变化中易________(填“得到”或“失去”)电子,形成离子的符号是________,镓原子失去电子后核内质子数为________,核外电子数为________。(2)下列原子结构示意图所对应的元素与镓元素的化学性质相似的是_____。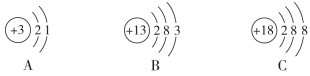
 16. (10分)【2023·张家口模拟】如图1是A、B、C、D四种元素的原子结构示意图及氟元素在元素周期表中的信息。根据图示回答下列问题。
16. (10分)【2023·张家口模拟】如图1是A、B、C、D四种元素的原子结构示意图及氟元素在元素周期表中的信息。根据图示回答下列问题。
 图1
图1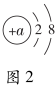 (1)与A化学性质相似的原子是________(填字母)。(2)A~E共表示________种元素。(3)根据E图示所给信息,写出氟离子的符号________。(4)原子得到或失去电子后形成离子。某离子的结构示意图如图2所示:①当a=________时,该粒子是原子。②当a=8时,该粒子是________(填“原子”“阳离子”或“阴离子”)。三、简答题 (本题包括2小题,共20分)17. (8分)有A、B、C、D四种元素,A是地壳中含量最多的金属元素,B元素原子第三电子层比第二电子层少一个电子,C元素的原子得到2个电子以及D元素的原子失去一个电子后所得离子均与氖原子具有相同的电子层结构,试回答:(1)写出上述四种元素的符号:A_______;B_______;C_______;D_______。(2)画出有关粒子结构示意图:A原子____________;B离子____________。18. (12分)【2023·泰安模拟】元素周期表是学习和研究化学的重要工具。如表是元素周期表中的一部分,请按表中信息填空。 族周期 ⅠAⅡAⅢAⅣAⅤAⅥAⅦA023 Li锂6. 9414 Be铍9. 0125 B硼10. 816 C碳12. 017 N氮14. 018 O氧16. 009 F氟19. 0010 Ne氖20. 18311 Na钠22. 9912 Mg镁24. 3113 Al铝26. 9814 Si硅28. 0915 P磷30. 9716 S硫32. 0617 Cl氯35. 4518 Ar氩39. 95(1)人体中含量最多的元素的核电荷数为________,属于________(填“金属”或“非金属”)元素。(2)原子序数为16的原子在化学变化中易________(填“得到”或“失去”)电子,形成的离子的符号是________。(3)锂元素和钠元素的化学性质相似,理由是________________________________________________________________________________________。(4)已知C-12原子的质量为a g,则磷原子的质量为________。(5)实验证明:在上表中同一横行,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强(稀有气体原子除外);在同一纵行中,从上到下,原子失去电子的能力逐渐增强,得到电子的能力逐渐减弱。上表中,失去电子能力最强的原子是________(填元素符号,下同),得到电子能力最强的原子是________。四、探究实验题 (本题包括1小题,共13分)19. (13分)图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ所示。
(1)与A化学性质相似的原子是________(填字母)。(2)A~E共表示________种元素。(3)根据E图示所给信息,写出氟离子的符号________。(4)原子得到或失去电子后形成离子。某离子的结构示意图如图2所示:①当a=________时,该粒子是原子。②当a=8时,该粒子是________(填“原子”“阳离子”或“阴离子”)。三、简答题 (本题包括2小题,共20分)17. (8分)有A、B、C、D四种元素,A是地壳中含量最多的金属元素,B元素原子第三电子层比第二电子层少一个电子,C元素的原子得到2个电子以及D元素的原子失去一个电子后所得离子均与氖原子具有相同的电子层结构,试回答:(1)写出上述四种元素的符号:A_______;B_______;C_______;D_______。(2)画出有关粒子结构示意图:A原子____________;B离子____________。18. (12分)【2023·泰安模拟】元素周期表是学习和研究化学的重要工具。如表是元素周期表中的一部分,请按表中信息填空。 族周期 ⅠAⅡAⅢAⅣAⅤAⅥAⅦA023 Li锂6. 9414 Be铍9. 0125 B硼10. 816 C碳12. 017 N氮14. 018 O氧16. 009 F氟19. 0010 Ne氖20. 18311 Na钠22. 9912 Mg镁24. 3113 Al铝26. 9814 Si硅28. 0915 P磷30. 9716 S硫32. 0617 Cl氯35. 4518 Ar氩39. 95(1)人体中含量最多的元素的核电荷数为________,属于________(填“金属”或“非金属”)元素。(2)原子序数为16的原子在化学变化中易________(填“得到”或“失去”)电子,形成的离子的符号是________。(3)锂元素和钠元素的化学性质相似,理由是________________________________________________________________________________________。(4)已知C-12原子的质量为a g,则磷原子的质量为________。(5)实验证明:在上表中同一横行,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强(稀有气体原子除外);在同一纵行中,从上到下,原子失去电子的能力逐渐增强,得到电子的能力逐渐减弱。上表中,失去电子能力最强的原子是________(填元素符号,下同),得到电子能力最强的原子是________。四、探究实验题 (本题包括1小题,共13分)19. (13分)图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ所示。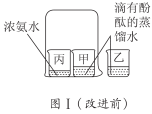
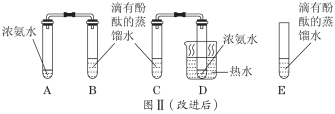
 【实验操作】a. 向B、C、E三支试管中分别加入5 mL蒸馏水,各滴入1~2滴无色酚酞试液,振荡,观察溶液颜色;b. 在A、D试管中分别加入2 mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。【分析讨论】(1)E试管放滴有酚酞的蒸馏水的目的是__________________________________________________________________________________。(2)进行操作b时观察到的现象是___________________________________。(3)由此可以得到的实验结论是:①__________________________________;②_________________________________-。(4)对比改进前的实验,改进后实验的优点是________________________________________________________________________________ (写两条)。
【实验操作】a. 向B、C、E三支试管中分别加入5 mL蒸馏水,各滴入1~2滴无色酚酞试液,振荡,观察溶液颜色;b. 在A、D试管中分别加入2 mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。【分析讨论】(1)E试管放滴有酚酞的蒸馏水的目的是__________________________________________________________________________________。(2)进行操作b时观察到的现象是___________________________________。(3)由此可以得到的实验结论是:①__________________________________;②_________________________________-。(4)对比改进前的实验,改进后实验的优点是________________________________________________________________________________ (写两条)。
答案一、1. D2. A 点拨:氧分子构成氧气,空气中含有氧气,故含有氧分子,A正确;B、C、D中均含有氧元素,不含氧分子,不符合题意。3. B 点拨:水蒸发是物理变化,从微观角度分析,分子的种类不变,分子间间隔变大,分子的数目和大小均不变,B正确。4. A 点拨:原子中,质子数=核外电子数,钛原子的质子数为22,则其核外有22个电子。5. A 点拨:原子中,电子的质量很小,可忽略不计,因此原子的质量主要集中在原子核上,A正确;原子核中,质子数与中子数不一定相等,B错误;元素的种类由质子数来决定,元素的化学性质与原子的最外层电子数关系密切,C、D错误。6. B 7. B8. B 点拨:相对原子质量不是原子实际质量,单位不是“g”;B错误;Al3+核外电子数为10,Li+核外电子数为2,Al3+比Li+多8个电子,D正确。9. B 点拨:①属于氟元素,属非金属元素,④属于铝元素,属于金属元素,A错误;②③中质子数大于核外电子数,属阳离子,⑤中质子数=电子数,属原子,C错误;②和③质子数不同,不属于同种元素,D错误。10. C 点拨:铁离子的符号为Fe3+,A错误;由图示可知硅的相对原子质量为28. 09,质子数为14,B不正确;![]()
 中质子数大于电子数,表示Mg2+,C正确;2个氮原子可表示为2N,D错误。11. B 点拨:α粒子轰击金箔后,大多数α粒子未发生偏转,说明金原子中有相对较大空间,即金原子核体积很小;部分α粒子发生偏转,说明受到斥力作用,可知金原子核带正电荷;有的α粒子被弹回,说明撞上了质量较大的粒子,即金原子核质量比α粒子大得多,A、C、D均正确;由该实验无法得知电子带负电,B符合题意。12. D 点拨:化学变化中,分子可以再分,原子不能再分,反应前后原子的种类和数量不变,A、B均错误;1个尿素分子中含有4个氢原子,C错误;由反应示意图可知,在一定条件下,物质间可以相互转化,D正确。二、13. (1)2H;2Al3+;2NO-3(2)2个镁离子;1个镁离子带2个单位正电荷(3)①氢、氧两种原子 ②碳、氧两种元素14. (1)氢分子;钠离子和氯离子;原子(2)①A ②Ⅰ;碳原子、氧原子15. (1)18;31;四;失去;Ga3+;31;28 (2)B点拨:(1)x=31-2-8-3=18,原子序数=质子数,则镓元素的原子序数为31。镓原子核外有4个电子层,位于元素周期表中第四周期;镓原子的最外层电子数为3,在化学变化中易失去最外层电子,形成带3个单位正电荷的Ga3+。(2)最外层电子数相同的原子,化学性质一般相似,B项Al原子的最外层电子数为3,与Ga的化学性质相似。16. (1)D (2)五 (3)F- (4)①10 ②阴离子三、17. (1)Al;Cl;O;Na (2)
中质子数大于电子数,表示Mg2+,C正确;2个氮原子可表示为2N,D错误。11. B 点拨:α粒子轰击金箔后,大多数α粒子未发生偏转,说明金原子中有相对较大空间,即金原子核体积很小;部分α粒子发生偏转,说明受到斥力作用,可知金原子核带正电荷;有的α粒子被弹回,说明撞上了质量较大的粒子,即金原子核质量比α粒子大得多,A、C、D均正确;由该实验无法得知电子带负电,B符合题意。12. D 点拨:化学变化中,分子可以再分,原子不能再分,反应前后原子的种类和数量不变,A、B均错误;1个尿素分子中含有4个氢原子,C错误;由反应示意图可知,在一定条件下,物质间可以相互转化,D正确。二、13. (1)2H;2Al3+;2NO-3(2)2个镁离子;1个镁离子带2个单位正电荷(3)①氢、氧两种原子 ②碳、氧两种元素14. (1)氢分子;钠离子和氯离子;原子(2)①A ②Ⅰ;碳原子、氧原子15. (1)18;31;四;失去;Ga3+;31;28 (2)B点拨:(1)x=31-2-8-3=18,原子序数=质子数,则镓元素的原子序数为31。镓原子核外有4个电子层,位于元素周期表中第四周期;镓原子的最外层电子数为3,在化学变化中易失去最外层电子,形成带3个单位正电荷的Ga3+。(2)最外层电子数相同的原子,化学性质一般相似,B项Al原子的最外层电子数为3,与Ga的化学性质相似。16. (1)D (2)五 (3)F- (4)①10 ②阴离子三、17. (1)Al;Cl;O;Na (2) 
 18. (1)8;非金属 (2)得到;S2-(3)原子的最外层电子数相同 (4)a g (5)Na;F四、19. (1)进行对比,证明空气不能使酚酞试液变红(2)B试管中的酚酞试液慢慢变红色,C试管中的酚酞试液很快变红色 (3)①分子客观存在,并总在不断运动 ②温度越高,分子运动速率越快 (4)能尽量防止氨气逸出污染空气,能够说明分子运动的快慢与温度的关系等
18. (1)8;非金属 (2)得到;S2-(3)原子的最外层电子数相同 (4)a g (5)Na;F四、19. (1)进行对比,证明空气不能使酚酞试液变红(2)B试管中的酚酞试液慢慢变红色,C试管中的酚酞试液很快变红色 (3)①分子客观存在,并总在不断运动 ②温度越高,分子运动速率越快 (4)能尽量防止氨气逸出污染空气,能够说明分子运动的快慢与温度的关系等






