科学八年级上册第5节 物质的溶解优秀课后复习题
展开 
![]()
1.有M、N两种物质,20℃时20克水最多溶解5克M,60℃时100克水里最多溶解10克N。则M、N的溶解度大小是( )
A.M>N B.M<N C.M=N D.无法比较
2.现有一定温度的氯化铵饱和溶液200克,欲改变此溶液中溶质的质量分数,可采用的方法是( )
A. 温度不变,蒸发掉20克水 B. 温度不变,加入10克氯化铵固体
C. 温度不变,取出10克原溶液 D. 温度不变,加入20克水
3.无土栽培技术是植物根能直接接触培养液的栽培方法,小金在炎热的夏天从冰箱拿出一瓶硝酸钾培养液如图甲,一段时间后变成了图乙所示(不考虑水的蒸发)。溶液从甲状态到乙状态过程中,不变的科学量是( )

A.溶质质量 B.溶剂质量 C.溶液质量 D.溶质质量分数
4.在温度不变的条件下,欲使溶质的质量分数变为原来2倍,下列最可行的是( )。
A.将20克氯化钠饱和溶液蒸发掉10克水
B.将20克氯化钠不饱和溶液蒸发掉10克水
C.在10克10%的氯化钠溶液中,加人5克40%的氯化钠溶液
D.在10克氯化钠不饱和溶液中加人10克氯化钠固体
5.20C时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分到溶解,实验过程如图所示。下列分析正确的是( )
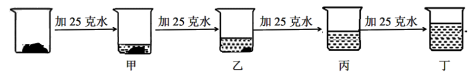
A.甲烧杯中,硝酸钾溶液是不饱和溶液
B.丁烧杯中,硝酸钾溶液是不饱和溶液
C.乙→丙过程中,硝酸钾溶液的溶质质量分数变大温地破
D.丙→丁过程中,硝酸钾溶液的溶质质量分数变大
6.20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( )。

A.所得溶液可能都是饱和溶液 B.20℃时,乙溶液的溶质质量最小
C.溶液溶质的质量分数 :甲>丙>乙 D.升高温度,溶液溶质的质量分数一定变大
7.如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,下列说法错误的是( )
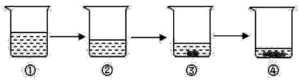
A.①溶液肯定是不饱和溶液
B.溶液中溶质质量的关系为:①=②>③>④
C.在②→④过程中,氯化钠的质量分数始终不变
D.将④烧杯中的混合物过滤后所得的滤液为饱和溶液
8.熟石灰在80℃时,饱和溶液溶质的质量分数为x,20℃时,饱和溶液溶质的质量分数为y,常压下取80℃时熟石灰饱和溶液a g,蒸发掉w g水,趁热滤去析出的固体,再恢复到20℃,滤液中溶质质量分数为z,则下列关系正确的是( )
A.y=z B.z>x>y C.y>x>z D.x=z
9.现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是( )
A.m质∶m剂=1∶10 B.m质∶m液=1∶10
C.m质∶m液=1∶11 D.m剂∶m液=10∶11
10.根据图示实验、部分记录和溶解度曲线,判断下列说法正确的是( )

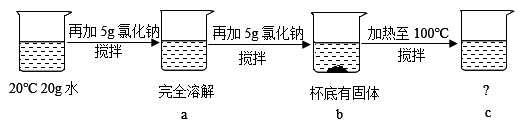
A.无法判断a中溶液是否为饱和溶液
B.c中溶液溶质的质量分数为33.3%
C.b中溶液在加热过程中始终为饱和溶液
D.用降温的的方法可获得大量氯化钠晶体
11.在20℃时,100克5%的食盐溶液温度升高到60℃(忽略水分蒸发),则溶质的质量分数为________ ;若将该溶液恒温蒸发水分,则溶液中溶质的质量分数会________(选填“增大”或“减小”) ;在20℃时,当溶液成为________时,该溶液的质量分数最大,其最大值为________。(20°C时,食盐的溶解度为36克)
12.学习《物质的溶解》时小科同学进行了如下实验:往A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入50g、25g、5g同种固体物质,充分溶解后,静置,现象如图所示。
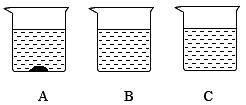
回答下列问题:
(1)小科认为,A烧杯中的溶液一定是饱和溶液。他的判断依据是___________;
(2)A、B、C三只烧杯中,溶液的溶质质量分数大小关系是___________。
13.如下图为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。
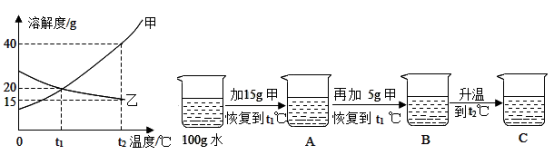
(1)t1℃时,甲的溶解度______乙的溶解度(填“大于”或“小于”或“等于”)。
(2)t2℃时,100g乙的饱和溶液中溶解______g乙溶质。(保留整数)
(3)某同学在t1℃时开始如下实验,得到相应的溶液A、B、C。
在溶液A、B、C中,属于饱和溶液的是______;在溶液C中再加入25g甲后,充分搅拌,恢复到t1℃,所得溶液的质量为______。
14.农民伯伯在挑选种子时,要挑选颗粒饱满的当作种子,通常用10%-20%的食盐溶液选种。现需配制200千克质量分数为16%的食盐溶液,问:
(1)需要食盐______千克;
(2)你认为农民伯伯该挑选______(选填“浮在液面上”或“沉入盐水中”)的用作种子;
(3)取上述配制好的质量分数为16%的食盐溶液45千克,配制成质量分数变为9%的食盐水,则需加多少千克水______?
15.如图是某同学为配制10%的食盐溶液操作示意图。请据图回答:
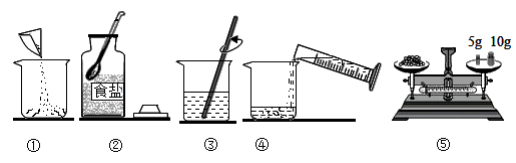
(1)配制溶液共有五个步骤,请按正确顺序补充完整:②→________④→③
(2)下列情况中,会使食盐溶液质量分数低于10%的是________。
A.称取的食盐不纯,有杂质
B.配制好的溶液转移时,不小心有少量液体溅出
16.下图是某同学配制50克质量分数为15%的蔗糖溶液的操作过程示意图。试回答下列问题。

(1)配制溶液的操作步骤有 :①溶解 ;②称量 ;③计算 ;④装瓶存放。正确的操作顺序是________(填序号)。
(2)该实验中应称取蔗糖的质量是________克。
(3)该实验中应取________毫升水,应选择________(选填“10"或“50" )毫升规格的量筒。
(4)操作步骤E中玻璃棒的作用是________。
(5)若配制的溶液溶质质量分数小于15% ,则造成误差的原因可能有________。
①称量时砝码和蔗糖放反了,并且使用了游码②取水时仰视读数
③溶解时有少量水溅出④装瓶时有溶液洒落
17.某同学在实验室观察到浓硫酸瓶上的标签如表所示。
浓硫酸(H2SO4)500毫升 | |
溶质的质量分数 | 98% |
密度 | 1.84克/厘米3 |
相对分子质量 | 98 |
强腐蚀性,阴冷,密封储藏 | |
(1)这瓶浓硫酸溶液的质量是多少克 ?该溶液中的溶质质量是多少克 ?
(2)欲配制1000克质量分数为19.6%的稀硫酸,需要这种浓硫酸多少毫升 ?需要加水多少毫升 ?
18.疫情期间学校经常要对教室进行消毒处理。现医务室购买了一桶消毒液,上面标有“20L,1.1g/cm3,20%”的字样。请计算:
(1)这一桶消毒液总质量是多少千克?其中含溶质的质量是多少千克?
(2)学校共有40间教室,每间教室需要用去2%的消毒液2kg,则需要从20%的原装消毒液中取出多少千克溶液来配制?
答案及解析
1.【答案】D
【解析】在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度,根据溶解度的定义分析。
谈到溶解度,就必须指明温度,而比较不同物质溶解度的大小时,必须控制温度相同,否则比较就没有意义,故D正确,而A、B、C错误。
2.【答案】 D
【解答】氯化铵已经达到饱和,如果温度不变,那么它的溶解度不变,即饱和溶液的溶质质量分数保持不变。
蒸发掉20g水后仍然为饱和溶液,溶质质量分数不变,故A错误;
加入10g氯化铵固体,但是不会溶解,溶质质量分数不变,故B错误;
取出10g溶液,不会改变剩余溶液的溶质质量分数,故C错误;
温度不变,加入20g水后,溶液的质量会增大而溶质质量不变,那么溶质质量分数减小,故D正确。
故选D。
3.【答案】B
【解析】溶质质量分数是表示溶液浓度的一种方法,它是溶质质量与溶液质量之比,溶质是被溶解的物质,溶剂是能溶解其他物质的物质。
乙图中原本没有溶解的硝酸钾消失了,因此溶质硝酸钾的质量增大,但是能溶解其他物质的物质(溶剂)质量没有改变,B符合题意。
4.【答案】 C
【解答】A、将20克氯化钠饱和溶液蒸发掉10克水 ,仍是该温度下的饱和溶液,溶质质量分数不变,不符合题意;
B、 将20克氯化钠不饱和溶液蒸发掉10克水,若无晶体析出,则可使溶质质量分数变为原了2倍,但若析出晶体,则不能 ,不符合题意;
C、 在10克10%的氯化钠溶液中,加人5克40%的氯化钠溶液 ,所得溶液的溶质质量分数为![]() =20%,符合题意;
=20%,符合题意;
D、在10克氯化钠不饱和溶液中加入10克氯化钠固体 ,因未确定原溶液的溶质质量分数,所以混合后的溶质质量分数不有确定,不符合题意;
故选C。
5.【答案】B
【解析】根据有固体未溶解的溶液一定是饱和溶液,向杯底有固体剩余的溶液中加水,溶质质量分数可能不变分析。
A、 甲烧杯中,硝酸钾未完全溶解,是饱和溶液 ,不符合题意;
B、丁烧杯中为丙烧杯中溶液再加25克水形成,一定是硝酸钾的不饱和溶液 ,符合题意;
C、乙→丙过程中,若固体刚好溶解,即丙是饱和溶液时,硝酸钾溶液的溶质质量分数不变,不符合题意;
D、丙→丁过程中,硝酸钾溶液的溶质质量分数变小,不符合题意;
6.【答案】 A
【解答】A、甲和丙有固体剩余,一定是饱和溶液,乙全部溶解,可能饱和可能不饱和,符合题意;
B、 20℃时,乙溶液中溶质质量最多,溶质质量最大 ,不符合题意;
C、由图示可知,等质量三种固体乙溶解最多,其次是丙,甲溶解的最少,则溶液溶质的质量分数 甲<丙<乙 ,不符合题意;
D、因不确定三种物质溶解度随温度的变化规律,所以升高温度,溶液溶质的质量分数不一定变大 ,不符合题意;
故选A。
7.【答案】C
【解析】(1)②为饱和溶液,将①和②的溶剂质量比较大小即可;
(2)析出的晶体越多,溶质的质量越少;
(3)饱和溶液的溶质质量分数与溶解度有关;
(4)如果溶液中有晶体出现,那么它肯定是饱和溶液。
【解答】A.①蒸发溶剂得到②,即①中溶剂的质量肯定大于②的溶剂质量。因为②为饱和溶液,那么①肯定为不饱和溶液,故A正确不合题意;
B.①和②中都没有溶质析出,那么它们的溶质质量相等,即①=②;③中析出氯化钠的质量小于④,那么③中溶质的质量大于④,因此溶质质量大小关系:①=②>③>④,故B正确不合题意;
C.②③④都是饱和溶液,②和③的温度相同,那么氯化钠的溶解度相同,则溶质质量分数相同;④的温度高,氯化钠的溶解度改变,则溶质质量分数改变,故C错误符合题意;
D.④中有氯化钠晶体析出,肯定为饱和溶液,故D正确不合题意。
8.【答案】 D
【解答】熟石灰在80℃时,饱和溶液溶质的质量分数为x,20℃时,饱和溶液溶质的质量分数为y,
因素氢氧化钙的溶解度随温度升高而减小,所以饱和溶液的溶质质量分数x<y。
常压下取80℃时熟石灰饱和溶液a g,蒸发掉w g水,趁热滤去析出的固体此时还是该温度下的饱和溶液,也就是此时溶质的质量分数为x。再恢复到20℃,此时有高温度下的饱和溶液变成了低温的不饱和溶液,但是溶质和溶剂没有变化,所以溶质的质量分数保持不变,所以x=z。
综上所述,z=x<y。
故选D。
9.【答案】B
【分析】根据溶液中的组成判断可知,食盐水的溶质是食盐,溶剂是水;由题意可知,该食盐水中溶质的质量分数为10%,也就是,溶质质量与溶液质量之比是:10:100(即1:10)。
【详解】A、由分析可知,m质∶m剂=1∶9,故错误;
B、由分析可知,m质∶m液=1∶10,故正确;
C、由分析可知,m质∶m液=1∶10,故错误;
D、由分析可知,m剂∶m液=9∶10,故错误。
故选B。
10.【答案】C
【详解】A、由图可知,20℃时氯化钠的溶解度约为36g,则此时20g水中最多溶解7.2g氯化钠,20℃将5g氯化钠放入20g水中,氯化钠固体会完全溶解形成不饱和溶液,选项错误;
B、100℃时,氯化钠的溶解度为40g,20g水中最多溶解氯化钠8g,则题目中加入的10g氯化钠只能溶解8g,所得溶液的溶质质量分数=![]() ×100%≈28.6%,选项错误;
×100%≈28.6%,选项错误;
C、b溶液的底部有固体剩余,溶液为饱和溶液,升温至100℃时,c溶液中只能溶解8g氯化钠,溶液为饱和溶液,即b中溶液在加热过程中始终为饱和溶液,选项正确;
D、氯化钠的溶解度随温度升高而增大,氮氯化钠的溶解度收温度影响较小,用降温的的方法不能获得大量氯化钠晶体,应选择蒸发结晶的方法来获得氯化钠晶体,选项错误;
故选C。
11【答案】5%;增大;饱和溶液;26.47%
【解析】根据溶质量分数=溶质质量/溶液质量、改变温度饱和溶液变不饱和溶液时溶质质量分数不变,蒸发溶剂时溶质质量分数增大,一定温度下饱和溶液溶质质量分数达到最大值且等于溶解度/100+溶解度分析。
【解答】 在20℃时,100克5%的食盐溶液温度升高到60℃,变成不饱和溶液,溶质质量分数不变,仍为5%;若将该溶液恒温蒸发水分,则溶液中溶质的质量分数会因溶剂质量减小而增大 ;在20℃时, 当溶液成为饱和溶液时溶质质量分数最大,20℃食盐的溶解度为36克 ,则饱和溶液溶质质量分数为![]() =26.47%。
=26.47%。
12.【答案】 A中有剩余固体(或A中有不溶解的固体等)(合理即可) A≥B>C(或C<B≤A)
【解析】(1)A烧杯中有固体剩余,不能继续溶解,一定是该物质的饱和溶液。所以他的判断依据是A中有不溶解的固体。
(2)A、B、C三只烧杯中分别装入等质量的水,A为该温度下的饱和溶液,BC均无固体剩余,B中加入固体的质量比C多,则B可能是饱和溶液,也可能是不饱和溶液,C为不饱和溶液,则溶液的溶质质量分数大小关系是A≥B>C。
13.【答案】 等于 13 B 120g
【详解】(1)由图可知,t1℃时,甲、乙的溶解度曲线相交,表明t1℃时,甲的溶解度等于乙的溶解度,故填等于。
(2)由图可知,t2℃时乙的溶解度为15g,则t2℃时,100g乙的饱和溶液中溶解溶质乙的质量=100g×![]() ×100%≈13g,故填13。
×100%≈13g,故填13。
(3)由图可知,t1℃时甲的溶解度为20g,A烧杯中的溶液是t1℃时100g水中溶解15g甲,形成甲的不饱和溶液,选项错误;
B烧杯中的溶液是t1℃时100g水中溶解20g甲形成的溶液,恰好是甲的饱和溶液,选项正确;
由图可知,t2℃时甲的溶解度为40g,C烧杯中的溶液是t2℃时100g水中溶解20g甲形成的溶液,是甲的不饱和溶液,选项错误,故填B;
由图可知,t1℃时甲的溶解度为20g,在溶液C中再加入25g甲后,烧杯中甲的质量=20g+25g=45g,恢复到t1℃,溶液中只能溶解20g甲,所得溶液的质量=100g+20g=120g,故填120。
14.【答案】 32 沉入盐水中 35kg
【详解】(1)需要食盐的质量为:200kg×16%=32kg;
(2)漂浮在水面上的种子,密度小于盐水;在水里下沉的种子,密度大于盐水,种子的密度越大,说明种子籽粒越饱满,因此农民伯伯应该挑选沉入盐水中的种子。
(3)解: 设用16%的食盐溶液45千克,配制成质量分数变为9%的食盐水,需加加水的质量为x,根据溶液稀释前后溶质的质量相等,有16%×45kg=9%×(45kg+x),x=35kg。
15.【答案】(1)⑤→① (2)A
【解析】(1)根据配制一定浓度的溶液的实验过程分析;
(2)根据溶质质量分数=![]() 可知,溶质质量偏小,要么是溶质质量偏小,要么是溶剂质量偏大,据此分析判断。
可知,溶质质量偏小,要么是溶质质量偏小,要么是溶剂质量偏大,据此分析判断。
【解答】(1)配制10%的氯化钠溶液的步骤为:②取出食盐;⑤称量食盐;①将食盐倒入烧杯;④量筒量取水倒入烧杯;③用玻璃棒搅拌,直到完全溶解。
则正确的顺序为:②→⑤→①→④→③。
(2)A.称取的食盐不纯,有杂质,那么溶质的质量偏小,故A符合题意;
B.配制好的溶液转移时,不小心有少量液体溅出。由于溶液均一稳定,因此不会影响溶液的溶质质量分数,故B不合题意。
16.【答案】(1)③②①④
(2)7.5
(3)42.5;50
(4)搅拌,加速蔗精溶解
(5)①②
【解析】(1)根据配制溶液的操作步骤分析;
(2)根据溶质质量=溶液质量×溶质质量分数分析;
(3)根据溶液质量=溶质质量+溶剂质量分析;
(4)根据溶解时玻璃棒的搅拌作用分析;
(5)根据溶质质量分数偏小可能是溶质偏小或溶剂偏多分析。
【解答】(1)配制溶液的操作步骤为计算、称量、溶解、装瓶,即顺序为③②①④;
(2)该实验中应称取蔗糖的质量是50克×15%=7.5g;
(3)该实验中应取用水的质量为50g-7.5g=42.5g,体积为42.5毫升,应选择50毫升规格的量筒;
(4)E为溶解,玻璃棒的作用是搅拌,加速蔗精溶解 ;
(5)①称量时砝码和蔗糖放反了,并且使用了游码,会使溶质质量偏小,使溶质质量分数偏小,正确;②取水时仰视读数,会使水的实际体积偏大,溶质质量分数偏小,正确;③溶解时有少量水溅出,会使溶质质量分数因溶剂偏小而偏大,错误;④装瓶时有溶液洒落不影响溶质质量分数大小,错误;
17.【答案】(1)这瓶浓硫酸溶液的质量为500毫升× 1.84克/厘米3 =920克,
该溶液中的溶质质量是920克 ×98%=901.6克;
(2)设需浓硫酸质量为x
1000克×19.6% =98%x
x=2000克,
则体积为200克÷ 1.84克/厘米3 =108.7毫升,
需水的质量为1000克-200克=800克,体积为800毫升。
【解析】(1)根据溶质质量=溶液质量×溶质质量分数,溶液质量=溶液体积×密度分析;
(2)根据溶液稀释前后溶质质量不变及所加水的质量即为稀溶液质量-浓溶液质量分析。
18.【答案】(1)解:20L=20000cm3
消毒液的总质量=20000cm3×1.1g/cm3=22000g=22kg
溶质的质量=22kg×20%=4.4kg
答:消毒液总质量为22kg,其中含溶质的质量为4.4kg。
(2)解:需要2%的消毒液的质量=40×2kg=80kg
设需要20%的消毒液的质量为x
80kg×2%=x×20%
x=8kg
答:需要20%的消毒液的质量为8kg。
初中科学第4节 变阻器优秀课堂检测: 这是一份初中科学第4节 变阻器优秀课堂检测,共10页。试卷主要包含了用滑动变阻器改变小灯泡的亮度等内容,欢迎下载使用。
浙教版八年级上册第2章 天气与气候第2节 气温优秀当堂达标检测题: 这是一份浙教版八年级上册第2章 天气与气候第2节 气温优秀当堂达标检测题,共6页。试卷主要包含了在以下词语中,下列说法指天气的是,下图中,昼夜温差最小的是等内容,欢迎下载使用。
初中科学浙教版八年级上册第5节 物质的溶解精品随堂练习题: 这是一份初中科学浙教版八年级上册第5节 物质的溶解精品随堂练习题,共8页。试卷主要包含了如图为A、B、C三种固体物质等内容,欢迎下载使用。