



- 2024岳阳县一中高三开学考试政治试题含答案 试卷 0 次下载
- 2024岳阳县一中高三开学考试地理试题含答案 试卷 0 次下载
- 2024岳阳县一中高三开学考试历史试题含答案 试卷 0 次下载
- 2024岳阳县一中高三开学考试生物试题含答案 试卷 0 次下载
- 2024岳阳县一中高三开学考试物理试题含答案 试卷 1 次下载
2024岳阳县一中高三开学考试化学试题含答案
展开![]() 2021级高三上学期入学考试
2021级高三上学期入学考试
化学试卷
满分100分 时量75分钟
可能用到的相对原子质量:N14 O 16 ![]() 64
64
一.选择题(共14小题,每小题3分,共42分)
★1.化学为创造美好生活贡献力量。下列对我国科技成就的有关解读错误的是( )
选项 | 科技动态 | 化学解读 |
A | 成功制备 高性能新型纤维 聚合物锂离子电池 | 该电池将化学能全部转化成电能 |
B | 诞生迄今最轻镁同位素(18Mg) | 该核素含6个中子和12个质子 |
C | 首次实现以CO2和H2为原料人工合成淀粉 | 淀粉是粮食的主要 成分,属于糖类 |
D | 发现PM2.5污染治理中NH3减排比NOx更有效 | 回收NH3可以制造氮肥、硝酸等 |
★2.下列实验操作规范且能达到实验目的的是( )
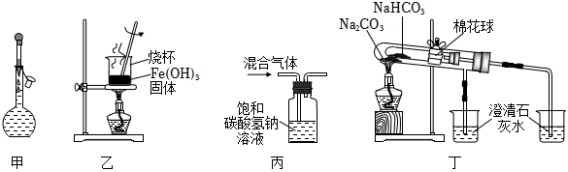
A.通过图甲所示操作配制1mol/L的氯化钠溶液
B.用装置乙灼烧Fe(OH)3固体制Fe2O3
C.用丙装置除去Cl2中含有的少量HCl
D.利用装置丁比较碳酸钠与碳酸氢钠的热稳定性
★3.对于下列性质的比较正确的是( )
A.离子半径:r(Cl﹣)>r(S2﹣)>r(Na+)
B.元素的电负性:Si<P<N
C.稳定性:H2O>H2S>HCl
D.晶格能:MgO>NaBr>NaCl
★4.下列物质:①甲烷②乙烯③乙炔④苯⑤甲苯,既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色的是( )
A.①② B.②③ C.②③⑤ D.②③④
★5.下列符号表征错误的是( )
A.![]() 的水解方程式为:
的水解方程式为:![]() H2O⇌H3O+
H2O⇌H3O+![]()
B.H2分子中σ键的电子云轮廓图:![]()
C.H2S的VSEPR模型: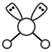
D.MgCl2的形成过程:![]()
★6.咖啡酸片常用于手术时止血,其活性成分咖啡酸的结构简式如图所示,下列说法正确的是( )
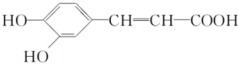
A.一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为3:1
B.1mol该物质与足量饱和NaHCO3溶液反应,可放出22.4LCO2(标准状况)
C.1mol该物质与足量浓溴水反应,消耗3molBr2
D.含有2个酚羟基、1个碳碳双键和1个羧基的咖啡酸的同分异构体有11种
7.宏观辨识与微观探析是化学学科核心素养之一,下列离子方程式能完全表示相应事实的是( )
A.向![]() 溶液中滴加过量的氨水:
溶液中滴加过量的氨水: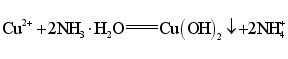
B.用过量的热烧碱溶液检验![]() 中的
中的![]() :
: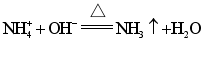
C.在强碱溶液中次氯酸钠与![]() 反应生成
反应生成![]() :
: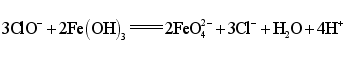
D.用![]() 溶液检验亚铁离子:
溶液检验亚铁离子: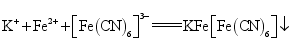
8.设![]() 为阿伏加德罗常数的值,下列说法错误的是( )
为阿伏加德罗常数的值,下列说法错误的是( )
A.由![]() 与
与![]() 组成的4.6g混合气体中含有的氮原子数为
组成的4.6g混合气体中含有的氮原子数为![]()
B.标准状况下,11.2L![]() 中含有的分子数为
中含有的分子数为![]()
C.3.2g![]() 完全溶于一定量的浓硝酸中,转移的电子数一定为
完全溶于一定量的浓硝酸中,转移的电子数一定为![]()
D.25℃时,1L![]() 为12的
为12的![]() 溶液中含有
溶液中含有![]() 的数目为
的数目为![]()
★9.硼酸(H3BO3)为一元弱酸,已知H3BO3与足量NaOH溶液反应的离子方程式为:H3BO3+OH﹣=B(OH)4﹣,H3BO3可以通过电解的方法制备。其工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。下列说法正确的是( )
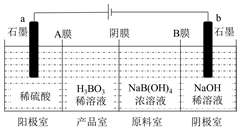
A.电子流向:电源负极→b电极→电解液→a 电极→电源正极
B.阳极的电极反应式为:2H2O﹣4e﹣═O2↑+4H+
C.当电路中通过3mol电子时,可得到1mol H3BO3
D.A膜为阳膜,B膜为阴膜,且穿过A膜和B膜的离子数相同
★10.实验室分离Fe3+和Al3+的流程如图:
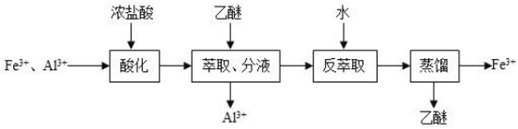
已知:Fe3+在浓盐酸中生成亮黄色配离子[FeCl4]﹣,该配离子在乙醚(Et2O,沸点34.6℃)中生成配合物Et2O•H+•[FeCl4]﹣。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管,冷却水从冷凝管下口通入
★11.室温下,取10mL0.1mol⋅L﹣1某二元酸H2A,滴加0.1mol⋅L﹣1NaOH溶液。已知:H2A═H++HA﹣,HA﹣⇌H++A2﹣,下列说法不正确的是( )
A.0.1mol⋅L﹣1H2A溶液中有c(H+)﹣c(OH﹣)﹣c(A2﹣)=0.1mol⋅L﹣1
B.当滴加至中性时,溶液中c(Na+)=c(HA﹣)+2c(A2﹣),用去NaOH溶液的体积小于10mL
C.当用去NaOH溶液体积10mL时,溶液的pH<7,此时溶液中有c(A2﹣)=c(H+)﹣c(OH﹣)
D.当用去NaOH溶液体积20mL时,此时溶液中有c(Na+)=2c(HA﹣)+2c(A2﹣)
★12.金属Ni可活化C2H6放出CH4,其反应历程如图所示:
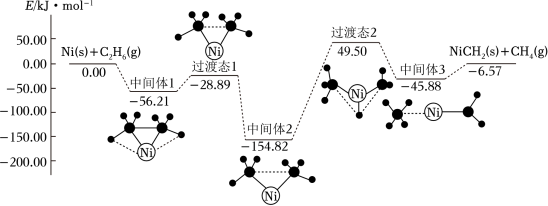
下列关于活化历程的说法错误的是( )
A.中间体1→中间体2的过程是放热过程
B.加入催化剂可降低该反应的反应热,加快反应速率
C.Ni和C2H6的总键能小于NiCH2和CH4的总键能
D.中间体2→中间体3的过程是决定整个历程反应速率的关键步骤
13.下列实验探究方案不能达到探究目的的是( )
选项 | 探究方案 | 探究目的 |
A | 将二氧化硫气体通入碘和淀粉的混合溶液中,观察溶液颜色的变化 | 探究还原性: |
B | 向盛有 | 探究 |
C | 加热溴乙烷和氢氧化钠-乙醇混合溶液,将产生的气体通入高锰酸钾溶液中,观察溶液颜色的变化 | 探究溴乙烷在此条件下发生的是取代反应还是消去反应 |
D | 向盛有等浓度的 | 证明 |
 14.25℃时,向25mL
14.25℃时,向25mL![]()
![]() 溶液中加入
溶液中加入![]() 固体或通入
固体或通入![]() 气体,混合溶液中
气体,混合溶液中![]() [
[![]() 或
或![]() ]与
]与![]() 的关系如图所示(忽略溶液体积变化和
的关系如图所示(忽略溶液体积变化和![]() 可能逸出)。下列有关叙述正确的是( )
可能逸出)。下列有关叙述正确的是( )
A.c点![]()
B.![]() 的
的![]() 约为
约为![]()
C.b点有关微粒浓度的大小关系为![]()
D.从b点到e点,水电离产生的![]() 先减小后增大
先减小后增大
二.非选择题(每空2分,共58分)
15.亚硝酰硫酸[M(NOSO4H)=127g•mol﹣1]主要用于分散染料重氮反应中取代亚硝酸钠,从而降低成本,提高产品质量。实验室用如图1装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。
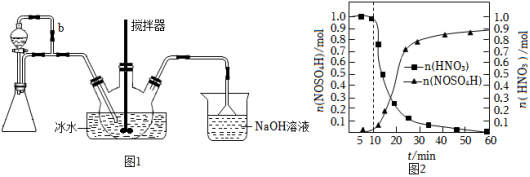
(1)装置A制取SO2,则A中反应的化学方程式为 ,导管b的作用是 _
(2)SO2与装置B中盛有的浓硫酸和浓硝酸的混合液在维持体系温度不得高于20℃的条件下,反应制得NOSO4H。反应过程中,亚硝酰硫酸和硝酸的物质的量随时间的变化如图2所示。
①装置B中发生反应的化学反应方程式为 。
②反应进行到10min后,反应速度明显加快,其可能的原因是 。
(3)装置C的主要作用是 。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是 。
(5)测定亚硝酰硫酸NOSO4H的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入0.1000mol•L﹣1、60.00mL的KMnO4标准溶液和10.00mL 25% H2SO4溶液,然后摇匀。用0.2500mol•L﹣1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:
2KMnO4+5NOSO4H+2H2O═K2SO4+2MnSO4+5HNO3+2H2SO4
2MnO4﹣+5C2O42﹣+16H+═2Mn2++10CO2↑+8H2O
达到滴定终点时的现象为 ,亚硝酰硫酸的纯度为 。(精确到0.1%)若其他操作及读数均正确,滴定到终点后,下列操作会导致所测定样品中NOSO4H的纯度偏大的是 。(填字母)
A.滴加草酸钠标准溶液时,滴加前仰视读数,滴加后俯视读数
B.滴加草酸钠标准溶液时,开始时尖嘴处无气泡,结束时出现气泡
C.滴定过程中,将挂在锥形瓶壁上的草酸钠标准溶液滴用蒸馏水冲进瓶内
16.铅铬黄是一种颜料,主要成分是铬酸铅![]() (摩尔质量323g/mol)。现以
(摩尔质量323g/mol)。现以![]() 和
和![]() 等为原料制备该物质,并测定产物纯度。
等为原料制备该物质,并测定产物纯度。
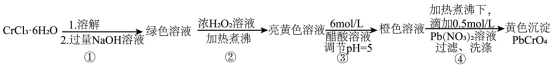
回答下列问题:
(1)已知![]() 不溶于水,具有两性。第①步所得绿色溶液中的有色离子是_______。
不溶于水,具有两性。第①步所得绿色溶液中的有色离子是_______。
(2)第②步生成了![]() ,写出该步骤的离子方程式_______。为了使
,写出该步骤的离子方程式_______。为了使![]() 反应充分而不剩余,以下方案中最合理的是_______(填序号)。
反应充分而不剩余,以下方案中最合理的是_______(填序号)。
A.首先加热绿色溶液,然后将一定量![]() 浓溶液滴入其中
浓溶液滴入其中
B.首先加热![]() 浓溶液,然后转入热的绿色溶液中
浓溶液,然后转入热的绿色溶液中
C.首先将一定量![]() 浓溶液滴入绿色溶液中,然后加热煮沸
浓溶液滴入绿色溶液中,然后加热煮沸
(3)第③步调节pH=5的目的是为了将![]() 转化为_______(填写离子符号),并且防止在碱性条件下_______形成沉淀。
转化为_______(填写离子符号),并且防止在碱性条件下_______形成沉淀。
(4)由于铬酸铅的溶解度比重铬酸铅的小的多,在第④步中逐滴滴加![]() 溶液后,产生
溶液后,产生![]() 黄色沉淀,此时为了提高铅铬黄的产率,可补加少最NaOH溶液,请用化学平衡移动原理加以解释:_______。
黄色沉淀,此时为了提高铅铬黄的产率,可补加少最NaOH溶液,请用化学平衡移动原理加以解释:_______。
17.铜阳极泥分银渣含有铅、锡、钡以及金、银等有价值的金属元素,具有较高的综合利用价值,其中锡主要以![]() 形式存在,铅、钡主要以硫酸盐的形式存在。分银渣分离的工艺流程如图,请回答下列问题:
形式存在,铅、钡主要以硫酸盐的形式存在。分银渣分离的工艺流程如图,请回答下列问题:

已知:
①常温下,部分碳酸盐、硫酸盐的溶度积常数如下表:
盐 |
|
|
|
|
|
|
|
|
|
②![]() 不溶于水,也难溶于酸和碱。
不溶于水,也难溶于酸和碱。
(1)已知Sn与C同主族,则基态Sn原子的价层电子轨道表示式为。
(2)请根据提供的数据判断分银渣分离的工艺流程中,②应该填入的元素名称分别为;Y溶液的溶质分别为。
(3)工艺流程中钡碳酸转化的原理为(用离子方程式表示),使![]() 转化成
转化成![]() ,需要使
,需要使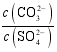 最少等于。
最少等于。
(4)加入HCl、![]() 溶液可使Au、Ag转化成
溶液可使Au、Ag转化成![]() 、
、![]() ,写出Au转化成
,写出Au转化成![]() 的离子方程式:。
的离子方程式:。
(5)由金的X射线衍射图像可知,其晶胞属于面心立方晶胞(如图)。若金原子的半径为rcm,金的密度为![]() ,金原子的摩尔质量为
,金原子的摩尔质量为![]() ,则阿伏加德罗常数(
,则阿伏加德罗常数(![]() )的计算表达式
)的计算表达式![]() __________(用含r、
__________(用含r、![]() 、M的代数式表示)。
、M的代数式表示)。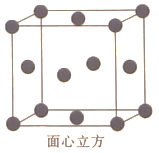
18.酮基布洛芬片是用于治疗各种关节炎、强直性脊柱炎引起的关节肿痛以及痛经、牙痛、术后痛和癌性痛等的非处方药。其合成路线如图所示:
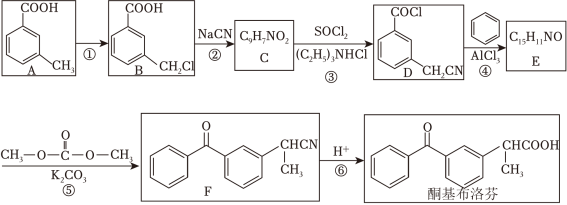
(1)A的化学名称为 。
(2)B中官能团的名称为 ,B→C的反应类型为 。
(3)写出E的结构简式: 。
(4)![]() 中C原子的杂化方式有 。
中C原子的杂化方式有 。
(5)H为C的同分异构体,则符合下列条件的H有 种。
①除苯环外不含其他环状结构
②含有硝基,且直接连在苯环上
③分子中无甲基
(6)以乙烷和碳酸二甲酯(![]() )为原料(无机试剂任选),设计制备异丁酸的一种合成路线 。
)为原料(无机试剂任选),设计制备异丁酸的一种合成路线 。
2024安徽六校高三开学考试化学试题: 这是一份2024安徽六校高三开学考试化学试题,共8页。
2023-2024学年江苏镇江高三开学考试 化学试题(含答案): 这是一份2023-2024学年江苏镇江高三开学考试 化学试题(含答案),共11页。
2024扬州中学高三上学期开学考试化学试题含答案: 这是一份2024扬州中学高三上学期开学考试化学试题含答案,共10页。试卷主要包含了 单项选择题, 非选择题等内容,欢迎下载使用。












