






人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量示范课课件ppt
展开1.理解物质的量及其单位2.理解摩尔质量的概念3.掌握物质的量与微粒数目、摩尔质量之间的换算
1.通过学生理解物质的量、摩尔质量的概念的理解,培养学生宏观辨识与微观探析的化学核心素养。2.通过设置有效练习使学生理解物质的量、摩尔质量的应用,培养学习论据推理与模型认知的化学核心素养。3.通过摩尔质量的计算对学生进行规范化解题格式的训练,强化学生的论据推理与模型认知的化学核心素养。
钻石早在4000多年前就被人类发现,事实上它已在地表蕴藏亿万年。由于它所散发出来的光泽永恒灿烂,在远古法老时代,钻石是贵族独有的珍宝,逐渐被用来象征爱情的坚贞不渝。关于它的传说也美丽得令人心动,希腊人说钻石是星星坠落地面的碎片,也传说它是天神的眼泪。不论是怎样的传说,现在钻石对于我们来说都是一种美丽的代表。你知道钻石的重量单位是什么吗?
克拉是宝石的重量单位,1克拉等于0.2 g。在相当长的一个历史时期,各国所用的“克拉”表示的重量略有不同:巴黎 — 0.205 g,伦敦 — 0.20530 g,佛罗伦萨 — 0.197 20 g,马德里— 0.205 39 g,柏林 — 0.20544 g,阿姆斯特丹 — 0.20570 g,里斯本 — 0.20539 g,法兰克福— 0.20577 g,维也纳 — 0.20613 g,威尼斯 — 0.20770 g,印度 — 0.20735 g。
1907年巴黎召开的国际计量委员会第四次大会上,正式通过将标准克拉定为0.200 g。
拿什么来衡量宝石的重量呢?许多民族的祖先不谋而合,都想到用当地常见的植物种子。欧洲许多国家最初是用它们盛产的大麦来作砝码。但是各地区出产的大麦大小不同,重量差异大,用它称宝石,常常发生争端,最后找到一种种子----金合欢树的种子来作统一标准,因希腊人叫这种种子为“克拉”,就把它作为宝石的重量单位。
你一口气能喝多少克水?
你知不知道一口气喝下了多少个水分子?
一滴水中所含的水分子数,让全世界65亿人去数,每人每分钟数100个,日夜不停的数,需要5千年才能数完。
想办法在水分子数和水的质量之间找到一个桥梁——集体单位。。
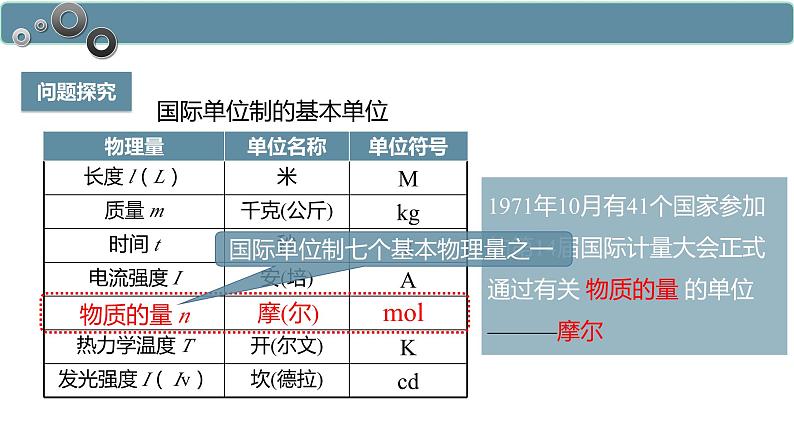
1971年10月有41个国家参加的第14届国际计量大会正式通过有关 物质的量 的单位———摩尔
单位名称:_______ 符号:_____
2. 定义:表示含有一定数目粒子的集合体
1打铅笔:1双袜子:1世纪:
1ml某种微粒是多少个呢?(如:1ml水分子有多少个水分子呢?)
3. 使用:(1)使用“摩尔”作单位时,所指粒子必须十分明确,且仅限于微观粒子。(2)要用化学式指明微粒种类或其组合。
纠错:2mlH,1mlH2,1.5mlNaOH,3mlOH-,1.5mlCa(OH)2,0.5mle-
3. 用摩尔为单位表示某物质的物质的量时,必须指明物质微粒的名称、符号或化学式。如:1 ml H、1 ml H+、 1 ml H2 ,不能用 “1 ml 氢”这样表示。
1. “物质的量”是一个物理量的全称,是一个专有名词,不能当成物质的数量或质量来理解。
2. 摩尔只能描述原子、分子、离子、质子、中子和电子等微观粒子,不能描述宏观物质。
4. 物质的量的数值可以是整数,也可以是小数。
意大利物理学家、化学家。1776年8月9日生于都灵的一个贵族家庭。1792年8月9日入都灵大学学习法学,1796年获法学博士,以后从事律师工作。1800~1805年又专门攻读数学和物理学,尔后主要从事物理学、化学研究。1811年,提出分子学说:分子由原子组成,并推出同体积气体在同温同压下含有同数目的分子,又称阿伏加德罗定律。阿伏加德罗对6.02 × 1023这个数据的得出有着重大贡献,故用其名字表示该常数以示纪念,即将6.02 × 1023 ml-1叫做阿伏加德罗常数,用NA表示。
1. 定义:1ml任何粒子的粒子数叫做阿伏加德罗常数。
NA 6.02×1023 ml-1
联系: π = 3.14 ???
1ml任何粒子的粒子数
(NA)单位:ml-1
3. n、N、NA 关系:
1ml物质的质量是多少?
1ml任何微粒的质量以克为单位时,在数值上等于该微粒的相对原子质量或相对分子质量
2. 符号:
1ml O2的质量是( )O2的摩尔质量是( )O2的相对分子质量是( )
单位物质的量的物质所具有的质量
g· ml-1 或 kg· ml-1
【解】Na2CO3的相对分子质量106,摩尔质量为106g·ml-1。
答:26.5g Na2CO3的物质的量是0.25ml。
26.5g Na2CO3的物质的量是多少?
× 6.02×1023
÷ 6.02×1023
1. 下列说法中正确的是( )A.摩尔是国际单位制中的七个物理量之一B.0.5 ml H2O中含有的原子数目为1.5NA C.64 g氧相当于2 ml氧D.1 ml任何物质都约含有6.02×1023个原子
2. 设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )A. 1 ml OH-所含电子数为10NAB. 2 L 0.5 ml·L-1Na2SO4溶液中阴离子所带电荷数为0.2NAC. 0.05mlH2O含有的氢原子数为0.05NAD. 14 g由CO和N2组成的混合气体中含有的分子总数为NA
3. NA代表阿伏加德罗常数,下列说法中正确的是( )A. 0.1 ml钠原子变成钠离子时,失去的电子数为0.2NAB. 0.2NA个硫酸分子与0.2 ml磷酸含有相同的氧原子数C. 1 ml 氧气和臭氧的混合气体中含有的氧原子数目为2.5NAD.NA个氧分子与NA个氖分子所含原子的物质的量之比为1∶1
高中人教版 (2019)第二章 海水中的重要元素——钠和氯第三节 物质的量完美版ppt课件: 这是一份高中人教版 (2019)<a href="/hx/tb_c161983_t3/?tag_id=26" target="_blank">第二章 海水中的重要元素——钠和氯第三节 物质的量完美版ppt课件</a>,共28页。PPT课件主要包含了考纲要求,一粒大米,水是由水分子构成,一物质的量,mol氢原子,mol氢气分子,mol氢离子,阿伏伽德罗常数,012kg,02×1023等内容,欢迎下载使用。
高中人教版 (2019)第三节 物质的量教学ppt课件: 这是一份高中人教版 (2019)第三节 物质的量教学ppt课件,共30页。PPT课件主要包含了素养要求,任务1,物质的量,任务2,摩尔质量,限时训练,任务3等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第三节 物质的量教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第三节 物质的量教学课件ppt,共20页。PPT课件主要包含了学习目标等内容,欢迎下载使用。













