

所属成套资源:2024届高三新高考化学大一轮专题练习 (76份)
2024届高三新高考化学大一轮专题练习—水溶液中的离子反应与平衡(有答案)
展开
这是一份2024届高三新高考化学大一轮专题练习—水溶液中的离子反应与平衡(有答案),共25页。试卷主要包含了单选题,原理综合题,工业流程题等内容,欢迎下载使用。
2024届高三新高考化学大一轮专题练习—水溶液中的离子反应与平衡
一、单选题
1.(山东省聊城市齐鲁名校大联盟2023届高三第三次联考化学试题)高纯三氯氧磷是集成电路、太阳能电池生产的掺杂剂。实验室可通过以下实验步骤测定三氯氧磷产品中氯元素的含量,并计算产品的纯度[已知:常温下,,,呈白色]。
①取产品置于盛蒸馏水的水解瓶中,摇动至完全水解,将水解液配成溶液并预处理排除含磷粒子的影响。
②取溶液于锥形瓶中,向其中加入的标准溶液,使完全沉淀,再加入硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴溶液作指示剂,用标准溶液滴定过量至终点,所用体积为。
假设杂质不参加反应,则下列说法正确的是
A.配制好的标准溶液可盛放在棕色广口试剂瓶中
B.实验过程中可用甲苯代替硝基苯进行实验
C.滴定终点时锥形瓶中有血红色沉淀生成
D.实验过程中若忘记加入硝基苯,会导致所测的含量偏低
2.(2023春·北京东城·高三汇文中学校考期中)下列方程式与所给事实不相符的是
A.向ZnS浊液中滴加溶液,白色浑浊变为黑色:
B.用白醋去除水垢的离子方程式:
C.向溶液中滴加少量浓,溶液橙色加深:
D.氯化铵的水溶液显酸性:
3.(2023春·广东茂名·高三茂名市第一中学校考阶段练习)常温下,往5mL蒸馏水中加入一定量的Mg(OH)2固体后,再加入Fe3+与Mg2+等物质的量的FeCl3的溶液,测得-lgc~进程曲线如图所示,下列说法不正确的是
A.加入Mg(OH)2固体存在沉淀溶解平衡Mg(OH)2(s)Mg2+(aq)+2OH-(aq),使得c(H+)减少
B.加入FeCl3溶液后,c(Mg2+)增大,存在沉淀的转化
C.加入FeCl3溶液后,存在Fe3+水解,c(H+)增大
D.若增加FeCl3溶液的用量,最终pH会大于5
4.(2023·辽宁朝阳·朝阳市第一高级中学校联考二模)下列装置或操作能达到相应实验目的的是
A.甲装置用于酸性溶液滴定溶液
B.乙装置用于判断,且可转化成
C.丙装置可用于吸收氨气,且能防止倒吸
D.丁装置可用于除去氯气中的HCl
5.(2023·辽宁朝阳·朝阳市第一高级中学校联考二模)室温下,向的溶液中滴加的NaOH溶液时,pH、(、或)随V(NaOH溶液)变化的曲线如图。下列叙述不正确的是
A.常温下,的第一步电离平衡常数
B.当V(NaOH溶液)=10mL时,
C.V(NaOH溶液)=20mL时,水的电离程度最大
D.常温下,当时,有
6.(2022秋·陕西西安·高三长安一中校考期末)已知常温下,浓度均为的4种钠盐溶液的如下表,下列说法中正确的是
溶质
11.6
10.3
8.3
5.2
A.将足量通入溶液,发生反应的离子方程式为
B.向氯水中加入固体,可以增大氯水中次氯酸的浓度
C.常温下,、、三种溶液,pH最小的是溶液
D.溶液中离子浓度大小顺序为
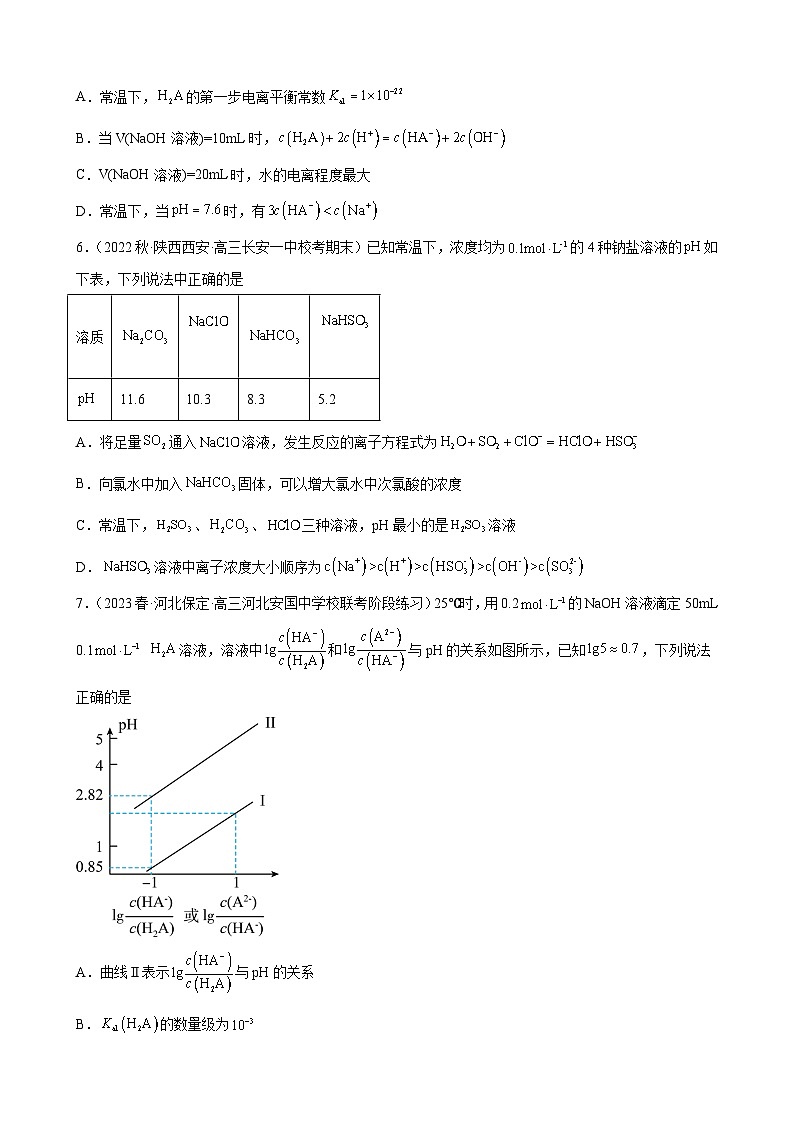
7.(2023春·河北保定·高三河北安国中学校联考阶段练习)25℃时,用0.2的NaOH溶液滴定50mL 0.1 溶液,溶液中和与pH的关系如图所示,已知,下列说法正确的是
A.曲线Ⅱ表示与pH的关系
B.的数量级为
C.滴入25mL NaOH溶液时,溶液呈碱性,存在关系
D.滴入50mL NaOH溶液时,溶液的pH约为8.26
8.(2023春·河北保定·高三河北安国中学校联考阶段练习)下列由实验操作、现象得到的结论错误的是
选项
实验操作
现象
结论
A
向5mL 0.1 溶液中先加入2mL 0.4 NaOH溶液,再加入1mL 0.1 溶液
溶液中先出现蓝色沉淀,后出现黑色沉淀
B
向某溶液中滴入少量氯化钡溶液
产生白色沉淀
溶液中可能含有
C
将盛有气体的密闭容器压缩体积
气体颜色先变深后变浅
平衡向消耗气体的方向移动
D
将适量氯水滴入石蕊溶液中
石蕊溶液先变红后褪色
氯水具有酸性和漂白性
A.A B.B C.C D.D
9.(2023春·江苏南通·高三海安高级中学校考阶段练习)某研究小组为探究沉淀能否由一个溶度积较小的物质转化为溶度积较大的物质,设计了如图所示实验流程。
已知:该温度下,,,的溶解度为。忽略体积变化,下列说法正确的是
A.经过步骤①,溶液中
B.经过步骤②,溶液中
C.经过步骤②,约有60%的转化为
D.步骤②中,加入过量,步骤③中沉淀可完全溶解
10.(2023春·江苏南通·高三海安高级中学校考阶段练习)已知的含磷废水中的磷以磷酸及其盐的形式存在。某温度下,磷酸的与溶液的的关系如图,下列叙述不正确的是
A.该废水中离子浓度存在关系:
B.若逐渐增大该废水的,溶液中将将先增大后减小
C.室温下,的平衡常数
D.向废水中加入生成沉淀除磷后,溶液将增大
11.(2023·海南·海南中学校联考一模)常温下,三种物质的与的关系如图所示,已知:为阳离子浓度的负对数,为阴离子浓度的负对数。下列说法正确的是
A.常温下,溶度积:
B.O点对应的不饱和溶液
C.常温时,的平衡常数
D.常温下,向等浓度的和的混合溶液中逐滴加入溶液,先析出沉淀
12.(2023春·湖北恩施·高三校联考阶段练习)常温下,向1LpH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示。下列叙述错误的是
A.a点溶液中,水电离出的c(H+)=1×10-10mol•L-1
B.b点溶液中,水电离出的c(H+)=1×10-7mol•L-1
C.c点溶液中,c(Na+)>c(HCO)>c(CO)
D.d点溶液中,c(Na+)=2c(CO)+c(HCO)
13.(2023春·浙江杭州·高三校联考阶段练习)25℃时,将HCl气体缓慢通入0.1mol∙L-1的氨水中,溶液的pH、体系中粒子浓度的对数值(lgc)与反应物的物质的的关系如图所示。若忽略溶液体积变化,下列有关说法不正确的是
A.P2所示溶液:
B.t=0.5时,
C.25℃时,的电离平衡常数为10-9.25
D.P3所示溶液:
14.(2023秋·江苏泰州·高三校联考期末)室温下,下列实验探究方案能够达到探究目的的是
选项
探究方案
探究目的
A
向盛有Fe(NO3)2溶液的试管中滴加几滴稀硫酸,振荡,观察溶液颜色变化
SO具有氧化性
B
向盛有KMnO4溶液的试管中通入SO2,观察溶液颜色变化
SO2具有还原性
C
向盛有NaCl和KI混合溶液的试管中滴加几滴AgNO3溶液,振荡,观察沉淀颜色
Ksp(AgCl)>Ksp(AgI)
D
向试管中加入0.5 g淀粉和4 mL 2 mol·L-1 H2SO4溶液,加热。冷却后,向其中加入少量新制的Cu(OH)2,加热,观察现象
淀粉水解液中存在还原性糖
A.A B.B C.C D.D
二、原理综合题
15.(2023·山西临汾·统考二模)氮在自然界中的存在十分广泛。某实验小组对不同含氮物质做了相关研究。请回答下列问题:
(1)氨的用途十分广泛,是制造硝酸和氮肥的重要原料。298K、101kPa条件下。合成氨每产生2molNH3,放出92.2kJ热量。已知:
1molN-H键断裂吸收的能量约等于___________kJ。
(2)将NH3和NO2以一定的流速,分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中NO2含量,从而确定尾气脱氮率(即NO2的转化率),结果如图所示:
a点________(填“是”或“不是”)平衡状态;脱氮率a~b段呈现如图变化,原因是_________。
(3)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。
①该铁氮化合物的化学式为___________。
②该晶体结构的另一种晶胞表示中,N处于顶点位置,则Fe(III)、Fe(II)分别处于___________、___________位置。
(4)25℃时,将10mL0.03mol/LNH4Cl溶液和10mL0.01mol/LAgNO3溶液混合(忽略溶液混合后的体积变化),混合后溶液中c(Ag+)为____________[25℃时,Ksp(AgCl)=1.8×10-10]。用数字传感器探究AgCl的沉淀溶解平衡。实验测得悬浊液中溶解的氯化物浓度变化如图所示,其中a点表示AgCl溶于NH4Cl溶液形成的悬浊液,下列说法正确的是___________(填字母标号)。
a.b点可能加入了NH4Cl(s) b.c点后无黄色沉淀生成
c.d点c(Ag+)
相关试卷
这是一份2024届高三新高考化学大一轮专题练习—水溶液中的离子反应与平衡,共28页。试卷主要包含了单选题,原理综合题,工业流程题等内容,欢迎下载使用。
这是一份2024届高三新高考化学大一轮专题练习—水溶液中的离子反应与平衡,共25页。试卷主要包含了单选题,多选题,工业流程题等内容,欢迎下载使用。
这是一份2024届高三新高考化学大一轮专题练习:化学平衡(有答案),共23页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。








