

福建省泉州科技中学2022-2023学年高一上学期期中考试化学试题
展开
这是一份福建省泉州科技中学2022-2023学年高一上学期期中考试化学试题,共9页。试卷主要包含了 下列叙述中正确的是, 下列物质分类正确的组合是, 下列电离方程式错误的是,下列物质属于电解质的是,8ml·L-1Al3溶液B等内容,欢迎下载使用。
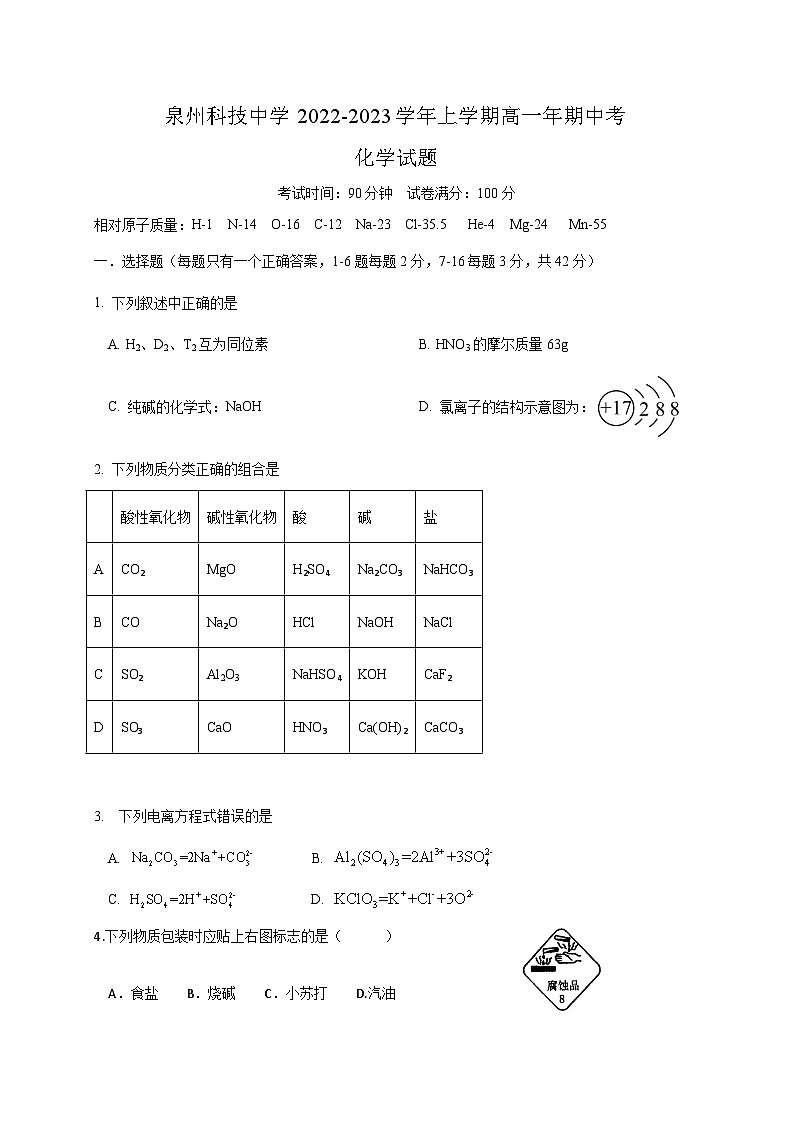
泉州科技中学2022-2023学年上学期高一年期中考化学试题考试时间:90分钟 试卷满分:100分 相对原子质量:H-1 N-14 O-16 C-12 Na-23 Cl-35.5 He-4 Mg-24 Mn-55一.选择题(每题只有一个正确答案,1-6题每题2分,7-16每题3分,共42分)1. 下列叙述中正确的是A. H2、D2、T2互为同位素 B. HNO3的摩尔质量63g C. 纯碱的化学式:NaOH D. 氯离子的结构示意图为:2. 下列物质分类正确的组合是 酸性氧化物碱性氧化物酸碱盐ACO2MgOH2SO4Na2CO3NaHCO3BCONa2OHClNaOHNaClCSO2Al2O3NaHSO4KOHCaF2DSO3CaOHNO3Ca(OH)2CaCO3 3. 下列电离方程式错误的是A. B. C. D. 4.下列物质包装时应贴上右图标志的是( ) A.食盐 B.烧碱 C.小苏打 D.汽油5.有人设想将碳酸钙通过的加工方法使之变为纳米碳酸钙(碳酸钙粒子直径是几纳米至几十纳米),这将引起建筑材料的性能发生巨变。下列关于纳米碳酸钙的推测可能发生的是A. 纳米碳酸钙的水溶液会浑浊不清B. 纳米碳酸钙分散到水中能产生丁达尔效应C. 纳米碳酸钙化学性质已与原来碳酸钙完全不同D. 纳米碳酸钙的粒子不能透过滤纸6. 氧化还原反应与四个基本反应类型的关系如下图所示,则下列化学反应属于阴影部分的是A. Cl2+2KBr=Br2+2KClB. 2NaHCO3Na2CO3+H2O+CO2↑C. 2Na2O2+2CO2=2Na2CO3+O2(提示:Na2O2中的氧元素显-1价)D. 4Fe(OH)2+O2+2H2O=4Fe(OH)37.下列物质属于电解质的是A.熔融的氯化钾 B.Cu C.CO2 D.食盐水8. 下列溶液中的物质的量浓度最大的是A. 5mL0.8mol·L-1Al(NO3)3溶液 B. 20mL1mol·L-1Mg(NO3)2溶液C. 20mL1.8mol·L-1AgNO3溶液 D. 30mL0.5mol·L-1Cu(NO3)2溶液9. 下列关于同温同压下的两种气体12C18O和14N2的判断正确的是A. 体积相等时密度相等 B. 原子数相等时具有的中子数相等C. 体积相等时具有的电子数相等 D. 质量相等时具有的质子数相等 10.用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )11. 下列有关实验现象的记录错误的是( )A. 用玻璃棒蘸取氯水滴在pH试纸上,可以测得氯水的pH值B. 红热的铜丝可以在氯气中燃烧,生成棕黄色的烟,溶于水形成蓝色溶液C. 氯气通入含有酚酞的氢氧化钠溶液,溶液红色褪去,再加入氢氧化钠,溶液不变色D. 氯水滴入碳酸钠溶液,有气体生成12. 在离子中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是A. x-25 B. A-x+25 C. A-x-23 D. x-2313. NA表示阿伏加德罗常数的值,下列说法正确的是A.常温常压下,11.2L氧气所含的O原子数为NAB.1mol/L的CaCl2溶液中含有的Cl﹣为2NAC.2.4g镁转化为Mg2+时失去的电子数目为0.2NAD.标准状况下,2g氦气所含原子数目为NA 14. 下列关于物质的检验的说法不正确的是( )A. 待检液中加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有NH4+B. 观察钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,置于煤气灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察C. 加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,一定含有SO42-D. 待检液中加入氯化钡溶液有白色沉淀生成,再加入盐酸,沉淀消失且产生无色无味的气体,则待检液中一定含有CO32-15. 现只用一种试剂(可以加热)鉴别 NH4Cl、(NH4)2SO4、K2SO4、 NaCl四种无色溶液,该试剂是 A. Ba(OH)2溶液 B. BaCl2溶液 C.AgNO3溶液 D. NaOH溶液16.分别用20mL1mol·L-1BaCl2溶液恰好可使体积比为1∶2∶3的硫酸铁、硫酸镁和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是A.3∶2∶1 B. 1∶2∶3 C. 1∶3∶3 D. 2∶3∶2 二.填空题(5题,共58分)17. (11分)自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。 Ⅰ.如图A为实验室制蒸馏装置示意图,根据图示回答下列问题。(1)图中有两处明显的错误是:①___________;②___________。(2)A仪器的名称是___________,B仪器的名称是___________。(3)实验时A中除加入液体混合物外,还需要加入少量的___________,其作用是___________。 Ⅱ.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D序号填入适当的空格中。(1)碳酸钙悬浊液中分离出碳酸钙___;(2)分离酒精和水___;(3)分离植物油和水___;(4)氯化钠溶液中分离出氯化钠___;(5)氯化钠溶液中分离出水___。18. (10分)设NA表示阿伏伽德罗常数的值,回答下列问题:(1)0.3molNH3分子中所含原子数与___个H2O分子中所含原子数相等。(2)将2.0g NaOH固体溶于水配成1.0L溶液,则所配制溶液的物质的量浓度为___。(3)同温同压下,同体积的H2和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为___。(4)448mL某气体在标准状况下的质量为1.28g,该气体的摩尔质量为___。(5)9.2g氮的氧化物NOX中N原子的物质的量为0.2mol,则x的数值为________。 19.(14分) 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。(1)装置Ⅰ中仪器c的名称是___,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___。(2)装置Ⅱ的作用是___(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___。(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___装置(填序号)。(5)有一种“地康法”制取氯气的反应原理如图所示:①反应Ⅰ属于___反应。(填四种基本反应类型之一)②在450℃条件下,反应Ⅱ的化学方程式为____。③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:______________________________。 20. (14分) “84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶84消毒液,该消毒液通常稀释到100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:84消毒液
【有效成分】NaClO
【规格】1000 mL
【质量分数】25%
【密度】1.19 g/cm3(1)该84消毒液NaClO物质的量浓度约为___(保留1位小数)。(2)工业上用Cl2与浓氢氧化钠溶液反应制取84消毒液,请写出反应的化学方程式____________________。(3)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是___(填字母)。A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器B.使用前要检查容量瓶是否漏液C.容量瓶上标有容积、温度和浓度D.需要称量NaClO固体的质量为149.0g
(4)一瓶上述84消毒液理论上能吸收空气中___L的CO2(标准状况下)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)(5)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因___,某消毒小组人员用18.4mol·L-1的浓硫酸配制500mL2.3mol·L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为___mL。(6)在配制稀硫酸过程中,下列操作中能使所配溶液的浓度偏高的有___(填代号)。①用量筒量取98%的硫酸时俯视②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中③转移前,容量瓶中含有少量蒸馏水④定容时,加蒸馏水超过标线,又用胶头滴管吸出⑤定容时,俯视刻度线⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线 21. (9分) 17.4g MnO2与240 mL 10 mol/L(密度为1.10g/mL)的盐酸(足量)混合加热(不考虑盐酸挥发),使其充分反应后,再向溶液中加入足量的AgNO3溶液。(已知:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O)试求:(1)10 mol/L的盐酸的质量分数 (2)产生的气体在标准状况下的体积 (3)产生沉淀的质量 泉州科技中学2022-2023学年上学期高一年期中考化学试题参考答案12345678910111213141516DDDBBCAACBABCCAD 【17答案-每空1分】 Ⅰ(1)①. 温度计水银球未置于支管口附近 ②. 冷凝管进出水方向上进下出 (2) ①. 蒸馏烧瓶 ②. 冷凝管 (3) ①. 沸石(或碎瓷片) ②. 防止暴沸 Ⅱ(1)B (2)A (3)C (4)D (5)A【18答案-每空2分】(1)2.408×10 23 (2)0.05mol/L (3)32g/mol (4)64g/mol (5) 2【19答案-除标注外其它每空2分】(1) ①. 分液漏斗(1分) ②. MnO2+4HClMnCl2+Cl2↑+2H2O (2)除去氯气中的氯化氢气体 (3)溶液先变红,后褪色 (4)④ (5)①. 复分解(1分); ②. 2CuCl2+O22CuO+2Cl2 ③. 3Cl2+8NH3=6NH4Cl+N2【20答案-每空2分】(1)4.0 (2)Cl2+2NaOH=NaCl+NaClO+H2O (3)AC (4)89.6 (5) ①. H2SO4+2NaClO=Na2SO4+2HClO ②. 62.5 (6)②⑤【21答案-每步3分】 ①. 33.2% ②. 4.48L ③. 287g
相关试卷
这是一份福建省泉州科技中学2023-2024学年高二上学期期中考试化学试题含答案,共11页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份福建省泉州科技中学2023-2024学年高一上学期期中考试化学试卷含答案,共14页。试卷主要包含了选择题,解答题等内容,欢迎下载使用。
这是一份福建省泉州科技中学2021-2022学年高一上学期期中考试化学试题【试卷+答案】,共9页。试卷主要包含了5 Zn-65,下列物质分类的正确组合是,2L H2中含有的氢分子数为0,现有下列九种物质等内容,欢迎下载使用。









