



所属成套资源:江苏省南通市如皋市2023-2024学年高三上学期期初考试押题
江苏省南通市如皋市2023-2024学年高三上学期期初考试押题化学试题
展开
这是一份江苏省南通市如皋市2023-2024学年高三上学期期初考试押题化学试题,文件包含精品解析江苏省南通市如皋市2024届高三上学期期初考试押题卷化学试题原卷版docx、精品解析江苏省南通市如皋市2024届高三上学期期初考试押题卷化学试题解析版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
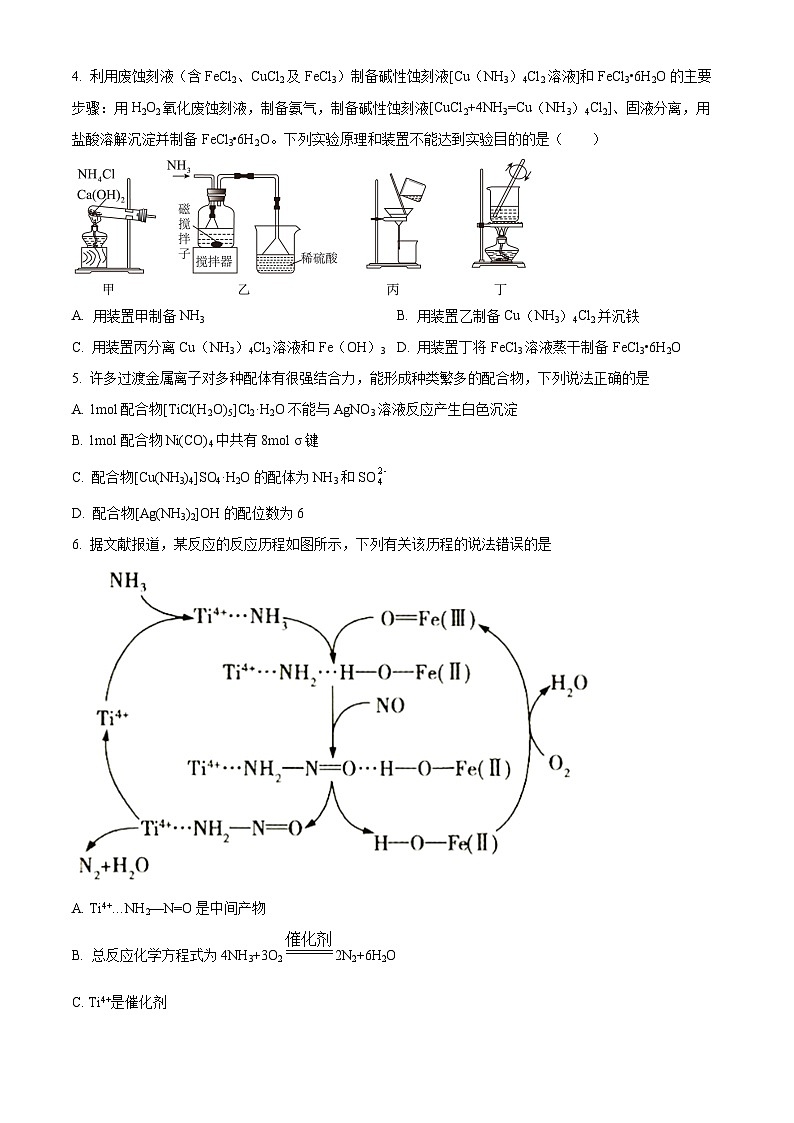
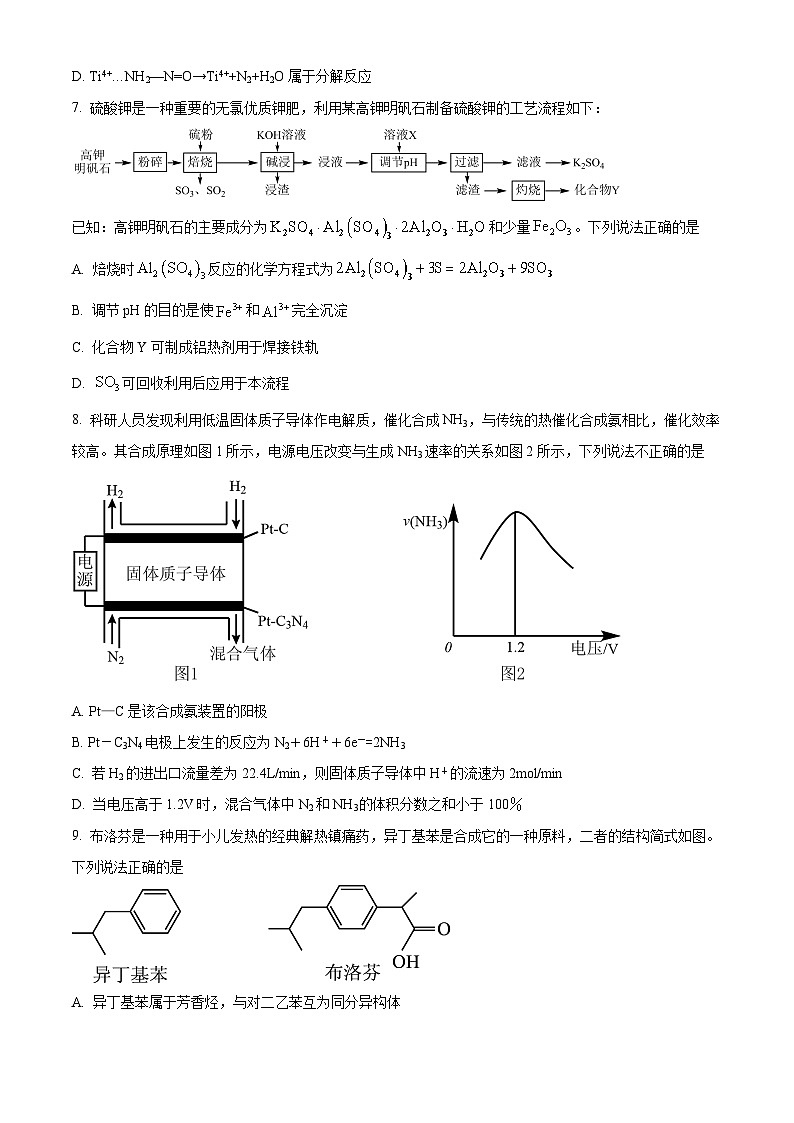
江苏省南通市如皋市2024届上学期期初考试押题卷化学学科一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。1. 新型冠状病毒可通过气溶胶传播,气溶胶属于胶体的一种。下列关于胶体的叙述,不正确的是A. 明矾净水利用了胶体的吸附性B. 依据丁达尔效应可将分散系分为溶液、胶体与浊液C. 雾是气溶胶,在阳光下可观察到丁达尔效应D. 用渗析法分离胶体与溶液2. 化学与生活密切相关。下列化学用语或描述表达正确的是A. 基态硫原子的轨道表示式: B. H2S的电子式: C. SO2的VSEPR模型: D. 中子数为9的氮原子N3. X、Y、Z、N是原子序数依次增大的4种短周期元素,其元素性质或原子结构如下表。下列说法正确的是元素元素性质或原子结构X原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能低于同周期相邻元素Y原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能高于同周期相邻元素Z其价电子中,在不同形状的原子轨道中运动的电子数相等N只有一个不成对电子 A. 原子半径:B. 元素的电负性:C. 元素的第一电离能:D. X的基态原子的电子轨道表示式:4. 利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl3•6H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3=Cu(NH3)4Cl2]、固液分离,用盐酸溶解沉淀并制备FeCl3•6H2O。下列实验原理和装置不能达到实验目的的是( )A. 用装置甲制备NH3 B. 用装置乙制备Cu(NH3)4Cl2并沉铁C. 用装置丙分离Cu(NH3)4Cl2溶液和Fe(OH)3 D. 用装置丁将FeCl3溶液蒸干制备FeCl3•6H2O5. 许多过渡金属离子对多种配体有很强结合力,能形成种类繁多的配合物,下列说法正确的是A. 1mol配合物[TiCl(H2O)5]Cl2·H2O不能与AgNO3溶液反应产生白色沉淀B. 1mol配合物Ni(CO)4中共有8mol σ键C. 配合物[Cu(NH3)4]SO4·H2O的配体为NH3和SOD. 配合物[Ag(NH3)2]OH的配位数为66. 据文献报道,某反应的反应历程如图所示,下列有关该历程的说法错误的是A. Ti4+…NH2—N=O是中间产物B. 总反应化学方程式为4NH3+3O22N2+6H2OC. Ti4+是催化剂D. Ti4+…NH2—N=O→Ti4++N2+H2O属于分解反应7. 硫酸钾是一种重要的无氯优质钾肥,利用某高钾明矾石制备硫酸钾的工艺流程如下:已知:高钾明矾石的主要成分为和少量。下列说法正确的是A. 焙烧时反应的化学方程式为B. 调节pH的目的是使和完全沉淀C. 化合物Y可制成铝热剂用于焊接铁轨D. 可回收利用后应用于本流程8. 科研人员发现利用低温固体质子导体作电解质,催化合成NH3,与传统的热催化合成氨相比,催化效率较高。其合成原理如图1所示,电源电压改变与生成NH3速率的关系如图2所示,下列说法不正确的是 A. Pt—C是该合成氨装置的阳极B. Pt-C3N4电极上发生的反应为N2+6H++6e-=2NH3C. 若H2的进出口流量差为22.4L/min,则固体质子导体中H+的流速为2mol/minD. 当电压高于1.2V时,混合气体中N2和NH3体积分数之和小于100%9. 布洛芬是一种用于小儿发热的经典解热镇痛药,异丁基苯是合成它的一种原料,二者的结构简式如图。下列说法正确的是A. 异丁基苯属于芳香烃,与对二乙苯互为同分异构体B. 异丁基苯和布洛芬中碳原子均有和杂化C. 1mol布洛芬与足量溶液反应生成D. 两者均能发生加成、取代和消去反应10. 含氮物质可发生如下反应:①②③下列说法正确的是A. 常温下,NO与混合能立即看到红棕色气体,说明该反应已达平衡B. 反应②的C. 反应③消耗,理论上会生成标准状况下约D. 利用反应①、②、③可以同时处理含量较高的废气和含的废水11. 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是选项实验操作和现象结论A向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色X溶液中一定含有Fe2+B向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色Br2的氧化性比I2的强C用pH试纸测得: CH,COONa溶液的pH约为9,NaNO2溶液的pH约为8HNO2电离出H+的能力一定比CH3COOH的强D将Na2SO3样品溶于水,滴加稀盐酸酸化Ba( NO3)2溶液,产生白色沉淀Na2SO3样品已变质 A. A B. B C. C D. D12. 室温下,通过下列实验探究的性质。已知:25℃时,的、的。实验1:配制溶液,测得溶液约为12;实验2:取溶液,向其中加入少量固体充分搅拌,一段时间后过滤。向滤渣中加入足量稀盐酸,固体完全溶解;实验3:取溶液,向其中缓慢滴入等体积稀盐酸。下列说法正确的是A. 实验1所得溶液中,B. 根据实验2,可推测C. 实验3反应后溶液中存在:D. 25℃时,反应平衡常数13. 碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如下:反应I ;反应Ⅱ 在不同容器中分别发生反应I、反应Ⅱ,不同压强(P1或P2)下分别达平衡时,两个反应中随温度变化的关系如图所示。下列说法正确的是 A. 压强大小:B. 在如图所示条件下,反应I可表示为 C. 选择反应Ⅱ的小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌反应能顺利进行D. 一定条件下将C与ZnO置于同一密闭容器中反应,当时,增大的值,可减少平衡时气体中的含量二、非选择题:共4题,共61分。14. 五氧化二钒是广泛用于冶金、化工等行业的催化剂。工业上以石煤(主要成分为,含有少量、等杂质)为原料制备,主要经过“焙烧、水浸、除杂、沉钒、灼烧”等过程。已知:①溶于水,难溶于水。②,。回答下列问题:(1)向石煤中加纯碱,在通入空气的条件下焙烧,转化为,该反应的化学方程式为_______。(2)向水浸后的溶液中加入生成、沉淀以除去硅、磷,除杂后的溶液中的浓度为,此时溶液中_______;磷、硅去除率随温度变化的曲线如图所示,随着温度升高除磷率下降而除硅率升高,可能的原因是_______。(3)“沉矾”时加入析出,沉钒温度需控制在50℃左右,温度不能过高的原因为_______。(4)在空气中灼烧得。称取0.80g灼烧后的产物,加入稀硫酸溶解后,向其中加入溶液25mL,再用溶液滴定过量的溶液至终点,消耗溶液的体积为4.00mL,则产物中的质量分数为_______(写出计算过程)。已知: (5)还原可制得,如图为的晶胞,该晶胞中钒的配位数为_______。
15. 化合物J是一种昆虫生长调节剂,其人工合成路线如下:(1)C的分子式,其结构简式为___________。(2)合成时不采用的方法,原因是___________。(3)F→G反应需控制在130℃左右,温度过高会有一种分子式为的副产物生成,该副产物的结构简式为___________。(4)H的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___________。①能发生银镜反应,能与溶液发生显色,碱性条件水解②分子中含有4种不同化学环境的氢原子;(5)已知:。写出以甲苯、为原料制备的合成路线流程图_____________(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。16. 汽车尾气已成为城市空气主要污染源,治理汽车尾气的SCR(选择性催化还原)和NSR (NOx储存还原)技术均可有效降低柴油发动机工作过程中排放的NOx。(1)SCR工作原理①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式是___________。②反应器中NH3还原NO2的化学方程式是___________。(2)NSR(NOx储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx 的储存和还原。①BaO吸收NO2的反应中氧化剂与还原剂的物质的量之比是___________。②富燃条件下Pt表面反应的化学方程式是___________。③若柴油中硫含量较高,在稀燃过程中,BaO吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因:___________。④研究发现:尾气中的CO2对BaO吸收氮氧化物有影响。一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如下图所示。则:一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因是___________;当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,原因可能是___________。17. CuCl用作有机合成催化剂等工业。CuCl露置于潮湿的空气中易被氧化和水解,酸性条件下易歧化,难溶于水,易溶于浓盐酸并生成[CuCl2]-。(1)基态Cu+核外电子排布式是_______。(2)实验测得:CuCl属于共价化合物,气态CuCl分子的相对分子质量为199,该分子中含有配位键,则气态CuCl分子的结构式可能为_______。(3)已知:①Ksp(CuCl)≈1×10-7,②反应2Cu+=Cu+Cu2+平衡常数K≈1×106。有人预设用反应Cu(s)+Cu2++2Cl-=2CuCl(s)制备CuCl (s),试预测该反应进行的程度大小:_______ (填写“几乎完全反应”或“几乎不反应”)。工业上有多种制备CuCl的方法:方法一:将废铜粉与食盐水、浓盐酸料液混合,在60~70℃缓慢通入空气进行氧化。静置,取上层清液加水稀释,生成CuCl沉淀,过滤,沉淀经洗涤、干燥得CuCl产品并真空保存。方法二:将Na2SO3的水溶液逐滴加入CuCl2的水溶液中,再加入少量浓盐酸混匀,充分反应后过滤,沉淀经洗涤、干燥得CuCl产品并真空保存。(4)“方法一”中:①反应温度控制在60~70℃,目的是_______。②加入浓盐酸的目的是_______。(5)“方法二”中:①总反应的离子方程式是_______。②加入Na2SO3溶液体积(V)与溶液pH关系如图1。当Na2SO3溶液体积大于500 mL时,溶液pH增大的原因是_______。③用酸或碱液调控反应混合液的pH,则CuCl产率见图2。pH<2.5时,CuCl产率相对较低;pH>3.5时,CuCl产率又迅速下降。试分析原因: _______。
相关试卷
这是一份江苏省泰州中学2023-2024学年高三上学期期初调研考试化学试题,共11页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。
这是一份江苏省泰州中学2023-2024学年高三上学期期初调研考试化学试题,共11页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。
这是一份2021-2022学年江苏省南通市如皋市高二下学期期初调研化学试题(Word版),共11页。试卷主要包含了 下列图示与对应的叙述相符的是等内容,欢迎下载使用。









