



2024届高三化学高考备考一轮复习专题:卤代烃、醇、酚、醛、酮和羧酸课件
展开1.能写出卤代烃、醇、酚、醛、酮、羧酸的类别通式、官能团、简单代表物的结构简式及名称,能列举各类有机化合物的典型代表物的主要物理性质。
2.能描述说明、分析解释卤代烃、醇、酚、醛、酮、羧酸的典型代表物的重要反应,能书写相应的化学方程式。
3.能基于官能团、价键类型、特点及反应规律分析和推断含有典型官能团的有机化合物的化学性质。
烃分子里的氢原子被 卤素原子 取代后生成的化合物。通式可表示为R—X(其中R—表示烃基),官能团名称为 碳卤键 。
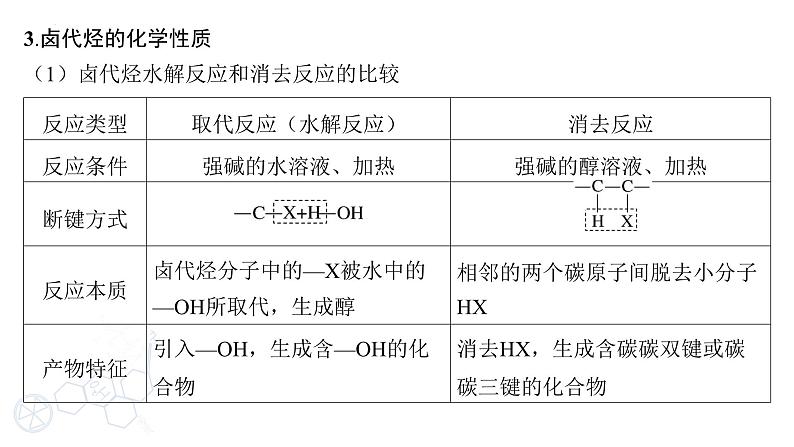
(1)卤代烃水解反应和消去反应的比较
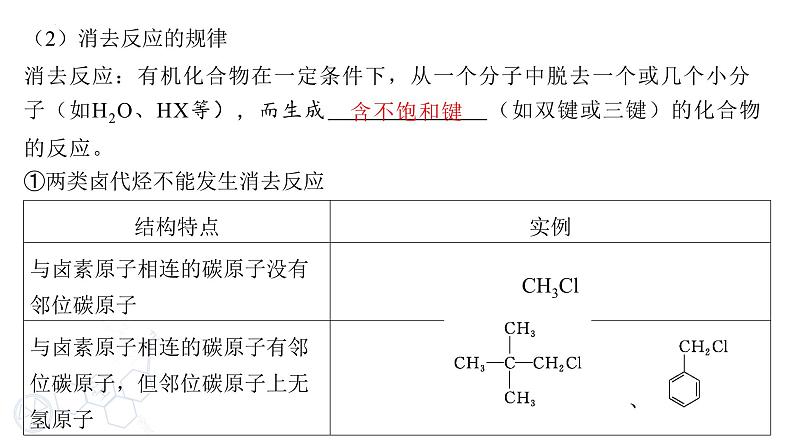
消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成 含不饱和键 (如双键或三键)的化合物的反应。
①两类卤代烃不能发生消去反应
②有两种或三种邻位碳原子,且碳原子上均带有氢原子时,发生消去反应可生成不同的产物。例如: +NaOH
③ 型卤代烃,发生消去反应可以生成R—C≡C—R',如BrCH2CH2Br+2NaOH CH≡CH↑+2NaBr+2H2O。
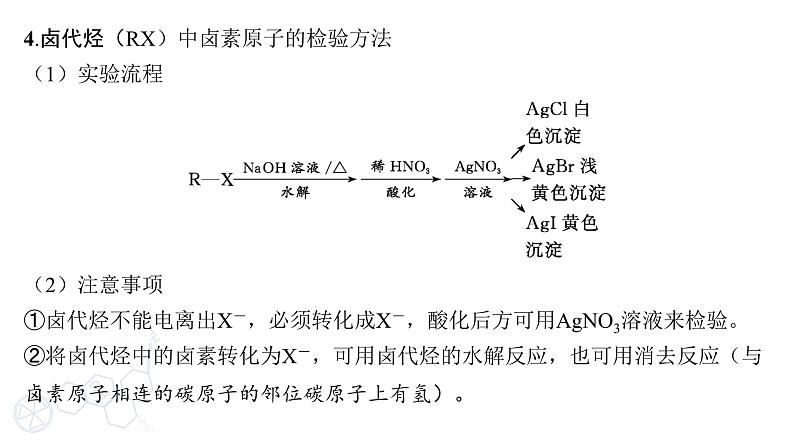
4.卤代烃(RX)中卤素原子的检验方法
①卤代烃不能电离出X-,必须转化成X-,酸化后方可用AgNO3溶液来检验。
②将卤代烃中的卤素转化为X-,可用卤代烃的水解反应,也可用消去反应(与卤素原子相连的碳原子的邻位碳原子上有氢)。
1.正误判断(正确的打“√”,错误的打“×”)。
(1)CH3CH2Cl的沸点比CH3CH3的沸点高。( )
(2)溴乙烷与NaOH的乙醇溶液共热生成乙烯。( )
(3)在溴乙烷中加入AgNO3溶液,立即产生淡黄色沉淀。( )
(4)取溴乙烷的水解液,向其中加入AgNO3溶液,可观察到淡黄色沉淀。( )
(5)所有卤代烃都能够发生水解反应和消去反应。( )
2.下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
A.CH3Cl B.
C. D.
3.在有机反应中,反应物相同而条件不同,可得到不同的主产物,如:
请写出实现下列转变的合成路线图。
(1)由CH3CH2CH2CH2Br通过两步反应合成 。
答案:CH3CH2CH2CH2Br
(2)由CH3CH2CH2CH2Br通过三步反应合成 。
(1)概念:羟基与烃基或苯环侧链上的碳原子相连的化合物。饱和一元醇的分子通式为 CnH2n+1OH(n≥1) 。
CnH2n+1OH(n≥1)
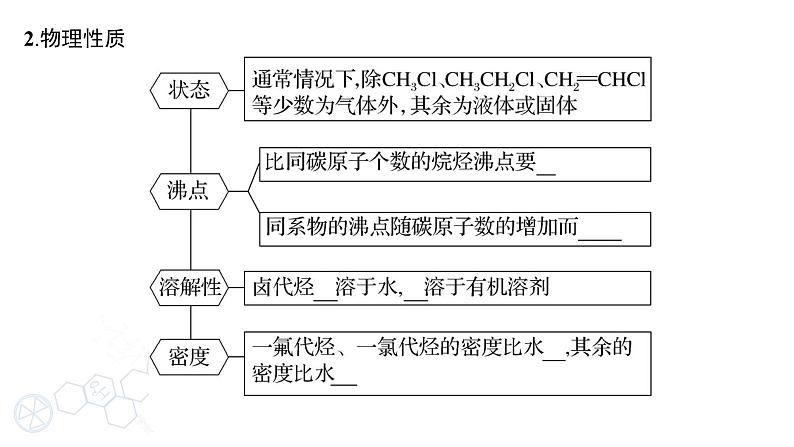
2.物理性质的递变规律
(2)醇分子的断键部位及反应类型
以1-丙醇为例,完成下列条件下的化学方程式,并指明断键部位。
3.醇类的化学性质(1)根据结构预测醇类的化学性质醇的官能团羟基(—OH),决定了醇的主要化学性质,受羟基的影响,C—H的极性增强,一定条件也可能断键发生化学反应。
d.浓硫酸,加热,分子内脱水
CH3CH2CH2OH+CH3COOH
CH3COOCH2CH2CH3+H2O , ① 。
CH3CH2CH2OH
CH3CH2CH2OH+CH3COOH
CH3COOCH2CH2CH3+H2O
2CH3CH2CH2OH+O2 2CH3CH2CHO+2H2O , ①③ 。
2CH3CH2CH2OH+O2
2CH3CH2CHO+2H2O
(1)概念:羟基与苯环直接相连而形成的化合物,最简单的酚为苯酚 ( )
(1)羟基中氢原子的反应
b.与活泼金属反应:与Na反应的化学方程式为
c.与碱反应:苯酚的浑浊液 液体变 澄清 溶液又变 浑浊 。
(2)苯环上氢原子的取代反应
苯酚与饱和溴水反应的化学方程式为
反应产生白色沉淀,此反应常用于苯酚的定性检验和定量测定。
该过程中发生反应的化学方程式分别为
与H2反应的化学方程式为
+3H2 。
苯酚与FeCl3溶液作用显 紫 色,利用这一反应可以检验苯酚的存在。
(1)医用酒精的浓度通常为95%。( )
(2)0.1 ml乙醇与足量的钠反应生成0.05 ml H2,说明每个乙醇分子中有一个羟基。( )
(3)CH3OH和 都属于醇类,且二者互为同系物。( )
(4)CH3CH2OH在水中的溶解度大于 在水中的溶解度。( )
(5)CH3OH、CH3CH2OH、 的沸点逐渐升高。( )
(6)所有的醇都能发生氧化反应和消去反应。( )
(7) 和 含有的官能团相同,二者的化学性质相似。( )
2.结合下表已知信息,判断下列相关叙述正确的是( )
3.白藜芦醇具有抗癌性,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中。其结构简式如图所示:
(1)能够跟1 ml该化合物反应的NaOH的最大物质的量是 。
(2)能够跟1 ml该化合物反应的Br2、H2的最大物质的量分别是 、 。
答案:6 ml 7 ml
4.下列四种有机物的分子式均为C4H10O。
①CH3CH2CH2CH2OH
分析其结构特点,用序号解答下列问题:
(1)其中能与钠反应产生H2的有 。
(2)能被氧化成含相同碳原子数的醛的是 。
(3)能被氧化成酮的是 。
(4)能发生消去反应且生成两种产物的是 。
(1)醇能否发生催化氧化及氧化产物类型取决于醇分子中是否有α-H及其个数:
(2)醇能否发生消去反应取决于醇分子中是否有β-H,若β碳原子上没有氢原子,则不能发生消去反应。
饱和一元醛的通式: CnH2nO(n≥1) ,饱和一元酮的通式: CnH2nO(n≥3) 。
CnH2nO(n≥1)
(2)常见的醛、酮及物理性质
(3)醛、酮的化学性质
①醛类的氧化反应(以乙醛为例)
②醛、酮的还原反应(催化加氢)
+H2 。
CH3COONH4+2Ag↓+3NH3+
+Cu2O↓+3H2O
③醛、酮与具有极性键共价分子的酮羰基加成反应:
(1)概念:由烃基或氢原子与羧基相连而构成的有机化合物。官能团名称为 羧基 ,饱和一元羧酸的分子通式为 CnH2nO2(n≥1) 。
(2)甲酸和乙酸的分子组成和结构
CnH2nO2(n≥1)
羧酸的性质取决于羧基,反应时的主要断键位置如图:
CH3CO18OCH2CH3+H2O
1.柔红酮是一种医药中间体,其结构简式如图所示。下列说法正确的是( )
2.某研究性学习小组,要设计检验柠檬醛( )中所含官能团的实验方案,需思考如下问题:
(1)检验分子中醛基常用的试剂是 ,化学方程式: (用通式RCHO表示)。
(2)检验碳碳双键常用的试剂是 。
答案:酸性KMnO4溶液(或溴的CCl4溶液)
(3)若只有酸性高锰酸钾溶液、新制的氢氧化铜和稀硫酸,应先检验的官能团是 ,原因是 ;操作过程是 。
答案:醛基 醛基、碳碳双键均能使酸性KMnO4溶液褪色 取少量柠檬醛,加入足量新制的氢氧化铜,加热煮沸,产生砖红色沉淀,证明含有醛基,充分反应后,用稀硫酸调至溶液呈酸性,再滴加酸性高锰酸钾溶液,溶液褪色,证明分子中还含有碳碳双键
3.已知某有机物的结构简式为 。
(1)当和 反应时,可转化为 。
(2)当和 反应时,可转化为 。
答案:NaOH(或Na2CO3)
(3)当和 反应时,可转化为 。
醇、酚、羧酸分子中羟基氢原子的活泼性比较
新信息考查官能团的结构和性质
1.γ-崖柏素具有天然活性,有酚的通性,结构如图。关于γ-崖柏素的说法错误的是( )
2.莲藕含多酚类物质,其典型结构简式如图所示。下列有关该类物质的说法错误的是( )
1.熟记常见官能团的名称、结构与性质
2.明确官能团反应中的7个定量关系
(1)1 ml 发生加成反应需1 ml H2(或Br2)。
(2)1 ml 发生加成反应需3 ml H2。
(3)1 ml —COOH 1 ml CO2。
(5)1 ml酚酯在碱性条件下充分水解最多可消耗2 ml NaOH。
(6)酚羟基每有1个邻位或对位氢原子,即可消耗1个溴分子发生取代反应。
(7)1 ml —COOR在酸性条件下水解消耗1 ml H2O。
1.有机物E具有抗肿瘤、镇痉等生物活性,它的一种合成方法的最后一步如下。下列说法正确的是( )
2.一种合成吲哚-2-酮类药物的中间体,其结构如图所示,下列有关X的说法不正确的是( )
3.一种具有广谱抗菌活性的有机物结构简式如图,下列关于该有机物的说法错误的是( )
4.中医药是中华民族的传统瑰宝,化合物Z是一种药物成分的中间体,可由有机物X和Y一定条件下合成,反应如下:
X Y
Z
下列说法中正确的是( )
乙酸乙酯的制备与性质探究
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量的产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。(1)配制①中混合溶液的方法为 ; 反应中浓硫酸的作用是 ;写出制取乙酸乙酯的化学方程式: 。
(2)上述实验中饱和碳酸钠溶液的作用是 (填字母)。
(3)步骤②中需要小火均匀加热,其主要理由是 ;步骤③所观察到的现象是 ;欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有 ;分离时,乙酸乙酯应从仪器 (填“下口放出”或“上口倒出”)。
答案:大火加热会导致大量的乙醇原料汽化而损失 液体分层,上层为无色有香味液体,下层为浅红色液体,振荡后下层液体颜色变浅 分液漏斗 上口倒出
(4)该同学反复实验,记录乙醇和乙酸的用量及乙酸乙酯的生成量数据如下表:
表中数据x的范围是 ;实验①②⑤探究的是 。
答案:1.57~1.76 增加乙醇或乙酸的用量对乙酸乙酯产量的影响
2024届高三化学高考备考一轮复习专题:醛 羧酸 羧酸衍生物课件PPT: 这是一份2024届高三化学高考备考一轮复习专题:醛 羧酸 羧酸衍生物课件PPT,共60页。PPT课件主要包含了烃基或氢原子,RCHO,HCHO,刺激性,CH3CHO,酮的化学性质,COOH,2羧酸的分类,3几种重要的羧酸,高级脂肪酸等内容,欢迎下载使用。
2024届高三化学高考备考一轮复习专题:卤代烃 醇 酚课件: 这是一份2024届高三化学高考备考一轮复习专题:卤代烃 醇 酚课件,共46页。PPT课件主要包含了卤素原子,碳卤键,物理性质,化学性质,不饱和键,卤代烃的制备,课堂点拨,醇的概述,醇类的物理性质,醇类的化学性质等内容,欢迎下载使用。
2024届高三化学高考备考一轮复习:卤代烃 醇与酚 醛与酮课件: 这是一份2024届高三化学高考备考一轮复习:卤代烃 醇与酚 醛与酮课件,共60页。PPT课件主要包含了卤代烃的化学性质,CH≡CH,HCl,3醇的分类,易溶于,苯酚的物理性质,+n-1H2O,RCH2OH,RCOOH,+H2O等内容,欢迎下载使用。












