






氢氧化钠和氢氧化钙变质-中考化学一轮复习课件PPT
展开
这是一份氢氧化钠和氢氧化钙变质-中考化学一轮复习课件PPT,共24页。PPT课件主要包含了氢氧化钠变质,氢氧化钙变质,例题精讲,实验与结论,有白色沉淀产生,有蓝色沉淀产生,将溶液中的碳酸钠除尽,CaOH2,实验步骤与现象等内容,欢迎下载使用。
一、氢氧化钠变质的探究
CO2+2NaOH=Na2CO3+H2O
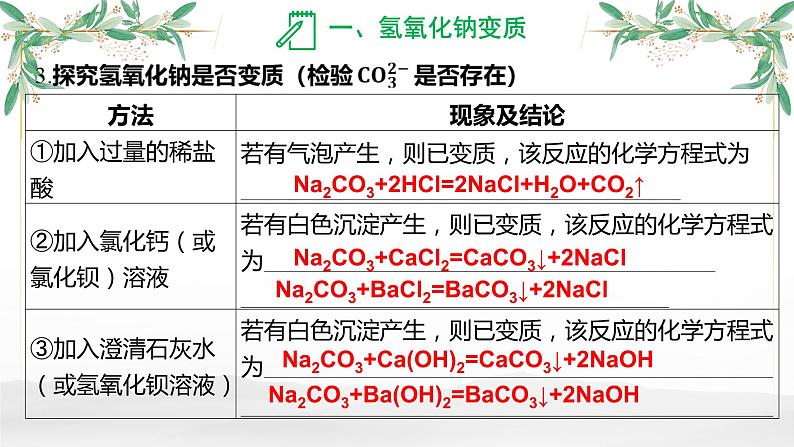
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+CaCl2=CaCO3↓+2NaCl
Na2CO3+BaCl2=BaCO3↓+2NaCl
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ba(OH)2=BaCO3↓+2NaOH
碳酸钠溶液也呈碱性,也能使无色酚酞溶液变红
(2)探究氢氧化钠是部分变质还是完全变质时,不能选用澄清石灰水或氢氧化钡溶液,原因是__________________________________________________________。
二者含有的氢氧根离子会对原溶液中氢氧根离子的检验造成干扰
(3)检验氢氧化钠是否变质时,需要加入______的稀盐酸,原因是_____________________________________________________________________________。
加入稀盐酸的量不能将氢氧化钠反应完或恰好将氢氧化钠反应完时,不会有气泡产生
二、氢氧化钙变质的探究
CO2+Ca(OH)2=CaCO3↓+H2O
3.探究氢氧化钙是否变质 取样,加入足量稀盐酸,有______产生,证明氢氧化钙已经变质,反应的化学方程式为____________________________________。 【小贴士】由于氢氧化钙微溶于水,不能通过加水溶解,观察溶液中是否有沉淀析出来判断氢氧化钙溶液是否变质。
例1.下列实验中,根据实验现象不能得到相应结论的是( )
例2.某化学兴趣小组的同学们发现了一瓶生产时间较久远的氢氧化钠固体,进行如图所示实验,成功探究出该久置氢氧化钠固体的变质程度。下列说法正确的是( )
A.氢氧化钠变质是因为吸收了空气中的水蒸气导致B.甲溶液可以选择稀盐酸或BaCl2溶液C.溶液B中的溶质一定只含有NaOH和甲D.步骤Ⅱ出现白色沉淀,步骤Ⅲ酚酞溶液变成红色,则说明样品部分变质
例3.分离、检验、鉴别、除杂等是最基本的实验技能。下列实验设计能达到实验目的的是( )
例4.酸、碱、盐是我们身边重要的物质,有着较广泛的用途。请回答下列问题(1)盛有氢氧化钠溶液的试剂瓶,如果密封不好,氢氧化钠就会变质。①写出氢氧化钠变质的化学方程式:________________________。②既能证明氢氧化钠变质,又能除去变质氢氧化钠中的杂质,该试剂是 ______(填序号)。A.稀盐酸B.Ca(OH)2溶液C.CaCl2溶液D.稀硫酸③变质后的氢氧化钠溶液,其pH (填“>7”“<7”或“=7”)。
2NaOH+CO2=Na2CO3+H2O
例5. 氢氧化钠是化工生产的重要原料,保存不妥易发生变质。某化学兴趣小组的同学在实验室中发现一瓶敞口放置的氢氧化钠溶液,对其是否变质以及变质程度产生了兴趣。【提出问题】氢氧化钠溶液是否变质及变质的程度?【猜想与假设】①没有变质;②部分变质;③全部变质。
【评价与解释】 实验结束后,小组同学对两种方案得出的结论不同进行了充分讨论,一致认为方案二科学合理,方案一有明显漏洞。你认为方案一的漏洞导致结论错误的原因是_______________________________________________;方案二中加入过量氯化钡溶液的目的是_______________________,向清液中滴加硫酸铜溶液后发生反应的化学方程式为_ ________________________________________。
滴入的稀盐酸的量过少,稀盐酸只与氢氧化钠反应
【反思与交流】 小明提出可以用氢氧化钡溶液替换氯化钡溶液,你是否认同并说明原因___________________________________________________________________________________。
不认同,使用氢氧化钡溶液会引入氢氧根离子,会对原物质中的氢氧根离子的检验造成干扰
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
【拓展延伸】 (1) 该氢氧化钠溶液变质的原因是_______________________________(用化学方程式表示),因此需______保存。
(2) 若要除去部分变质的氢氧化钠溶液中的碳酸钠,应在溶液中滴加________________________________,充分反应后再过滤。
适量氢氧化钙(或氢氧化钡)溶液
例6.农场需用熟石灰改良酸性土壤,为了确保改良效果,需要对库存的熟石灰是否变质进行检测。农场实验室取了一定量的熟石灰样品,对其成分进行如下探究。【提出问题】熟石灰样品的成分是什么?
【作出猜想】 猜想一:___________;
【实验分析】 (1) 实验人员根据步骤1认为猜想三正确。其实该结论并不严谨,请说明理由:____________________________________________________________。
(2) 解释步骤3有气泡产生的原因(用化学方程式表示):____________________________________。
【实验结论】 通过以上实验可以知道猜想____正确。
【评价与反思】熟石灰存放时应密封保存。农业上使用库存较久的熟石灰时要检测其成分。
CaCO3+2HCl=CaCl2+H2O+CO2↑
例7.某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠和一瓶未标浓度的稀盐酸,为测定氢氧化钠的变质情况和稀盐酸的浓度,他们取9.3g变质的氢氧化钠样品于锥形瓶中,加入50g水,充分溶解,再向锥形瓶中滴加未知浓度的稀盐酸,实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示。求:(1)9.3g样品中碳酸钠的质量。(2)未知浓度的稀盐酸的溶质质量分数。(3)加入50g稀盐酸时,溶液中溶质的质量分数。
(1)由图中数据可知,生成二氧化碳的质量为:(9.3g+50g+50g)﹣107.1g=2.2g,设9.3g样品中碳酸钠的质量为x,与碳酸钠反应的盐酸的质量为y,Na2CO3+2HCl═2NaCl+H2O+CO2↑106 73 44 x y 2.2g
x=5.3g,y=3.65g答:9.3g样品中碳酸钠的质量为5.3g。
(2)由(1)可知,与碳酸钠反应的氯化氢的质量为3.65g,则9.3g样品中氢氧化钠的质量为:9.3g﹣5.3g=4g,设与氢氧化钠反应的盐酸的质量为z,NaOH+HCl═NaCl+H2O40 36.54g z
z=3.65g所以反应的盐酸的总质量为:3.65g+3.65g=7.3g,则未知浓度的稀盐酸的溶质质量分数为:
×100%=14.6%答:未知浓度的稀盐酸的溶质质量分数为14.6%。
相关课件
这是一份中考化学二轮复习专题课件- 氢氧化钠变质的探究 (含答案),共16页。PPT课件主要包含了氢氧化钠是否变质了,课堂练习一,氢氧化钠没有变质,氢氧化钠全部变质,氢氧化钠部分变质,种情况,只有NaOH,只有Na2CO3,课堂练习二,课堂练习三等内容,欢迎下载使用。
这是一份中考化学二轮专题复习专题课件:氢氧化钠变质的探究 (含答案),共16页。PPT课件主要包含了氢氧化钠是否变质了,课堂练习一,氢氧化钠没有变质,氢氧化钠全部变质,氢氧化钠部分变质,种情况,只有NaOH,只有Na2CO3,课堂练习二,课堂练习三等内容,欢迎下载使用。
这是一份2023年中考化学复习---探究氢氧化钠变质课件,共21页。PPT课件主要包含了学习目标,已变质等内容,欢迎下载使用。








