



2022-2023 高考化学 核心知识 专题8 电化学课件PPT
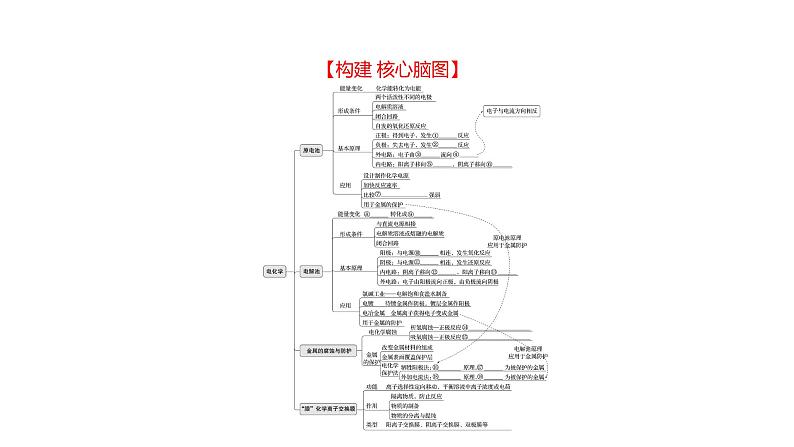
展开【排查 必备知识】【易错·排雷】 1.规避原电池工作原理的3个易错点(1)并非所有的氧化还原反应都能设计成原电池,只有放热的才可以设计成原电池。(2)溶液中阴阳离子与导线中电子的定向移动组成闭合回路。(3)活泼金属不一定作负极,如铝-NaOH溶液-镁电池中相对更活泼的金属镁作正极而铝作负极。
2.规避电解池电极反应的2个易错点(1) 电解池两电极的活泼性可不同,也可以相同。(2)阴极无论是惰性电极还是金属电极都不参与电极反应,发生反应的是溶液中的阳离子。3.规避金属腐蚀的3个易错点(1)电化学腐蚀类型多以吸氧腐蚀为主。(2)铜不能发生析氢腐蚀,只能发生吸氧腐蚀。(3)原电池反应是导致金属腐蚀的主要原因,但其仍能用来减缓金属的腐蚀。
【诊断·辨析】1.原电池(1)在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生。( )提示:电子不经过电解质溶液。(2)原电池工作时,溶液中的阳离子向负极移动,盐桥中的阳离子向正极移动。( )提示:阳离子向正极移动,阴离子移向负极。(3)某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥内可以是含琼脂的KCl饱和溶液。( )提示:琼脂中少量的Cl-会进入AgNO3溶液和银离子反应。(4)把锌片和铜片用导线连起来,浸入食盐水中,不能形成原电池。( )提示:发生了吸氧腐蚀形成原电池。
2.化学电源(1)碱性锌锰电池是一次电池,其中MnO2是催化剂,可使碱性锌锰电池的比能量高、可储存时间长。( )提示:碱性锌锰电池中MnO2是氧化剂参与电极反应。(2)铅酸蓄电池放电时,正极与负极质量均增加。( )提示:铅酸蓄电池放电时,负极铅、正极二氧化铅均转变为硫酸铅,质量均增加。(3)以葡萄糖为燃料的微生物燃料电池,放电过程中,H+从正极区向负极区迁移。( )提示:在原电池中阳离子在电解质溶液中移向正极。
3.电解原理(1)直流电源跟电解池连接后,电子从电源负极流向电解池阳极。( )提示:电解时电子从电源负极流向电解池阴极。(2)电解CuCl2溶液,阳极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色。( )提示:电解CuCl2溶液时,在阳极Cl-失电子变为Cl2,Cl2与KI反应生成I2。(3)电解盐酸、硫酸等溶液,H+放电,溶液的pH逐渐增大。( )提示:电解H2SO4溶液时,实际是电解H2O的过程,故溶液中c(H+)增大,pH减小。(4)用惰性电极电解饱和食盐水一段时间后,加入盐酸可使电解质溶液恢复到电解前的状态。( )提示:电解饱和食盐水,两极产生H2和Cl2,通入HCl气体即可使电解质溶液恢复到电解前的状态。
2022-2023 高考化学 核心知识 专题13 有机化学基础课件PPT: 这是一份2022-2023 高考化学 核心知识 专题13 有机化学基础课件PPT,共9页。
2022-2023 高考化学 核心知识 专题12 物质结构与性质课件PPT: 这是一份2022-2023 高考化学 核心知识 专题12 物质结构与性质课件PPT,共7页。
2022-2023 高考化学 核心知识 专题11 化学实验基础课件PPT: 这是一份2022-2023 高考化学 核心知识 专题11 化学实验基础课件PPT,共11页。PPT课件主要包含了构建核心脑图等内容,欢迎下载使用。












