





所属成套资源:全套中考化学复习高频考点集中练课件
中考化学复习高频考点集中练5金属的化学性质课件
展开
这是一份中考化学复习高频考点集中练5金属的化学性质课件,共24页。PPT课件主要包含了ZnNO32,AgNO3,CuAg,Fe2+等内容,欢迎下载使用。
类型一:金属活动性顺序的判断方法指导 (1)利用金属与氧气反应:金属与氧气反应的难易程度以及剧烈程度可以判断金属的活动性强弱。(较少用)(2)利用金属与稀酸的反应:若金属能与稀盐酸或稀硫酸反应,则其活动性位于氢前,若不能与稀盐酸或稀硫酸反应,则其活动性位于氢后。若两种金属均与稀盐酸或稀硫酸反应,则产生气体速率快的金属活动性强。
(3)利用金属与盐溶液反应(K、Ca、Na除外):若金属能将盐溶液中的金属置换出来,则该金属的活动性强于被置换出来的金属;若不能置换则该金属活动性弱于组成该盐的金属。
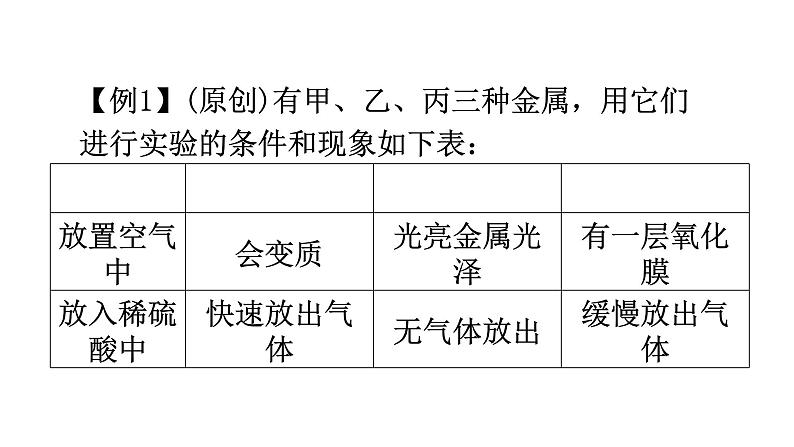
【例1】(原创)有甲、乙、丙三种金属,用它们进行实验的条件和现象如下表:
(1)根据以上信息,这三种金属活动性由强到弱的顺序是________(填字母)。A. 甲、乙、丙B. 甲、丙、乙C. 乙、丙、甲D. 丙、乙、甲(2)根据以上信息判断下列反应能否发生。(填“能”或“否”)①金属甲放入乙的盐溶液中:______;②金属乙放入丙的盐溶液中:________。
【举一反三】1. (2021湖北)通过下列三个实验,探究X、Y、Z三种金属的活动性顺序:X+HCl——不反应Y+H2SO4====YSO4+H2↑Z+X(NO3)2——不反应 则X、Y和Z的金属活动性由强到弱和(H)的位置顺序正确的是( )A. Y(H)、X、Z B. Y(H)、Z、X C. Y、X(H)、Z D. Y、Z(H)、X
2. 已知金属R和Fe、H活动性强弱关系为Fe>R>H,下列说法正确的是( )A. 金属R放入Zn(NO3)2溶液中,有Zn析出B. 金属R放入CuSO4溶液中,金属表面有紫红色固体析出C. 金属Fe(足量)放入R(NO3)2溶液中,溶液变黄色D. 金属铁放入AgNO3溶液中,一段时间后溶液质量变大
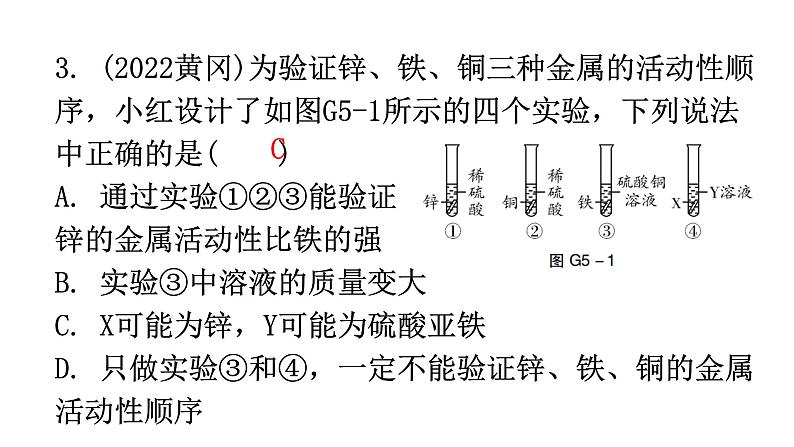
3. (2022黄冈)为验证锌、铁、铜三种金属的活动性顺序,小红设计了如图G5-1所示的四个实验,下列说法中正确的是( )A. 通过实验①②③能验证锌的金属活动性比铁的强B. 实验③中溶液的质量变大C. X可能为锌,Y可能为硫酸亚铁D. 只做实验③和④,一定不能验证锌、铁、铜的金属活动性顺序
(2)等质量的金属与足量酸反应,金属的价量比越大,产生的H2越多(如图G5-2丙、丁)。甲乙丙丁
【例2】下列图像中有关量的变化趋势与对应关系不正确的是( )A. 分别向足量的等质量的Fe、Zn中加入等质量、等浓度的稀盐酸B. 分别向等质量的Fe、Zn中加入足量的等质量、等浓度的稀盐酸C. 分别向等质量的Fe、Zn中不断加入等质量、等浓度的稀盐酸D. 分别向等质量、等浓度的稀盐酸中不断加入等质量的Fe、Zn
【举一反三】4. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图G5-3所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )A. 完全反应所需时间:丙>甲>乙B. 生成氢气的质量:甲>乙>丙C. 相对原子质量:乙>丙>甲D. 消耗硫酸的质量:甲>乙>丙
5. 质量相等的镁和铝分别和等浓度、等质量的稀盐酸反应,依据图G5-4判断下列叙述中正确的是( )A. 金属均反应完,一定有盐酸剩余B. 反应结束后,参加反应的镁和铝的质量比为4∶3C. 盐酸均反应完,一定有镁剩余D. 图中X、Y分别表示铝、镁的反应情况
类型三:金属与盐溶液反应后滤液、滤渣的成分分析方法指导 此类题目多涉及溶液中存在多个反应,解题时应遵循越远越优先反应原则,即在金属活动性顺序中两种金属活动性相差越大反应越先进行。可简单总结为:①滤液中一定存在活动性最强的金属的离子;②滤渣中一定存在活动性最弱的金属的单质。
【例3】(1)将过量Zn粉加入Cu(NO3)2溶液中,充分反应后过滤。观察到的现象是___________________________________________;滤渣的成分是________。滤液的成分是____________。(2)将过量Zn粉加入AgNO3和Cu(NO3)2的混合溶液中,充分反应后过滤。先发生的是Zn与________的反应,滤渣的成分是________________。
(3)将Zn粉加入AgNO3和Cu(NO3)2的混合溶液中,充分反应后若溶液为蓝色,则滤液中一定含有的是__________________________,可能含有的是______________。
Zn(NO3)2、Cu(NO3)2
【举一反三】6. (2021衡阳)向盛有Cu(NO3)2溶液的烧杯中加入一定量Zn粉和Ag粉的混合物,充分反应后过滤,得到滤渣和滤液。下列判断正确的是( )A. 滤渣中一定不含Zn,一定含Cu和AgB. 滤渣中一定不含Zn和Cu,一定含AgC. 滤液中一定含Zn(NO3)2,一定不含AgNO3D. 滤液中一定含Zn(NO3)2和Cu(NO3)2,可能含AgNO3
7. (2022邵阳)在硝酸铜、硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤。下列说法正确的是( )A. 若滤液为无色,则滤渣中一定有银和锌,可能有铜B. 若滤液为蓝色,则滤液中一定有Cu2+、Zn2+,可能有Ag+C. 若往滤渣中加入稀盐酸有气泡产生,则滤液中一定有Zn2+、Ag+,可能有Cu2+D. 若往滤液中加入稀盐酸有白色沉淀产生,则滤渣中一定有银和铜,可能有锌
8. (2022达州)处理某废旧金属后的溶液中含有Cu(NO3)2和AgNO3两种溶质,为回收其中的金属,向该溶液中加入一定量的铁粉,充分反应后过滤,再向滤渣中加入稀盐酸,无气泡产生。则滤液中一定含有的金属离子是________;滤渣中可能含有________。
类型四:金属与盐溶液反应图像方法指导金属1+盐1→金属2+盐2。(1)在盐1和盐2中金属化合价相同的情况下,若金属1的相对原子质量大于金属2,则反应后的金属质量减小(如图G5-5甲),盐溶液的质量增大(如图G5-5乙)。
(2)在盐1和盐2中金属化合价相同的情况下,若金属1的相对原子质量小于金属2,则反应后的金属质量增大(如图G5-5丙),盐溶液的质量减小(如图G5-5丁)。
【例4】向一定质量FeCl2和CuCl2的混合溶液中逐渐加入足量的锌粒,下列图像不能正确反映对应关系的是( )
【举一反三】9. 向一定量的AgNO3和Cu(NO3)2的混合溶液中加入Zn粉,所得溶液的质量与加入Zn粉质量关系如图G5-6所示,下列说法正确的是( )A. a点溶液中的溶质有2种 B. 取c点的固体,加入稀盐酸,有气泡产生 C. d点溶液中溶质为Zn(NO3)2D. 若取bc段溶液,滴加稀盐酸,有白色沉淀
相关课件
这是一份中考化学复习高频考点集中练10实验创新课件,共27页。PPT课件主要包含了长颈漏斗,分液漏斗,可以控制反应的速率,紫色石蕊溶液变红,操作简便节约药品等,①②③,℃的热水,试管内进入水的体积,铁要与氧气接触,水蒸气和氧气等内容,欢迎下载使用。
这是一份中考化学复习高频考点集中练9复分解反应的应用课件,共15页。PPT课件主要包含了有白色沉淀产生等内容,欢迎下载使用。
这是一份中考化学复习高频考点集中练8粗盐的提纯课件,共20页。PPT课件主要包含了较多量晶体,托盘天平,蒸发皿中出现较多固体,Na2CO3,把杂质除尽,HCl等内容,欢迎下载使用。










