




高中化学人教版 (2019)必修 第一册第二节 离子反应教学课件ppt
展开三国时期,诸葛亮在七擒孟获的过程中,蜀军由于误饮哑泉水、个个不能言语,生命危在旦夕。幸得巧遇老叟,指点迷津——饮用万安溪安乐泉水可解毒。终于转危为安,渡过难关。 哑泉水为何能致哑,万安溪安乐泉水又是什么灵丹妙药呢?
第2课时 离子反应及其表示法
通过实验事实认识离子反应及其发生的条件。 能正确书写离子方程式并能进行正误判断。
理解离子方程式的意义。
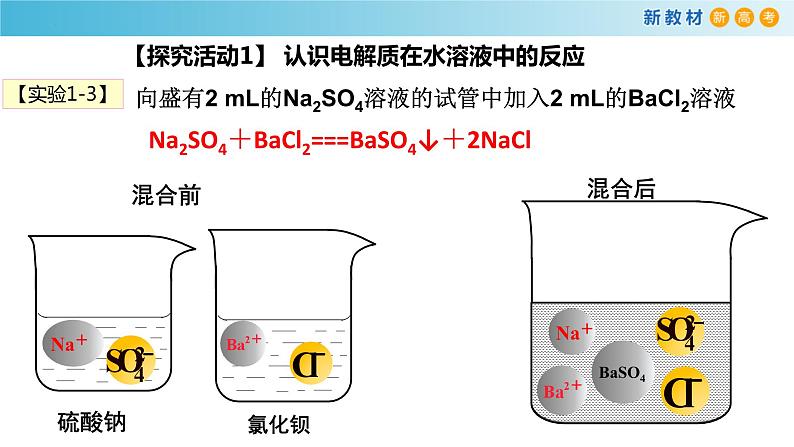
【探究活动1】 认识电解质在水溶液中的反应
向盛有2 mL的Na2SO4溶液的试管中加入2 mL的BaCl2溶液
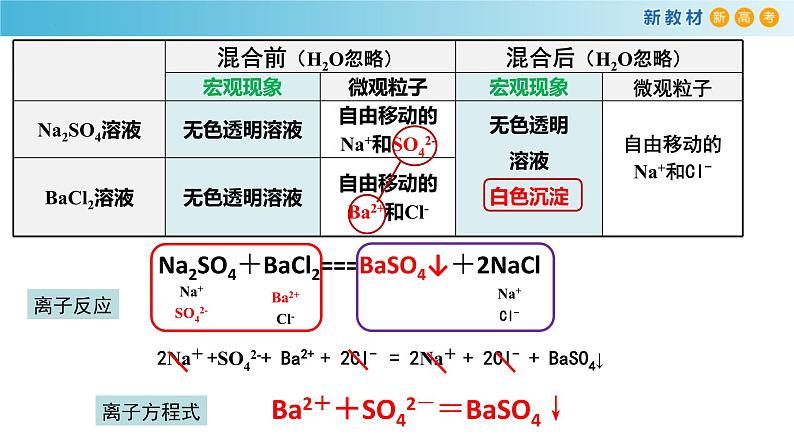
Na2SO4+BaCl2===BaSO4↓+2NaCl
Ba2+ + SO42- = BaSO4 ↓
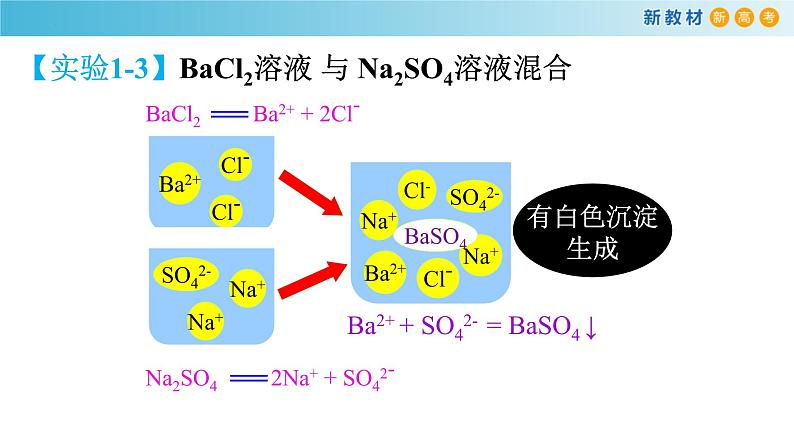
【实验1-3】BaCl2溶液 与 Na2SO4溶液混合
Ba2++SO42-=BaSO4↓
Na+SO42-
2Na+ +SO42-+ Ba2+ + 2Cl- = 2Na+ + 2Cl- + BaSO4↓
1.概念: 电解质在溶液中的反应实质上是离子之间的反应,这样的反应属于离子反应(在溶液中,有离子参加或生成的反应)。
用实际参加反应的离子符号来表示离子反应的式子。
分析溶液中存在的微粒
确定参与反应的微粒及数量
写出实际参加反应的微粒
二. 离子方程式的书写
写出Na2CO3与CaCl2溶液反应的离子方程式。
Ca2++CO32-=CaCO3↓
“哑泉致哑”、 “安乐泉解毒”
1995年10月国内某报刊报道,经科研人员研究,“哑泉”水中溶有CuSO4,“安乐泉”水质偏碱性。
用离子方程式解释解毒的原因。
Cu2++2OH-=Cu(OH)2↓
根据客观事实写出反应的化学方程式
把易溶于水且易电离的物质拆成离子形式,反应物和生成物中的弱酸、弱碱、水、不溶的物质和气体全部写化学式、单质、氧化物也均写化学式。
离子方程式的书写步骤:
(以硫酸钠与氯化钡反应为例)
可拆成离子形式的物质:
强酸:HCl、HNO3、H2SO4强碱:NaOH、KOH、Ba(OH)2可溶性盐:钾盐、钠盐、铵盐、硝酸盐及其它
CaCO3、BaSO4、Cu(OH)2等
CO2、H2S、SO2等
Na2O、 Na2O2 、Fe2O3等
不可拆成离子形式的物质:
删去方程式两边不参加反应的离子,将系数化成最简整数比
检查离子方程式两边元素的原子个数和电荷数是否相等。
Na2CO3 + 2HCl 2NaCl + CO2↑ + H2O
2Na+ + CO32- + 2H+ + 2Cl- 2Na+ + 2Cl- + CO2↑ + H2O
CO32- + 2H+ == CO2↑ + H2O
1、 写出碳酸钠与稀盐酸反应的离子方程式
根据以上书写步骤,请同学们交流讨论填写下表:
有的离子方程式可能出现某一侧所有物质均不能拆分的情况,例如③中所有生成物均不能拆分。
2HCO3- + 2H+ = 2H2O + 2CO2↑
一定要将方程式的系数化到最简
观察下面的方程式,化学方程式和离子方程式的意义有何不同?
四个不同的强酸强碱之间的中和反应,化学方程式不同
实质都是溶液中的H+和OH-的反应,离子方程式相同
【探究活动2】 离子方程式表示意义
化学方程式表示的是某一个特定的化学反应,而离子方程式能表示同一类化学反应。
表示某个具体的化学反应
表示同一类型的离子反应
H+ + OH- = H2O
表示强酸和强碱反应生成可溶性盐和水的中和反应。
Ba2+ + 2OH- + 2H+ + SO42- = BaSO4↓ + 2H2O
思考:可以表示H2SO4与Ba(OH)2反应吗?
4.(1)表示可溶性钙盐和可溶性碳酸盐反应的离子方程式为: 。 (2)离子反应Ba2+ + SO42- = BaSO4↓表示的可能是哪类反应?
Ca2+ + CO32- = CaCO3↓
可溶性硫酸盐和可溶性钡盐的反应、硫酸和可溶性钡盐的反应
练习:将下面的化学方程式改为离子方程式:(1)SO2 + Cl2 + 2H2O = H2SO4 + 2HCl(2)3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ + 4H2O
SO2 + Cl2 + 2H2O = 2H+ + SO42- + 2Cl- + 2H+
同一侧的相同离子要合并,例如反应(1)中的H+。
3Cu + 8H+ + 8NO3- = 3Cu2+ + 6NO3- + 2NO↑ + 4H2O
SO2 + Cl2 + 2H2O = 4H+ + SO42- + 2Cl-
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O
删去方程式两边的相同离子的时候,可能出现两边系数不同,只能删去一部分的情况,例如反应(2)中的NO3-
书写离子方程式应注意的问题
1、凡是不在溶液中进行的反应一般不能写离子方程式,如:NH4Cl固体与Ca(OH)2固体混合加热,只能写化学方程式。
1.表述为“澄清石灰水”、“饱和石灰水”、“Ca(OH)2溶液”时,可以拆;2.表述为“石灰乳”、“石灰浆”时不可以拆。
2、对于微溶物的处理:
①在反应物里:溶液状态(稀溶液),写离子形式; 在反应物里:浊液(如石灰乳),写化学式。 ②在生成物里:微溶物用化学式。
如:写出下列反应的离子方程式(1)CO2通入足量的澄清石灰水 CO2通入石灰乳(2)向NaOH浓溶液中滴加CaCl2溶液
CO2+Ca2++2OH- =CaCO3↓+H2O
Ca2++2OH- =Ca(OH)2↓
CO2+Ca(OH)2=CaCO3↓+H2O
Ca(OH)2、CaSO4、Ag2SO4、MgCO3
3、弱酸的酸式盐的酸根离子(HCO3- )不能拆开写, 强酸的酸根离子(HSO4- )要拆开
HCO3- + H+ = CO2↑+ H2O
H++ OH- =H2O
②NaHSO4溶液和NaOH溶液反应:
NaHCO3与氢氧化钠反应:
HCO3- +OH- =H2O+CO32-
如:①NaHCO3溶液和稀盐酸反应:
3.写出与下列离子方程式相对应的化学方程式:
(2) CO32- + 2H+ = H2O + CO2
(1) Cu2++ 2OH- =Cu(OH)2
强酸(硫酸,盐酸,硝酸等)
可溶性强碱(NaOH,KOH等)
强酸盐(硫酸盐,氯化物,硝酸盐)
练习:根据以上书写步骤,写出下列离子方程式
(1)CuO溶于稀硫酸中(2)KOH溶液与稀硫酸混合(3)氨水与稀盐酸混合(4)石灰水中充入少量CO2(5)石灰水中充入过量CO2(6)Na2CO3溶液与石灰水混合(7)CH3COONa溶液与稀盐酸混合(8)Zn与CuSO4溶液反应
人教版 (2019)必修 第一册第一节 钠及其化合物教学ppt课件: 这是一份人教版 (2019)必修 第一册第一节 钠及其化合物教学ppt课件,共20页。PPT课件主要包含了学习目标,砖红色,洋红色,紫红色,黄绿色等内容,欢迎下载使用。
人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt: 这是一份人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt,共25页。PPT课件主要包含了学习目标,课堂小结等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 离子反应教学ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 离子反应教学ppt课件,共24页。PPT课件主要包含了学习目标,活动一,活动二,离子共存的审题思路,一看颜色,二看酸碱性,三看反应等内容,欢迎下载使用。













