
广东省佛山市顺德华侨中学2023-2024学年高三上学期第一次月考化学试题
展开顺德区华侨中学2023学年高三年级8月月考
化学试卷
本试卷共20小题,满分100分。考试用时75分钟。
可用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Ca 40 Fe 56
一、单选题:(本题共有16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。每小题只有一个选项符合题意)
1. 今年假期,人文考古游持续成为热点。很多珍贵文物都记载着中华文明的灿烂成就,具有深邃的文化寓意和极高的学术价值。下列国宝级文物主要由合金材料制成的是( )
选项 | A | B | C | D |
文物 | ||||
名称 | 铸客大铜鼎 | 河姆渡出土陶灶 | 兽首玛瑙杯 | 角形玉杯 |
2.《石雅》云:“青金石色相如天,或复金屑散乱,光辉灿烂,若众星丽于天也。”青金石中主要矿物的化学组成可表示为(Na,Ca)8(AlSiO4)6(SO4,Cl,S)2,故其可看作由Na2SO4、Na2S、NaCl、CaCl2、CaSO4、Al2O3和SiO2等组成。下列说法正确的是( )
A.Al2O3和SiO2均既能与强酸反应,又能与强碱反应
B.Na2SO4、NaCl和Na2S的焰色都呈黄色
C.用AgNO3溶液可区分Na2SO4溶液和CaCl2溶液
D.以惰性材料为电极电解NaCl水溶液可制得金属钠
3.北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是( )
A.胆矾的化学式为CuSO4
B.胆矾可作为湿法冶铜的原料
C.“熬之则成胆矾”是浓缩结晶过程
D.“熬胆矾铁釜,久之亦化为铜”是发生了置换反应
4.下列生活应用或生产活动中物质的性质与用途具有对应关系的是( )
A.CaO易与水反应,可用作食品干燥剂
B.能使蛋白质变性,可用于制作颜料
C.Na有导电性,可用作快中子反应堆的热交换剂
D.具有氧化性,可用于漂白纸张
5. 下列说法正确的是( )
A.镀锌铁破损后,铁易被腐蚀
B.红酒中添加适量SO2可以起到杀菌和抗氧化的作用
C.牙膏中添加氟化物可用于预防龋齿,原因是氟化物具有氧化性
D.自来水厂常用明矾、O3、ClO2等作水处理剂,其作用都是杀菌消毒
6.物质的化学性质在日常生活和生产中有着广泛的运用。下列有关说法正确的是( )
A.O3是一种氧化性极强的气体,可用作餐具的消毒剂
B.常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸
C.工业上通过电解六水合氯化镁制取金属镁
D.FeCl3可以作止血剂是因为Fe3+具有强氧化性
7. 下列说法不正确的是( )
A.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
8.下列物质与其俗名匹配且相关叙述合理的是( )
A.双氧水:过氧化氢,受热稳定、易溶于水
B.铁红:氧化亚铁,可用作红色油漆的颜料
C.磁性氧化铁:四氧化三铁,为黑色晶体
D.苏打:碳酸氢钠,可用于治疗胃酸
9.根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向淀粉溶液中加适量20%H2SO4溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
B | 室温下,向HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
C | 室温下,向浓度均为的BaCl2和CaCl2混合溶液中加入足量Na2CO3溶液,出现白色沉淀 | 白色沉淀是BaCO3 |
D | 向H2O2溶液中滴加KMnO4溶液,溶液褪色 | H2O2具有氧化性 |
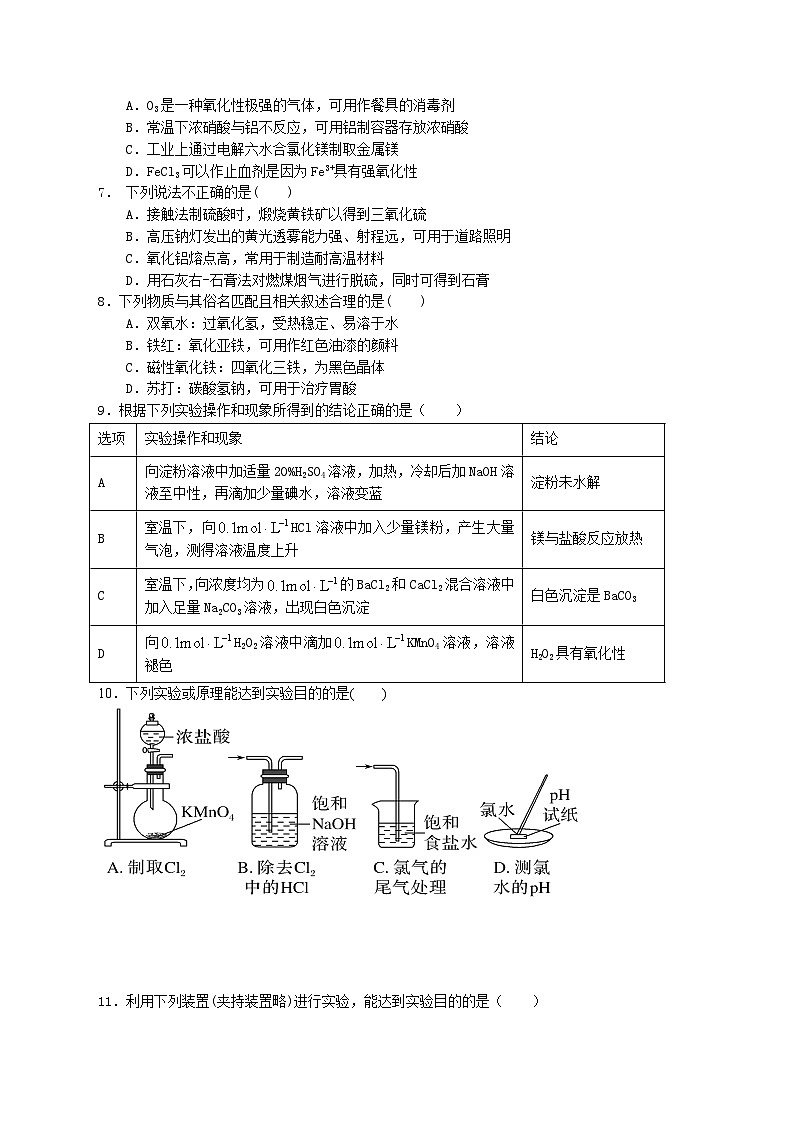
10.下列实验或原理能达到实验目的的是( )
11.利用下列装置(夹持装置略)进行实验,能达到实验目的的是( )
A.用甲装置制备并收集CO2
B.用乙装置制备溴苯并验证有HBr产生
C.用丙装置制备无水MgCl2
D.用丁装置在铁上镀铜
12. 宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( )
A. Na2O2放入水中:Na2O2 + H2O = 2NaOH + O2↑
B. H2O(g)通过灼热铁粉:3H2O + 2Fe = Fe2O3 + 3H2
C. 铜丝插入热的浓硫酸中:Cu + H2SO4 = CuSO4 + H2↑
D. SO2通入酸性KMnO4溶液中:5SO2 + 2H2O + 2MnO- 4 = 5SO2- 4+ 4H+ + 2Mn2+
13. 明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是( )
A. FeSO4的分解产物X为FeO B. 本流程涉及复分解反应
C. HNO3的沸点比H2SO4的低 D. 制备使用的铁锅易损坏
14. 室温下,下列实验探究方案不能达到探究目的的是 ( )
选项 | 探究方案 | 探究目的 |
A | 向盛有溶液的试管中滴加几滴溶液,振荡,再滴加几滴新制氯水,观察溶液颜色变化 | 具有还原性 |
B | 向盛有水溶液的试管中滴加几滴品红溶液,振荡,加热试管,观察溶液颜色变化 | 具有漂白性 |
C | 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | 的氧化性比的强 |
D | 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 | 是弱电解质 |
15.以黄铁矿(主要成分为FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染,其中一种流程如图所示。下列说法错误的是( )
A.黄铁矿中的FeS2在煅烧过程中作还原剂
B.欲得到更纯的NaHSO3,反应①应通入过量的SO2气体
C.还原铁粉用盐酸溶解后,可用KMnO4溶液滴定法来测定其纯度
D.加热NaHSO3制备Na2S2O5的化学方程式为2NaHSO3Na2S2O5+H2O
16. 如图为某实验测得溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正确的是( )
A. a点溶液的比c点溶液的小
B. a点时,
C. b点溶液中,
D. ab段,pH减小说明升温抑制了的水解
二、填空题(本题包括4个小题,共56分)
17.(16分)某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下。向硝酸酸化的0.05 mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取少量黑色固体,洗涤后,_______ (填操作和现象),证明黑色固体中含有Ag。
②取上层清液,滴加K3[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液中含有_________。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是___________________ (用离子方程式表示)。针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生(资料:Ag+与SCN-生成白色沉淀AgSCN),且溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号 | 取样时间/min | 现象 |
ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
ⅱ | 30 | 产生白色沉淀;较3 min时量少;溶液红色较3 min时加深 |
ⅲ | 120 | 产生白色沉淀;较30 min时量少;溶液红色较30 min时变浅 |
② 对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于________ (用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据_______ 现象,判断溶液中存在Ag+,可产生Fe3+。
③ 下列实验可证实假设a、b、c不是产生Fe3+的原因。
向硝酸酸化的________ 溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3 min时溶液呈浅红色,30 min后溶液几乎无色。
(3)根据实验现象,写出产生Fe3+的反应离子方程式______ 。
18. (14分)硫铁化合物(、等)应用广泛
(1)纳米可去除水中微量六价铬。在的水溶液中,纳米颗粒表面带正电荷,主要以、、等形式存在,纳米去除水中主要经过“吸附→反应→沉淀”的过程。
已知:Ksp(FeS)=6.5×10-18 Ksp[Fe(OH)2]=5.0×10-17
电离常数分别为 Ka1=1.1×10-7、Ka2=1.3×10-13
①写出基态Cr原子的价电子排布式 。
②在弱碱性溶液中,与反应生成、和单质S,其离子方程式为_______。
③在弱酸性溶液中,反应的平衡常数K的数值为_______ 。
④在溶液中,pH越大,去除水中的速率越慢,原因是_______ 。
(2)具有良好半导体性能。的一种晶体与晶体的结构相似,该晶体的一个晶胞中的数目为_______,在晶体中,每个S原子与三个紧邻,且间距相等,如图给出了晶胞中的和位于晶胞体心的(中的键位于晶胞体对角线上,晶胞中的其他已省略)。在下图中用“-”将其中一个S原子与紧邻的连接起来。
(3)、在空气中易被氧化,将在空气中氧化,测得氧化过程中剩余固体的质量与起始的质量的比值随温度变化的曲线如图所示。时,氧化成含有两种元素的固体产物为_______(填化学式)。
19.(12分)用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下:
已知:MnO2是一种两性氧化物;25 ℃时相关物质的Ksp见下表。
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
回答下列问题:
(1)Mn在周期表中的位置是:
(2)保持BaS投料量不变,随MnO2与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是________________________ 。
(3)滤液Ⅰ可循环使用,应当将其导入到________ 操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为________(填化学式),再使用氨水调溶液的pH,则pH的理论最小值为___________(当溶液中某离子浓度c≤1.0×10-5 mol·L-1时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为_____________________________________。
20.(16分)化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许______离子通过,氯气的逸出口是_______(填标号)。
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数
δ[δ(X)=,X为HClO或ClO−]与pH的关系如图(b)所示。
HClO的电离常数Ka值为______。
(3) Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为
歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为_____
_ 。
(4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为_____mol;产生“气泡”的化学方程式为____________ 。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是______
(用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000 kg该溶液需消耗氯气的质量为____ kg(保留整数)。
顺德区华侨中学2023学年高三年级8月月考
化学答案
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
A | B | A | A | B | A | A | C |
9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
B | A | C | D | A | D | C | A |
17.(14分)【答案】
(1)①加硝酸加热溶解固体,再滴加稀盐酸,产生白色沉淀。(或者加入足量稀盐酸(或稀硫酸),固体未完全溶解)。(2分) ②Fe2+(2分)
(2)Fe+2Fe3+=3Fe2+ 。(2分) ②4Fe2++O2+4H+=4Fe3++2H2O (2分)、白色沉淀(2分)
③0.05 mol·L-1 NaNO3溶液 (2分)
(3)Ag++Fe2+=Ag+Fe3+,(2分)
18.(14分)【答案】
(1) ①.3d54s1(2分) ②. (2分)
③. 5 (2分) ④. c(OH-)越大,表面吸附的的量越少 (2分)
(2) 4 (2分) (2分)
(3)Fe2O3(2分);设氧化成含有两种元素的固体产物化学式为FeOx,,则,则56+16x=80.04,x= ,即固体产物为Fe2O3
19.(12分)【答案】:
(1)第四周期ⅦB族(2分)
(2)过量的MnO2消耗了产生的Ba(OH)2(2分)
(3)蒸发(2分)
(4)H2O2(2分) 4.9(2分)
(5)Mn2++HCO+NH3·H2O===MnCO3↓+NH+H2O(2分)
20.(16分)【答案】
(1)Na+(2分) a(2分)
(2)10-7.5 (2分)
(3)2Cl2+HgO=HgCl2+Cl2O(2分)
(4)1.25(2分) NaHCO3+NaHSO4=CO2↑+Na2SO4+H2O(2分)
(5)ClO-+Cl-+2H+=Cl2↑+ H2O (2分) 203(2分)
广东省佛山市顺德区勒流中学、均安中学、龙江中学等十五校2023-2024学年高二上学期12月联考化学试题: 这是一份广东省佛山市顺德区勒流中学、均安中学、龙江中学等十五校2023-2024学年高二上学期12月联考化学试题,共10页。试卷主要包含了本试卷主要考试内容,可能用到的相对原子质量,下列有关活化分子的说法正确的是,下列与盐类水解有关的是,下列说法正确的是等内容,欢迎下载使用。
广东省佛山市顺德区郑裕彤中学2023-2024学年上学期高一10月月考化学试题(无答案): 这是一份广东省佛山市顺德区郑裕彤中学2023-2024学年上学期高一10月月考化学试题(无答案),共8页。试卷主要包含了8倍,则下列叙述正确的是,100等内容,欢迎下载使用。
广东省佛山市顺德区乐从中学2023-2024学年高一上学期10月月考化学试题: 这是一份广东省佛山市顺德区乐从中学2023-2024学年高一上学期10月月考化学试题,共8页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。












