




高中化学鲁科版 (2019)选择性必修3第2节 有机化合物结构的测定课文课件ppt
展开教学目的: 1. 掌握确定有机物元素组成和相对分子质量、实验式的方法。 2.了解不饱和度的概念,理解不饱和度在有机物结构确定中的作用。 3.掌握常见官能团的确定方法。 4.能通过计算和实验分析确定有机物的结构式或结构简式。 学习重点、难点: 掌握确定有机物结构简式的步骤和方法
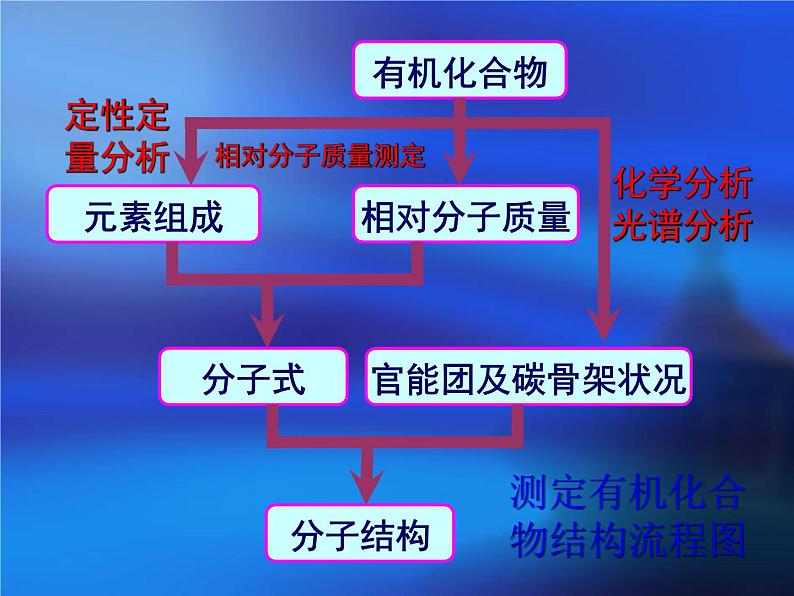
测定有机化合物结构流程图
一、怎样确定有机化合物的分子式?
(1)确定有机化合物的 ;
(2)测定有机化合物的 。
元素组成及各元素质量分数
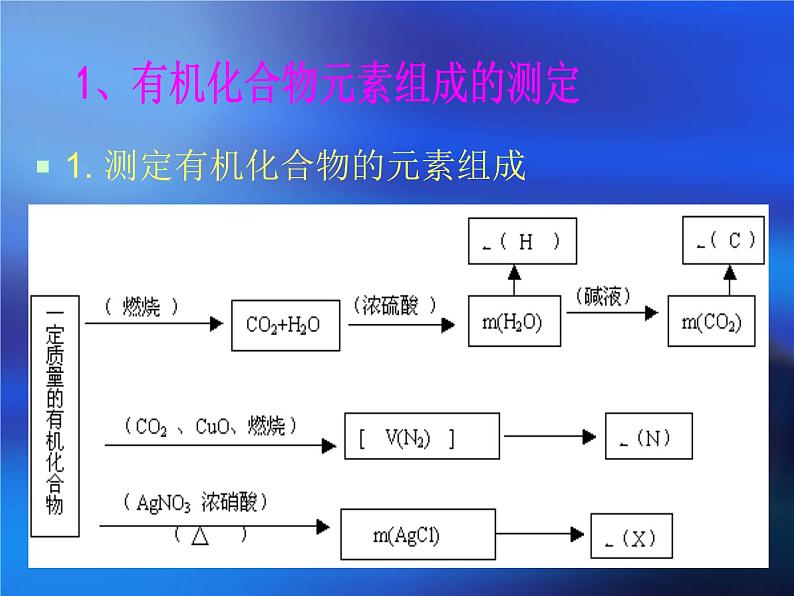
1. 测定有机化合物的元素组成
1、有机化合物元素组成的测定
2. 测定有机化合物的相对分子质量的方法 (1)依据气体的密度(标准状况):Mr=22.4×d (2)依据气体的相对密度(D):Mr=DA ×MA (3)依据理想气体状态方程:PV=nRT Mr=mRT/(PV) (4)气体的平均相对分子质量:=m总/n总 (5) 质谱法 根据有机化合物的质谱图,可看出有机化合物分子失去一个电子成为带正电荷的离子的质量大小,其中最大的离子质量就是有机化合物的相对分子质量。
3、求出有机化合物的实验式 由各元素的的质量分数,除以各自的相对原子质量,所得数值相比可求出各元素原子的个数比,即得最简式,又叫实验式。 实验式(最简式)和分子式的区别与联系 (1)最简式是表示化合物分子所含各元素的原子数目最简单整数比的式子。不能确切表明分子中的原子个数。 (2)分子式=(最简式)n,n值的求法需借助有机物的相对分子质量,由相对分子质量除以最简式的式量,即求出n值,也就求出了分子式。
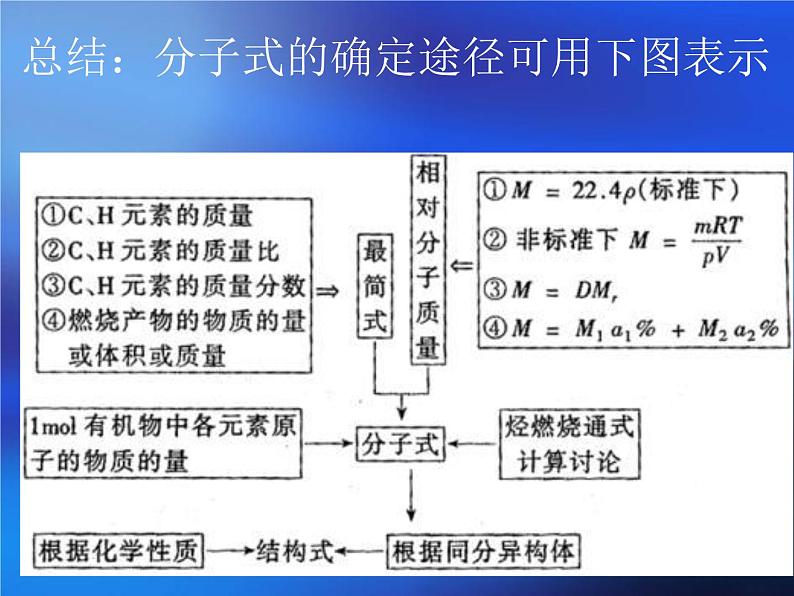
总结:分子式的确定途径可用下图表示
例1、燃烧某有机物A 1.50g,生成1.12LCO2(标准状况)和0.05mlH2O 。又测得A的相对分子质量是30,求该有机物的分子式。
二、怎样确定有机化合物的结构式?
根据 和 以及 可以确定有机物的结构式。
测定有机物的结构,关键步骤是判定有机物的不饱和度及其典型化学性质,进而确定有机物所含的官能团及其所处的位置。
二、有机化合物结构式的确定
1、有机化合物分子不饱和度的计算
烷烃分子的通式为CnH2n+2,分子中每减少2个碳氢键,同时必然会增加一个碳碳键,该碳碳键可能是重键(双键或叁键),也可能连接成环状,这些都称为增加了一个不饱和度,又叫缺氢指数,用字母 表示。
∴不饱和度可以为测定分子结构提供是否含双键、三键或碳环等信息
(1)几种常见官能团的不饱和度?(2)若只有C和H两种元素,总结不饱和度的计算公式?(3)若有机物中有X O N原子如何处理?
体会不饱和度的定义,思考下列问题:
有机化合物分子不饱和度的计算
分子的不饱和度=n(C)+1-n(H)/2
2、在计算不饱和度时,应注意:
若含有O(氧原子),可不予————;
若含有N(氮原子),就在氢原子总数中减去————。
1、式中各字母表示什么意义?
若有机物中含有X(卤素原子),可将其视为—————;
6+1-(5-1)/2=5
例如,分子式为C6H5NO2的分子的不饱和度为:
练习:求下列有机化合物的不饱和度。
(2)CH2=CH-CH=CH2
(4) 溴苯 C6H5Br
(3)乙醇 CH3CH2OH
官能团决定了有机物的 性质。 通过有机物的化学反应,可以推断有机物 可能具有的 。
2、确定有机化合物的官能团
请大家阅读教材P111表3-2-2 : 一些常见的官能团的检验方法
一些常见的官能团的化学检验方法
AgNO3和浓HNO3
新制Cu(OH)2悬浊液
(NH4)2Fe(SO4)2、H2SO4以及KOH的甲醇溶液
2、有机化合物结构式的确定
1、有机化合物分子式的确定
(1)有机化合物分子不饱和度的计算
(2)确定有机化合物的官能团
例1、某有机物样品3.26g,燃烧后得到4.74gCO2和 1.92gH2O,实验测得其相对分子质量为60,求该有机物的分子式。
解一:先求样品中各组成元素的质量,组成元素的物质的量之比求分子式。 由上述计算知:m(C)=1.29g, m(H)=0.213g m(O)=3.26g-1.29g-0.213g=1.75g n(C)∶n(H)∶n(O)=2∶4∶2 该有机物分子式为C2H4O2。
解二:根据燃烧反应方程式计算 CxHyOz+ →xCO2+ H2O 60 44x ×18=9y 3.26g 4.74g 1.92g 60∶44x=3.26g∶4.74g x=2 60∶9y= 3.26g∶1.92g y=4 z=(60-12×2-1×4)÷16=2 分子式为C2H4O2
例2. 由一种气态烷烃与一种气态烯烃组成的混合气,对氦气的相对密度是6,将1体积此混合气与4体积氧气混合,装入密闭容器中,用电火花点燃,使之充分燃烧。若反应前后均保持120℃,测得容器内压强比反应前增加了4%。求混合气体中烷烃与烯烃的分子式及各自的体积分数。
解析:(混)=6×4=24,Mr<24的烃只有CH4,设烯烃的分子式为CnH2n,体积为x。 CnH2n+1.5nO2 ——n CO2+nH2O(g) V 1 1.5n n n 0.5n-1 x 5×4% (0.5n-1)x= 5×4% 14nx+16(1-x)=24 解得: n= 4 x=0.2 (CH4)=80% (C4H8)=20%
高中化学鲁科版 (2019)选择性必修3第1节 认识有机化学教课内容课件ppt: 这是一份高中化学鲁科版 (2019)选择性必修3第1节 认识有机化学教课内容课件ppt,共29页。PPT课件主要包含了绝大多数含碳的化合物,有机化学的发展,有机物的分类,按组成元素分,按碳的骨架分类,脂肪烃,练习按碳的骨架分类,按官能团分类,CH3CH3,官能团不同等内容,欢迎下载使用。
高中化学鲁科版 (2019)必修 第一册第2节 硫的转化课文配套课件ppt: 这是一份高中化学鲁科版 (2019)必修 第一册第2节 硫的转化课文配套课件ppt,共60页。PPT课件主要包含了认识硫单质,硫单质的物理性质,硫的同素异形体,硫与非金属的反应,酸雨及其防治,酸雨成因,酸雨的形成等内容,欢迎下载使用。
高中化学人教版 (新课标)选修3 物质结构与性质第二节 原子结构与元素的性质集体备课课件ppt: 这是一份高中化学人教版 (新课标)选修3 物质结构与性质第二节 原子结构与元素的性质集体备课课件ppt,共35页。PPT课件主要包含了知识回顾,想一想,s区元素,ns1,ns2,p区元素,d区元素,n-1d,ds区元素,f区元素等内容,欢迎下载使用。













