

2024成都外国语学校高二上学期9月月考试题化学含答案
展开成都外国语学校2023—2024学年度(上)9月月考
高二化学试卷
注意事项:
1、本试卷分Ⅰ卷(选择题)和Ⅱ卷(非选择题)两部分。
2、本堂考试75分钟,满分100分。
3、答题前,考生务必先将自己的姓名、学号填写在答卷上,并使用2B铅笔填涂。
4、考试结束后,将答题卡交回。
可能用到的相对原子质量:H-1 C- 12 N-14 O-16 Na-23 S-32
第Ⅰ卷(选择题,共42分)
1、化学与生活、环境密切相关,下列说法不正确的是
A.绿色化学的核心是从源头上减少和消除工业生产对环境的污染
B.人工固氮主要是通过控制条件将氮气转化为氮的化合物
C.人造纤维、合成纤维和光导纤维都是有机高分子化合物
D.石油的裂解和裂化、煤的干馏、煤的气化和煤的液化都是化学变化
2、下列化学用语表示正确的是
A.乙烯的结构简式:CH2CH2 B.的结构示意图:
C.甲烷分子的空间填充模型: D.氮分子的电子式:
3、下列物质的转化中,不能够一步实现的是
A. →NO B. S→ C. → D. →
4、设为阿伏加德罗常数的值。下列说法正确的是
A.100mL 18mol/L浓硫酸与足量Cu粉加热反应,产生的分子数为0.9
B.标准状况下,11.2L 中含有的原子数为2
C.一定条件下,1mol 与足量反应,产生的分子数为2
D.4.6g 与的混合气体中含有的原子数目为0.3
5、下列指定反应的离子方程式正确的是
A.与稀硫酸混合后溶液变浑浊:
B.NH4HCO3溶液与足量NaOH溶液反应:HCO+OH-=CO32-+H2O
C.Fe与稀硝酸反应:Fe+2H+=Fe2++H2↑
D.实验室制备氨气:NH4ClNH3↑+HCl↑
6、下列实验或装置能达到实验目的的是
A.若将甲中注射器的活塞往右拉,能自动恢复到原位,说明甲装置气密性好
B.将甲虚线框中的装置换为乙装置,滴入稀硫酸后若注射器活塞右移,说明锌与硫酸反应为放热反应
C.用丙装置加热硫酸铜溶液,蒸干溶液制备胆矾晶体
D.用装置丁制取并收集纯净的NO气体
7、下列说法正确的是
A.C(s,金刚石)=C(s,石墨) ,则金刚石比石墨稳定
B.乙醇的燃烧热为,则乙醇燃烧的热化学方程式可表示为:
C. , ;则小于
D.在一定条件下将1mol和0.5mol置于密闭容器中充分反应,放出热量79.2kJ,则反应的热化学方程式为
8、制备相关物质,涉及的反应原理及部分流程不合理的是
A.制溴:浓缩海水溶液
B.制取镁:海水溶液
C.加热分解冶炼
D.制碘:干海带浸出液碘水 → 含苯溶液 →单质碘
9、山梨酸是常用的食品防腐剂,其结构简式如图所示,下列有关山梨酸的叙述错误的是
A.该分子中含有四种官能团 B.既能发生取代反应,又能发生加成反
C.分子式为C7H10O5 D.与互为同分异构体
10、下列实验操作、现象和实验结论均正确的是
选项 | 实验操作和现象 | 结论 |
A | 除去甲烷气体中混有的乙烯气体 | 将混合气体通过酸性KMnO4溶液洗气 |
B | 蔗糖和稀硫酸混合加热,冷却后加入NaOH溶液调至碱性,再加入新制Cu(OH)2,加热,有砖红色沉淀产生 | 蔗糖已经水解 |
C | 向蛋白质溶液中加入适量CuSO4溶液并充分混合,溶液中有沉淀析出 | 可用CuSO4溶液分离、提纯蛋白质 |
D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,观察能否产生无色气体 |
A.A B.B C.C D.D
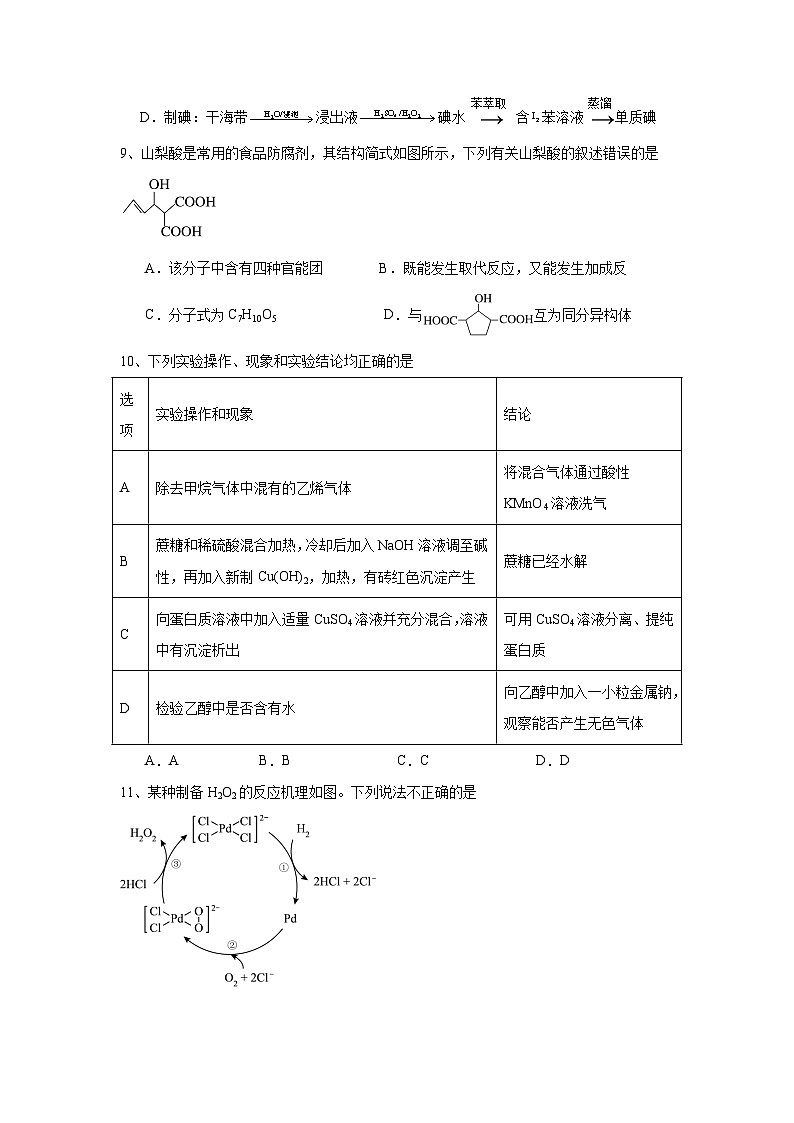
11、某种制备H2O2的反应机理如图。下列说法不正确的是
A.总反应可表示为H2+O2=H2O2 B.该反应历程中起到催化作用
C.HCl和Cl-可循环利用 D.①、②、③均为氧化还原反应
12、我国科学家合成了一种新型Au15/MoC材料,实现了低温催化水煤气变换。反应历程如图所示,其中吸附在催化剂表面的物种用“*”标注,TS指过渡态。下列有关说法不正确的是
A.新型Au15/MoC材料能实现低温催化水煤气变换主要原因是大幅度降低了活化能
B.如果换作铜系催化剂,题述反应的焓变会发生改变
C.该历程中制约反应速率的方程式为CO*+2H2O*→CO*+H2O*+OH*+H*
D.该过程有极性键的断裂和生成
13、将等物质的量的A、B混合于2L的恒容密闭容器中,发生反应:3A(g)+B(g)=xC(g)+2D(g),2min后测得c(D)=0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol/(L·min),下列说法正确的是
A.该反应方程式中,x=1 B.反应速率v(B)=0.25mol/(L·min)
C.2min时,A的物质的量为1.5mol D.2min时,A的转化率为60%
14、SO2可形成酸雨,是大气污染物。利用如图装置既可以吸收工厂排放的SO2又可以制得硫酸溶液。下列说法正确的是
A.电子的流动方向:a极→电解质溶液→b极
B.b极的电极反应式为O2+4e-+2H2O=4OH-
C.当电路中有2mol电子通过时,有4molH+透过质子交换膜进入右侧
D.该电池的总反应式为:2SO2+O2+2H2O=2H2SO4
第Ⅱ卷(非选择题,共58分)
15、对SO2、NOx、CO2和CO进行回收利用是节能减排的重要课题。
某温度下,向恒容密闭容器中充入NO2、SO2发生反应:NO2(g)+SO2(g)⇌SO3(g)+NO(g)。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是 (填序号)。
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是 (填字母)。
a.混合气体的密度保持不变 b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变 d.每生成1molSO3的同时消耗1molNO
(2)在体积为密闭容器中充入和,发生反应,测得、的物质的量随时间变化如图所示。
①反应到达3min时, (填“>”“<”或“=”)。
②0~5min内, 。
③反应达到平衡状态时,的体积分数为 %(保留1位小数)。
④a、b、c三点中代表达到平衡的是 ,a点的正反应速率 (填>、<或=)b点的逆反应速率
⑤“二甲醚(CH3OCH3)酸性燃料电池”的工作原理示意图如图所示。X电极为 (填“正”或“负”)极;该电极的电极反应式为: ,当消耗9.2g的二甲醚时,转移电子的数目为: 。
16、I.用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应反应热的测定。已知:实验中盐酸和氢氧化钠溶液的密度均为1g•cm-3,中和反应后溶液的比热容c=4.18J•g-1•℃-1)。
回答下列问题:
(1) b仪器名称______;不能用铜丝搅拌器代替b的理由是______。
(2)如果测量NaOH溶液温度后不把温度计上的碱用水冲洗干净,就直接测量盐酸的温度,则测得的ΔH______(填“偏大”、“偏小”或“无影响”)。
(3)若简易量热计不盖杯盖,则所测得中和反应反应热的绝对值______(填“偏大”、“偏小”或“无影响”)。
(4) 若四次平行操作测得终止温度与起始温度的温差(T2-T1)分别为①3.2℃、②4.3℃、③3.3℃、④3.4℃,则最终代入计算式的温差数据为______℃。已知反应过程中放出的热量Q可用公式Q=cmΔt计算,试计算该反应放出的热量______J(结果保留一位小数)。
II.化学反应伴随能量变化,获取反应能量变化有多条途径。回答下列问题:
(5)已知:
化学键 | C—H | C—C | C=C | H—H |
键能/(kJ·mol-1) | 412 | 348 | 612 | 436 |
则 +H2(g) ΔH= 。
(6)神舟系列火箭用偏二甲肼C2H8N2作燃料,N2O4作氧化剂,反应后产物无污染。
已知:反应1:N2(g)+2O2(g)=N2O4(g) △H=xkJ∙mol-1
反应2:C2H8N2(1)+4O2(g)=N2(g)+2CO2(g)+4H2O(g) △H2=ykJ∙mol-1
写出C2H8N2(1)和N2O4(g)反应生成N2(g)、CO2(g)、H2O(g)的热化学方程式: 。
17、硫酸的消耗量是衡量一个国家化学工业发展水平的标志。以黄铁矿(主要成分为)为原料生产和。
请回答下列问题:
(1)中铁元素的化合价为 ;试剂a为 。
(2)若要增大煅烧过程的反应速率,可采取的措施是 (任写一条即可)。
(3)煅烧时主要反应的化学方程式为 。
(4)“氧化”时,反应的化学方程式为 。
(5)可用于葡萄酒的抗氧化剂,用碘液可以测定葡萄酒中的含量。请配平其反应的化学方程式:
_____________________________________________
若要检验是否变质生成了,所用的试剂是 。
(6)在测定某葡萄酒中的含量时,取葡萄酒样品,消耗碘液。样品中的含量为 。
18、苯乙烯在一定条件下有如图转化关系,根据框图回答下列问题:
(1)苯乙烯中最多有 个原子共面,其与足量氢气在一定条件下充分反应生成的物质 的一氯代物有 种(不考虑立体异构)。
(2)物质B的官能团名称是 ,A→B的反应类型为 反应,A+C→D的化学方程式为: 。
(3)生成高聚物E的化学方程式为: 。
(4)物质C与甲醇的酯化产物分子式为 。该酯化产物的同分异构体中,满足以下情况的共有 种(不考虑立体异构)。
①含苯环且苯环上只有两个取代基;②能与NaHCO3溶液反应生成CO2。
成都外国语学校2023—2024学年度(上)9月月考
高二化学参考答案
1-5、CCBDA 6-10、ACBAB 11-14、DBCD
15、(1) a bd (2)> 0.5 17.9 c > 负 CH3OCH3-12e-+3H2O=2CO2+12H+ 2.4NA
16、(1)玻璃搅拌器 铜质金属导热能力强,造成较大误差
(2)偏大 (3)偏小 (4) 3.3 1379.4 (5) +124 kJ·mol-1
(6)C2H8N2(I)+2N2O4(g)=3N2(g)+2CO2(g)+4H2O(g) △H=(y-2x)kJ/mol
17、(1)+2 98.3%的浓硫酸 (2)将黄铁矿粉碎;提高煅烧温度;多鼓入空气等(3) (4)
(5) 23426 盐酸、溶液 (6)0.19
18、(1) 16 6 (2)醛基 氧化
+ +H2O
(3)n (4) C9H10O2 6
2024成都外国语学校高二上学期12月月考试题化学含答案: 这是一份2024成都外国语学校高二上学期12月月考试题化学含答案,共10页。试卷主要包含了本试卷分Ⅰ卷两部分,本堂考试75分钟,满分100分,答题前,考生务必先将自己的姓名,考试结束后,将答题卡交回等内容,欢迎下载使用。
2024长春外国语学校高二上学期12月月考试题化学含答案: 这是一份2024长春外国语学校高二上学期12月月考试题化学含答案,共5页。试卷主要包含了1ml·L-1的溶液中等内容,欢迎下载使用。
2024成都外国语学校高一上学期10月月考试题化学含解析: 这是一份2024成都外国语学校高一上学期10月月考试题化学含解析,共20页。试卷主要包含了本试卷分Ⅰ卷和Ⅱ卷两部分,答题前,考生务必先将自己的姓名,考试结束后,将答题卡交回等内容,欢迎下载使用。












