所属成套资源:全套人教版高中化学选择性必修2课时练习+章末提升含答案
高中人教版 (2019)第二节 原子结构与元素的性质同步训练题
展开
这是一份高中人教版 (2019)第二节 原子结构与元素的性质同步训练题,共14页。试卷主要包含了关于元素周期表的说法正确的是,元素A的各级电离能数据如下,8~1等内容,欢迎下载使用。
(一)基础巩固
1.(2023·广东高三四校联考)下列性质的比较,不能用元素周期律解释的是 ( )
A.原子半径:S>Cl
B.稳定性:H2SeCl-
D.酸性:H2SO4>H3PO4
解析:同周期主族元素,原子序数越大,原子半径越小,由于原子序数Cl>S,所以原子半径S>Cl,与元素周期律有关,A项正确;元素的非金属性越强,简单氢化物的稳定性越强,由于非金属性S>Se,所以稳定性H2SeH2S,所以结合质子能力S2->Cl-,不能用元素周期律解释,C项错误;元素的非金属性S>P,所以其最高价氧化物的水化物酸性H2SO4>H3PO4,与元素周期律有关,D项正确。
答案:C
2.(2022·广东惠州)关于元素周期表的说法正确的是 ( )
A.除ds区外,各区的名称来自按照构造原理最后填入电子的能级的符号
B.最外层电子数为2的元素都分布在s区
C.第二周期元素中,第一电离能介于B、N之间的有1种元素
D.第四周期的金属元素从左到右,元素的金属性依次减弱
解析:最外层电子数为2的元素不都分布在s区,如He在p区,Sc、Ti、V、Mn、Fe、C、Ni等在d区,B项错误;同一周期从左到右,元素的第一电离能呈增大趋势,ⅡA与ⅢA、VA与ⅥA之间反常,故第二周期元素中,第一电离能介于B、N之间的有Be、C、O 3种元素,C项错误;第四周期主族金属元素从左到右,元素的金属性依次减弱,副族元素不一定符合这种规律,如金属性:Zn>Fe,D项错误。
答案:A
3.下图表示前20号元素的原子序数和气态原子失去核外第一个电子所需的能量的变化关系,其中A、B、C各点表示的元素分别是 ( )
A.N、S、P B.F、Cl、O
C.He、Ne、Ar D.Si、C、B
解析:稀有气体元素的原子结构为稳定结构,失去一个电子所需能量是同周期元素中最高的,故A、B、C分别代表He、Ne、Ar。
答案:C
4.下列是几种基态原子的核外电子排布,电负性最大的元素是 ( )
A.1s22s22p4B.1s22s22p63s23p3
C.1s22s22p63s23p2D.1s22s22p63s23p64s2
解析:A项是氧元素,B项是磷元素,C项是硅元素,D项是钙元素,所以非金属性最强的元素是氧元素,即电负性最大的元素是氧元素。
答案:A
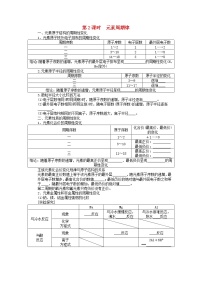
5.元素A的各级电离能数据如下:
则A元素的常见价态为 ( )
A.+1价 B.+2价
C.+3价 D.+4价
解析:通过观察A元素的各级电离能数据,发现I4≫I3,即A元素原子最外层有3个电子,常见价态为+3价。
答案:C
6.元素电负性随原子序数的递增而增强的是 ( )
A.NaNa;B、C、D三种元素分别为O、Na、S,其简单离子分别为O2-、Na+、S2-,其中O2-、Na+电子层结构相同,都为2层,S2-核外为三层,电子层数越多,半径越大,电子层数相同,核电荷数越大,半径越小,所以B、C、D三种元素的简单离子的半径由大到小的顺序为S2->O2->Na+。
答案:(1)7 1s22s22p63s23p63d54s1(或[Ar]3d54s1)
四 ⅠB 3d104s1
(2)N>O>S>Na S2->O2->Na+
(3)激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长(可见光区域)光的形式释放能量
9.电负性是元素的一种重要性质,电负性越大,其原子吸引电子的能力越强,在所形成的化合物中成为显负价的一方。下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,试回答下列问题。
(1)根据表中所给数据分析推测:
同主族不同元素的电负性变化的规律是 ;
同周期中,电负性与原子半径的关为 。
(2)预测周期表中电负性最大的元素应为 (填元素符号);估计钙元素的电负性的取值范围:
相关试卷
这是一份人教版 (2019)选择性必修2第二节 原子结构与元素的性质第2课时练习题,共2页。试卷主要包含了下列原子半径大小顺序正确的是,下列说法正确的是,下列有关电离能的说法中正确的是,下列对电负性的理解不正确的是,不能说明X的电负性比Y大的是等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修2第一节 原子结构第二课时课堂检测,共10页。试卷主要包含了下列关于微粒半径的说法正确的是,分析下列图表,回答问题等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修2第二节 原子结构与元素的性质免费课堂检测,共8页。