

吉林省梅河口市第五中学2024届高三化学上学期9月月考试题(Word版附答案)
展开
这是一份吉林省梅河口市第五中学2024届高三化学上学期9月月考试题(Word版附答案),共9页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。
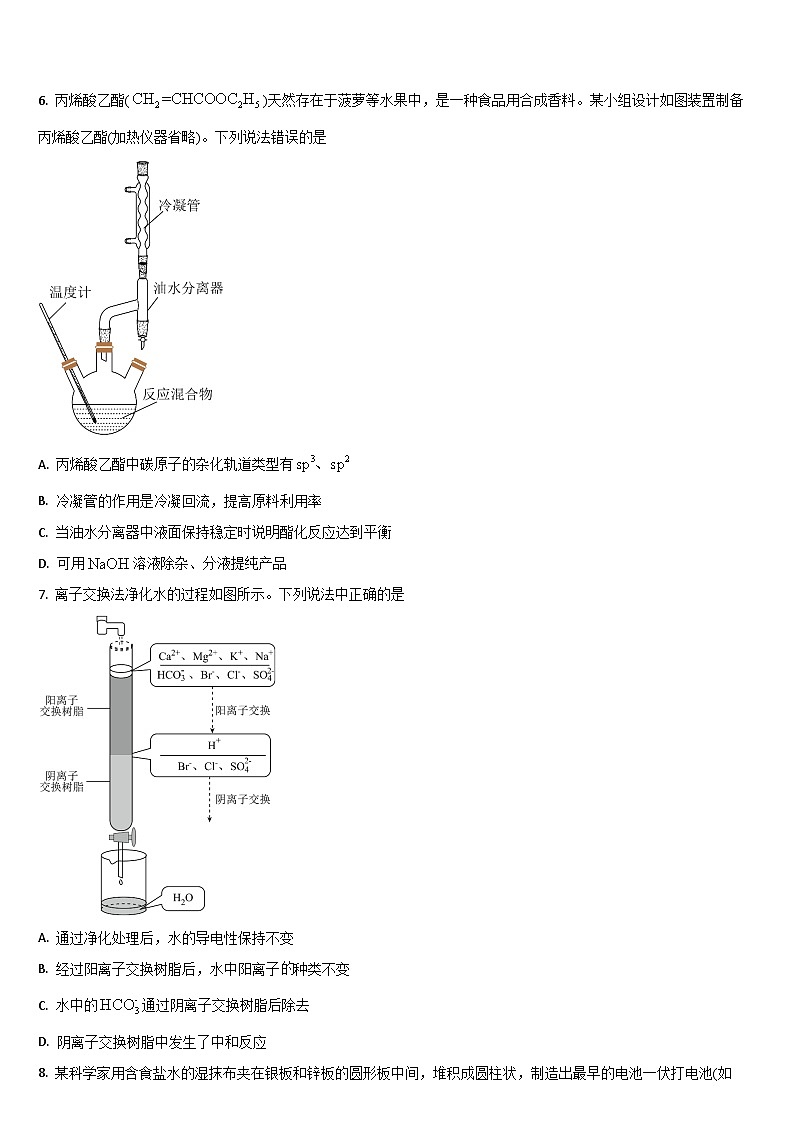
高三化学一、单项选择题(共计16个小题,每题4分,共64分)1.下列对文中描述内容的相关解释正确的是( )选项描述解释A丹砂烧之成水银,积变又还成丹砂两个反应互为可逆反应B凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之其中“瓦”的主要成分为硅酸盐C硝石(KNO3)……如握盐雪不冰,强烧之,紫青烟起产生“紫青烟”的原因为KNO3分解D其法用浓酒和糟入甑,蒸令气上,用器承滴露其中涉及的操作方法为蒸发浓缩2.NA是阿伏加德罗常数的值。下列说法正确的是( )A.22.4 L(标准状况)氮气中含有7NA个中子B.1 mol重水比1 mol水多NA个质子C.12 g 石墨烯和12 g金刚石均含有NA个碳原子D.1 L 1 mol·L-1NaCl溶液含有28NA个电子3.设NA为阿伏加德罗常数的值。下列说法正确的是( )A.1 mol OD-和17 g —OH所含的质子与中子均为9NAB.在标准状况下,4.48 L甲烷的氯代物分子含原子数目为NAC.8.8 g乙酸乙酯中含共用电子对的数目为1.3NAD.7.8 g Na2S与Na2O2的混合物,含离子总数为0.3NA4.下列实验操作都能达到预期目的的是( )①蒸干MgCl2溶液可得纯净的无水氯化镁;②可以采用多次渗析的方法分离、提纯蛋白质;③用广泛pH试纸测得某溶液pH为3.5;④滴入酚酞溶液确定纯碱中有无烧碱;⑤用米汤直接检验食用盐中是否含有碘元素;⑥用酸式滴定管量取20.00 mL高锰酸钾酸性溶液;⑦用溴的四氯化碳溶液除去混在甲烷中的乙烯气体A.⑥⑦ B.②⑥C.⑤⑥⑦ D.只有⑥5. 由下列实验及现象推出的相应结论正确的是( ) 实验现象结论A.某溶液中滴加铁氰化钾溶液产生蓝色沉淀原溶液中有Fe2+,无Fe3+B.向C6H5ONa溶液中通入CO2溶液变浑浊酸性:H2CO3>C6H5OHC.向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液生成黑色沉淀Ksp(CuS)<Ksp(ZnS)D.①某溶液中加入Ba(NO3)2溶液②再加足量盐酸①产生白色沉淀②仍有白色沉淀原溶液中有SO 6. 丙烯酸乙酯()天然存在于菠萝等水果中,是一种食品用合成香料。某小组设计如图装置制备丙烯酸乙酯(加热仪器省略)。下列说法错误的是A. 丙烯酸乙酯中碳原子的杂化轨道类型有B. 冷凝管的作用是冷凝回流,提高原料利用率C. 当油水分离器中液面保持稳定时说明酯化反应达到平衡D. 可用溶液除杂、分液提纯产品7. 离子交换法净化水的过程如图所示。下列说法中正确的是A. 通过净化处理后,水的导电性保持不变B. 经过阳离子交换树脂后,水中阳离子种类不变C. 水中的通过阴离子交换树脂后除去D. 阴离子交换树脂中发生了中和反应8. 某科学家用含食盐水的湿抹布夹在银板和锌板的圆形板中间,堆积成圆柱状,制造出最早的电池一伏打电池(如图)。下列叙述正确的是A. 该电池中电子由银极经导线流向锌极B. 银极上消耗(标准状况下)氧气时,转移电子C. 若用稀硫酸替代食盐水,则在正极放电的物质不变D. 该电池负极的电极反应式为9. 《明会典》中记载:“嘉靖中则例,通宝钱六百万文,合用二火黄铜四万七千二百七十二斤……”这里黄铜是铜锌合金。下列说法错误的是A. 锌、铜均位于元素周期表的区B. 在铜、锌中,第二电离能与第一电离能相差较大的是锌C. 在潮湿空气中,与黄铜中的铜相比,纯铜中的铜更容易被腐蚀D. 用黄铜不用铁铸造“通宝钱”,主要因为黄铜的化学性质比铁稳定10. 已知:由镍、镁、碳三种元素组成的一种物质,晶胞如图所示,其中面心上的镍原子构成正八面体,正八面体的边长为,设为阿伏加德罗常数的值。下列说法正确的是A. 的价层电子排布式为B. 该物质可表示为C. 该晶体的摩尔体积为D. 处于状态的原子跃迁到基态时产生吸收光谱11. 光刻胶是光刻机制造芯片必不可少的重要材料,可用降冰片烯与马来酸酐共同加聚而成。下列说法不正确的是A. 1mol马来酸酐与氢氧化钠溶液反应最多消耗2molNaOHB. 降冰片烯与互为同分异构体C. 该光刻胶合成过程中可能会出现链节:D. 降冰片烯的一氯代物有4种12. 次磷酸(H3PO2)是一元中强酸,次磷酸钠(NaH2PO2)广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如图所示。下列有关说法正确的是A. Ni2+价电子的轨道表示式为B. “碱溶”时氧化剂与还原剂的物质的量之比为3:1C. PH3、PO中P的杂化方式相同,键角PO>PH3D. 次磷酸铵与足量氢氧化钠共热,发生反应NH+H2PO+3OH-NH3↑+3H2O+PO答案选C。13. 下列实验操作、现象及得出的结论均正确的是选项实验操作现象结论A向两支盛有KI3溶液的试管中分别滴加淀粉溶液和AgNO3溶液前者溶液变蓝,后者有黄色沉淀生成KI3溶液中存在平衡:II2+I-B向两支盛有5mL6%H2O2溶液的试管中分别加入1mL0.1mol/LFeCl3溶液和1mL0.1mol/LCuSO4溶液滴加FeCl3溶液比滴加CuSO4溶液的试管中相同时间内产生气泡多Fe3+催化效果好C向盛有Fe(NO3)2溶液的试管中加入1mol/L的硫酸试管口出现红棕色气体溶液中的NO被Fe2+还原为NO2D常温下,用pH计分别测定等体积1mol/LCH3COONH4溶液和0.1mol/L CH3COONH4溶液pHpH均为7 两种CH3COONH4溶液中水的电离程度相同 A. A B. B C. C D. D14. 苯乙醛可用于制备工业香料,工业上通过以下途径制备苯乙醛。下列说法正确的是A. 反应①、②和④符合绿色化学的原则B. 乙烯、苯乙醇、苯乙醛均能因反应而使酸性高锰酸钾溶液和溴水褪色C. 向 2 mL10%的硫酸铜溶液中滴加 5 滴 2%的氢氧化钠溶液,再加入 0.5 mL 苯乙醛溶液,加热,有砖红色沉淀出现D. 预测可以发生反应15. 氯化亚铜是一种白色结晶或白色粉末、微溶于水,不溶于稀盐酸和乙醇,见光易分解,暴露于潮湿的空气中易被氧化为绿色的Cu2(OH)3Cl。以CuCl2粗品(含Fe2+杂质)为原料制备CuCl晶体的工艺流程如图1。下列说法错误的是已知:在较高浓度的盐酸中,Fe3+能溶解于有机溶剂甲基异丁基甲酮中。A. “溶解”时加入的酸为浓盐酸B. “一系列操作”指抽滤、洗涤、干燥C. “萃取”时采用如图2所示方法进行振荡D. “还原”反应的离子方程式为2Cu2++SO2+2H2O+2Cl-=2CuCl↓+SO+4H+16. 零价纳米铁在有机氯化物降解等方面有重要作用,采用强还原剂硼氢化钾液相还原法制备纳米零价铁的化学反应如下:,其中B元素化合价不变。下列说法正确的是A. 是氧化产物B. 已知纳米Fe颗粒直径为60nm,则纳米Fe颗粒为胶体C. 若有参加反应,则反应中转移电子的物质的量为4molD. 该反应的氧化剂只有,还原剂只有 二、非选择题17.(12分)无水是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水的实验装置如图所示:E和G用来收集产物。回答下列问题:(1)在E、G处收集产物是利用了_______的性质。(2)实验过程中若F处出现堵塞,则在B处可观察到的现象是_______。可通过_______(填简单操作),使实验能继续进行。(3)某同学用干燥铁粉制得无水样品,该次实验的产率是_______。(4)实验室中还常用与晶体共热制备无水,其化学反应方程式为_______.检验水合三氯化铁原料中是否存在的试剂是_______。(填化学式)18. 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(,含有少量、、、等元素)制备的流程如下:已知:,,。回答下列问题:(1)硫酸溶矿主要反应的化学方程式为___________。为提高溶矿速率,可采取的措施___________(举1例)。(2)加入少量的作用是___________。(3)溶矿反应完成后,反应器中溶液,此时___________;用石灰乳调节至,除去的金属离子是___________。(4)加入少量溶液除去,生成的沉淀有___________。(5)在电解槽中,发生电解反应的离子方程式为___________。(6)煅烧窑中,生成反应的化学方程式是___________。19. 金属对有强吸附作用,被广泛用于硝基或羰基等不饱和基团的倠化氢化反应,将块状转化成多孔型雷尼后,其倠化活性显著提高。已知:①雷尼暴露在空气中可自然,在制备和使用时,需用水或有机溶剂保持表面“湿润”。②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。某实验小组制备雷尼并探究其催化氢化性能的实验如下:步骤1:雷尼的制备 步骤2:邻硝基苯胺的催化氢化反应反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置用于储存和监测反应过程。 回答下列问题:(1)仪器M的名称是___________;(2)操作(a)中,反应的离子方程式是___________;(3)操作(d)中,判断雷尼被水洗净的方法是___________;(4)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是___________;A. 丙酮 B. 四氯化碳 C. 乙醇 D. 正己烷(5)反应前应向装置II中通入一段时间,目的是___________;(6)向集气管中充入时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置II供气,此时孔路位置需调节为___________; (7)判断氢化反应完全的现象是___________。 1-16 BCDBB DDBDC BCADCC17.【答案】(1)易升华 (2)B处有气泡产生 适当加热F处 (3)80.00% (4)+6SOCl2=FeCl3+12HCl+6SO2 铁氰化钾 18 【答案】(1) ①. ②. 粉碎矿石、适当增大硫酸的浓度、适当升高温度等(其中一条) (2)将氧化为,便于形成沉淀而除去 (3) ①. ②. (4)和 (5) (6)19【答案】(1)恒压滴液漏斗 (2)2Al+2OH-+6H2O=2[Al(OH)]+3H2↑ (3)取最后一次洗涤液于试管中,滴加几滴酚酞,如果溶液不变粉红色,则证明洗涤干净,否则没有洗涤干净 (4)C (5)排除装置中的空气,防止雷尼Ni自燃 (6)C (7)集气管中液面不再改变
相关试卷
这是一份吉林省通化市梅河口市第五中学2023-2024学年高一上学期12月月考化学试题Word版含答案,文件包含化学试题docx、化学试题答案pdf等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。
这是一份吉林省梅河口市第五中学2023-2024学年高二上学期12月月考化学试题(Word版附答案),共8页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
这是一份四川省江油中学2023-2024学年高三化学上学期9月月考试题(Word版附解析),共6页。试卷主要包含了考试结束后,将答题卡交回, 下列实验能达到目的的是等内容,欢迎下载使用。








