

- 新高考化学模拟试卷45(原卷版+教师版) 试卷 0 次下载
- 新高考化学模拟试卷46(原卷版+教师版) 试卷 0 次下载
- 新高考化学模拟试卷48(原卷版+教师版) 试卷 0 次下载
- 新高考化学模拟试卷49(原卷版+教师版) 试卷 0 次下载
- 新高考化学模拟试卷50(原卷版+教师版) 试卷 0 次下载
新高考化学模拟试卷47(原卷版+教师版)
展开注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Fe 56 C 59
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要求.
1.党的二十大报告指出我国已进入创新型国家行列。下列说法正确的是
A.“华龙一号”核电机组使用的氦气不存在分子
B.“奋斗者号”潜水器含钛合金,其强度、韧性高于纯钛金属
C.“祖冲之二号”中的半导体存储器主要成分为 SKIPIF 1 < 0
D.“嫦娥五号”带回的月壤中含有磁铁矿,其主要成分为 SKIPIF 1 < 0
2.下列化学用语使用正确的是
A. SKIPIF 1 < 0 的系统命名:1,3-二丁烯
B.过氧化氢的电子式:
C.As原子的简化电子排布式: SKIPIF 1 < 0
D.顺-2-丁烯的结构简式:
3.绿矾( SKIPIF 1 < 0 )分解可制备铁红,同时产生 SKIPIF 1 < 0 、 SKIPIF 1 < 0 和 SKIPIF 1 < 0 。设NA为阿伏加德罗常数的值,下列说法错误的是
A. SKIPIF 1 < 0 溶液含有的阳离子数大于NA
B.0.5ml三聚 SKIPIF 1 < 0 分子( )中含有σ键数目为6 NA
C.绿矾分解生成16g SKIPIF 1 < 0 时,转移电子数为0.2 NA
D.22.4L SKIPIF 1 < 0 溶于水,溶液中 SKIPIF 1 < 0 、 SKIPIF 1 < 0 、 SKIPIF 1 < 0 的数目总和为NA
4.古代科学典籍富载化学知识,下述之物见其还原性者为
A.胆矾( SKIPIF 1 < 0 ):“熬胆矾铁釜,久之亦化为铜”
B.脂水(石油):“高奴县出脂水,……颇似淳漆,燃之如麻,但烟甚浓”
C.胡粉 SKIPIF 1 < 0 :“胡粉得雌黄( SKIPIF 1 < 0 )而色黑(PbS),盖相恶也”
D.炉甘石( SKIPIF 1 < 0 ):“其(炉甘石)底铺薪,发火煅红,……即倭铅(Zn)也”
5.X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与其最高价氧化物对应水化物反应生成盐;Y元素原子的核外电子只有8种运动状态;Z为短周期金属元素,其简单离子的半径在同周期中最小;基态W原子的未成对电子数为6。下列说法错误的是
A.第一电离能:X>Y> Z
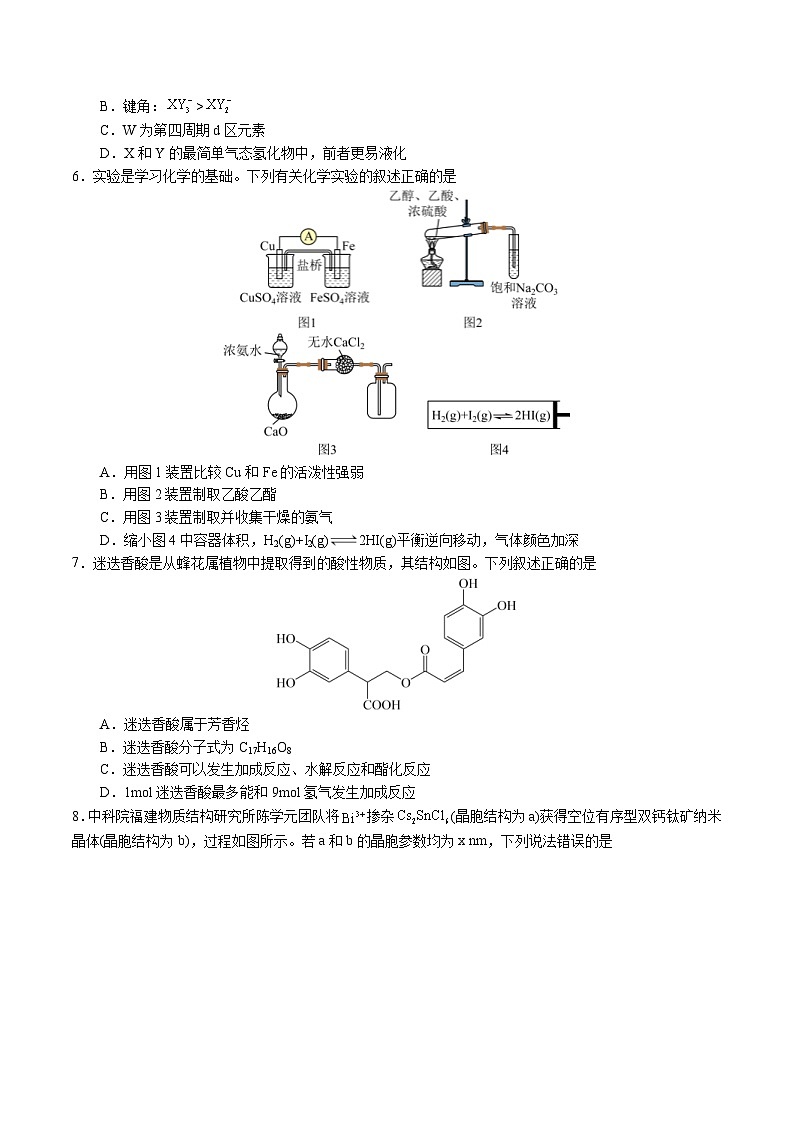
B.键角: SKIPIF 1 < 0 > SKIPIF 1 < 0
C.W为第四周期d区元素
D.X和Y的最简单气态氢化物中,前者更易液化
6.实验是学习化学的基础。下列有关化学实验的叙述正确的是
A.用图1装置比较Cu和Fe的活泼性强弱
B.用图2装置制取乙酸乙酯
C.用图3装置制取并收集干燥的氨气
D.缩小图4中容器体积,H2(g)+I2(g)2HI(g)平衡逆向移动,气体颜色加深
7.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是
A.迷迭香酸属于芳香烃
B.迷迭香酸分子式为C17H16O8
C.迷迭香酸可以发生加成反应、水解反应和酯化反应
D.1ml迷迭香酸最多能和9ml氢气发生加成反应
8.中科院福建物质结构研究所陈学元团队将 SKIPIF 1 < 0 掺杂 SKIPIF 1 < 0 (晶胞结构为a)获得空位有序型双钙钛矿纳米晶体(晶胞结构为b),过程如图所示。若a和b的晶胞参数均为x nm,下列说法错误的是
A.a中 SKIPIF 1 < 0 的配位数为8
B.a中两个最近的 SKIPIF 1 < 0 的距离为 SKIPIF 1 < 0
C.掺杂后的晶体的化学式为 SKIPIF 1 < 0
D. SKIPIF 1 < 0 和 SKIPIF 1 < 0 的中心原子的价层电子对数不相同
9.联氨(N2H4)可用于处理水中的溶解氧,其反应机理如下图所示:
下列说法不正确的是
A. SKIPIF 1 < 0 分子的共价键只有 SKIPIF 1 < 0 键
B. SKIPIF 1 < 0 具有还原性,在一定条件下可被 SKIPIF 1 < 0 氧化
C.②中反应产物是 SKIPIF 1 < 0 而不是 SKIPIF 1 < 0 ,说明 SKIPIF 1 < 0 相对较稳定
D.③中发生反应: SKIPIF 1 < 0
10.实验室以二氧化铺铈 SKIPIF 1 < 0 废渣为原料制备 SKIPIF 1 < 0 ,其部分实验过程如下:
已知: SKIPIF 1 < 0 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为:
SKIPIF 1 < 0 (水层) SKIPIF 1 < 0 (有机层) SKIPIF 1 < 0 (有机层)+ SKIPIF 1 < 0 (水层)。
下列说法正确的是
A.“酸浸”过程中 SKIPIF 1 < 0 做氧化剂
B.加氨水“中和”除去过量盐酸,主要目的是提高 SKIPIF 1 < 0 的萃取率
C.试剂a一定是盐酸
D.“沉淀”时反应的离子方程式为 SKIPIF 1 < 0
11.探究 SKIPIF 1 < 0 的性质,根据实验方案和现象,下列结论不正确的是
A.AB.BC.CD.D
12.能正确表示下列反应的离子方程式是
A. SKIPIF 1 < 0 溶液中滴入 SKIPIF 1 < 0 溶液: SKIPIF 1 < 0
B. SKIPIF 1 < 0 溶液中通入 SKIPIF 1 < 0 ,溶液变为黄绿色: SKIPIF 1 < 0
C. 溶液中加入少量盐酸:
D.泡沫灭火器的反应原理: SKIPIF 1 < 0
13.一种成本低、稳定性好的全碱性多硫化物---空气液流二次电池工作时,原理如图所示。下列说法正确的是
A.连接负载时,电极A为正极
B.连接负载时,阳极区的电极反应式为2 SKIPIF 1 < 0 - 2e- = SKIPIF 1 < 0
C.连接电源时,电路中每通过2 NA个电子,生成NaOH的质量为80 g
D.膜a为阴离子交换膜,膜b为阳离子交换膜
14. SKIPIF 1 < 0 制 SKIPIF 1 < 0 的平衡体系中存在如下反应:
反应Ⅰ: SKIPIF 1 < 0 SKIPIF 1 < 0
反应Ⅱ: SKIPIF 1 < 0 SKIPIF 1 < 0
将2 ml SKIPIF 1 < 0 和3 ml SKIPIF 1 < 0 投入容积为1L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性( SKIPIF 1 < 0 条件下)与温度、压强的关系如图所示。
已知:乙烯的选择性 SKIPIF 1 < 0 。下列说法错误的是
A.X代表温度,L代表压强
B. SKIPIF 1 < 0
C.N点时, SKIPIF 1 < 0 转化成的CO的物质的量为0.4 ml
D.M点时,反应Ⅰ的平衡常数为0.5
15.25 ℃时,用同一NaOH溶液分别滴定一元酸HA溶液和 SKIPIF 1 < 0 溶液,pM [p表示负对数,M表示 SKIPIF 1 < 0 、 SKIPIF 1 < 0 ]与溶液pH的变化关系如图所示。已知: SKIPIF 1 < 0 易溶于水,一般认为反应的平衡常数 SKIPIF 1 < 0 时反应进行完全。下列说法错误的是
A.HA为一元弱酸,25 ℃时 SKIPIF 1 < 0
B.线①代表滴定 SKIPIF 1 < 0 溶液时pM与溶液pH的变化关系
C.滴定HA溶液至x点时,溶液中 SKIPIF 1 < 0
D.滴定 SKIPIF 1 < 0 溶液至x点时,改为滴加HA溶液,沉淀逐渐完全溶解
二、非选择题:本题共4小题,共55分。
16.(14分)
钕铁硼( SKIPIF 1 < 0 )磁铁因其超强的磁性被誉为“永磁之王”。已知某钕铁硼废料中主要成分为 SKIPIF 1 < 0 等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物。以下为一种利用钕铁硼废料制取 SKIPIF 1 < 0 和 SKIPIF 1 < 0 的工艺流程:
①钕的活动性较强,能与酸发生置换反应,其稳定的化合价为 SKIPIF 1 < 0 价;
②某些金属氢氧化物沉淀完全时的 SKIPIF 1 < 0 如下表所示:
回答下列问题:
(1)钴( SKIPIF 1 < 0 )元素在元素周期表第_______周期第_______族。
(2)钕铁硼废料“浸出”前需“预处理”,先将其进行粉碎,再除去表面的矿物油污。除去矿物油污可以选择的试剂是_______(填标号)。
A.苯B. SKIPIF 1 < 0 溶液C.纯碱溶液D.稀硫酸
(3)“沉钕”过程调 SKIPIF 1 < 0 ,得到 SKIPIF 1 < 0 晶体,写出生成沉淀的离子方程式____________________________。
(4)“沉钕”后的滤液中加入试剂1的作用是_____________________;若溶液中 SKIPIF 1 < 0 ,根据表中数据计算,加入试剂2调节 SKIPIF 1 < 0 范围是6~_______(忽略过程中溶液体积变化)。
(5)“萃取”时发生反应: SKIPIF 1 < 0 ,则试剂3为______________,设计萃取、反萃取的目的是_____________________。
(6)某钴的一种氧化物也是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图甲中原子A的坐标为 SKIPIF 1 < 0 ,B为 SKIPIF 1 < 0 ,则C原子的坐标为_______。
②若阿伏加德罗常数的值为 SKIPIF 1 < 0 ,则晶体密度为_______ SKIPIF 1 < 0 (列出计算式)。
17.(13分)
将 SKIPIF 1 < 0 和 SKIPIF 1 < 0 两种气体转化为合成气( SKIPIF 1 < 0 和CO),可以实现能量综合利用,对环境保护具有十分重要的意义。甲烷及二氧化碳重整涉及以下反应:
Ⅰ. SKIPIF 1 < 0 SKIPIF 1 < 0 平衡常数 SKIPIF 1 < 0
Ⅱ. SKIPIF 1 < 0 SKIPIF 1 < 0 平衡常数 SKIPIF 1 < 0
Ⅲ. SKIPIF 1 < 0 SKIPIF 1 < 0 SKIPIF 1 < 0 SKIPIF 1 < 0 平衡常数 SKIPIF 1 < 0
(1) SKIPIF 1 < 0 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 ml该物质的焓变。对于稳定相态单质,其 SKIPIF 1 < 0 为零。根据下表数据,计算反应Ⅱ的反应热 SKIPIF 1 < 0 ___________,该反应正反应活化能___________逆反应活化能(填“大于”、“小于”或“等于”)。
(2)平衡常数 SKIPIF 1 < 0 ___________(用 SKIPIF 1 < 0 、 SKIPIF 1 < 0 表示)。
(3)一定温度下,维持压强 SKIPIF 1 < 0 ,向一密闭容器中通入等物质的量的 SKIPIF 1 < 0 和 SKIPIF 1 < 0 发生反应。已知反应Ⅱ的速率方程可表示为 SKIPIF 1 < 0 , SKIPIF 1 < 0 ,其中 SKIPIF 1 < 0 、 SKIPIF 1 < 0 分别为正、逆反应的速率常数,则以物质的分压表示的反应Ⅱ的平衡常数 SKIPIF 1 < 0 ___________(用 SKIPIF 1 < 0 、 SKIPIF 1 < 0 表示),另lgk与 SKIPIF 1 < 0 的关系如图所示,①、②、③、④四条直线中,表示 SKIPIF 1 < 0 的是___________(填序号), SKIPIF 1 < 0 温度时,图中A、B、C、D点的纵坐标分别为 SKIPIF 1 < 0 、 SKIPIF 1 < 0 、 SKIPIF 1 < 0 、 SKIPIF 1 < 0 ,达到平衡时,测得 SKIPIF 1 < 0 的转化率为60%,且体系中 SKIPIF 1 < 0 ,则 SKIPIF 1 < 0 ___________,以物质的分压表示的反应I的平衡常数 SKIPIF 1 < 0 ___________。(用含 SKIPIF 1 < 0 的代数式表示,已知:lg5=0.7)
18.(14分)
研究表明物质的颜色与吸收光的波长( SKIPIF 1 < 0 )有关,而颜色的深浅与吸光度(A)有关。如 SKIPIF 1 < 0 的吸光度随显色剂 SKIPIF 1 < 0 浓度的增大而增大(如图甲),随着n的增加,颜色由红色逐渐加深至血红色。某科研小组为了研究影响 SKIPIF 1 < 0 颜色的因素,设计了如下实验:
(1)配制500mL SKIPIF 1 < 0 的 SKIPIF 1 < 0 溶液。用电子天平准确称取8.125g无水 SKIPIF 1 < 0 晶体,溶解在约150mL_______中,冷却后配制成500mL溶液待用,此过程应该用到的玻璃仪器有烧杯、玻璃棒、量筒、500mL容量瓶、________________。
(2)取配制好的 SKIPIF 1 < 0 溶液5mL,加入( SKIPIF 1 < 0 KSCN溶液5mL,溶液呈红色,将此红色溶液平均分装在a、b、c三支试管中,进行分析:
①取a试管,加入抗坏血酸( )发现溶液红色立即褪去,小组成员查阅资料确认脱氢抗坏血液( )的产生是褪色的主要原因,则此过程反应的离子方程式为___________________________________________。
②取b试管,加入 SKIPIF 1 < 0 溶液,发现溶液红色缓慢褪去,同时产生大量无色、无味、无毒气体,经检验后确认气体有两种成分,其中一种是 SKIPIF 1 < 0 ,可用于检验另一种气体的试剂是________________。
③取c试管,发现红色溶液放置一段时间颜色变浅,具体的原因可能是______________。
(3)研究小组在研究酸碱性对 SKIPIF 1 < 0 与 SKIPIF 1 < 0 显色反应的平衡体系的影响时,通过数据采集器得到pH及显色时间对吸光度(A)的影响如图乙:
由图乙数据可以发现,进行该显色反应时需控制溶液pH为_______;pH太小或太大均不利于显色反应的研究,理由是_________________________。
(4) SKIPIF 1 < 0 与 SKIPIF 1 < 0 反应可以生成配位数从1到6的配离子 SKIPIF 1 < 0 ,其水溶液都是红色,而 SKIPIF 1 < 0 与 SKIPIF 1 < 0 配位时,溶液接近无色。研究小组收集到了 SKIPIF 1 < 0 的逐级稳定常数(K)的数据(见表),并由此推算出累积稳定常数( SKIPIF 1 < 0 ),已知 SKIPIF 1 < 0 。
如: SKIPIF 1 < 0
SKIPIF 1 < 0
则 SKIPIF 1 < 0 。
① SKIPIF 1 < 0 的平衡常数K=_______(保留3位有效数字)。
②某补血药片的主要成分是琥珀酸亚铁,现在已经部分变质(即铁元素被氧化),请根据表中数据设计实验证明该药片确实是部分变质:取部分变质的药片,剥去表面糖衣,研细成粉末,加水溶解,________________,则证明溶液中有 SKIPIF 1 < 0 ,即药片部分变质(试剂可以任选)
19.(14分)
呫吨酮衍生物是治疗糖尿病的有效药,某呫吨酮衍生物的合成路线如下。
已知:I. SKIPIF 1 < 0
II. SKIPIF 1 < 0 为苯基:
回答下列问题:
(1)A→B的反应类型为_______,该反应的目的是________________。
(2)C→D的过程中,被还原的官能团是_______(写名称)。
(3)下列有关说法错误的是_______。
A.化合物A的名称是2,6-二羟基苯甲酸乙酯
B.化合物B含4种不同官能团
C.化合物E既有酸性又有碱性
D.用 SKIPIF 1 < 0 溶液可以鉴别化合物F和G
(4)化合物F易溶于水,主要原因是________________。
(5)化合物E的同分异构体中,仅含-CONH2、-OH和苯环结构的有_______种。F→G的反应会生成一种副产物H,H与化合物G互为同分异构体,H的结构简式为_______。
(6)请你以及苯酚为原料参照上述流程信息合成呫吨酮():___________________________________________(其他无机试剂任选)。实验方案
现象
结论
A
测定均为离子化合物的 SKIPIF 1 < 0 和 SKIPIF 1 < 0
SKIPIF 1 < 0 的熔点更高
SKIPIF 1 < 0 中离子键强于 SKIPIF 1 < 0 中离子键
B
常温下,测定 SKIPIF 1 < 0 SKIPIF 1 < 0 溶液的 SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0 发生了水解
C
向 SKIPIF 1 < 0 SKIPIF 1 < 0 溶液中滴加1滴 SKIPIF 1 < 0 酸性 SKIPIF 1 < 0 溶液
SKIPIF 1 < 0 紫色褪去,溶液澄清
SKIPIF 1 < 0 将 SKIPIF 1 < 0 氧化为 SKIPIF 1 < 0
D
向 SKIPIF 1 < 0 溶液中加入 SKIPIF 1 < 0
产生淡黄色沉淀
SKIPIF 1 < 0 将 SKIPIF 1 < 0 氧化为 SKIPIF 1 < 0
沉淀
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
沉淀完全的 SKIPIF 1 < 0
5.2
3.2
9.4
9.5
10.1
8.5
物质
SKIPIF 1 < 0
SKIPIF 1 < 0
CO
SKIPIF 1 < 0
SKIPIF 1 < 0 ( SKIPIF 1 < 0 )
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
配位体
金属离子
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
26.9
22.9
20.0
0.79
0.79
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
4.47
SKIPIF 1 < 0
SKIPIF 1 < 0
—
—
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
—
—
—
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
—
—
—
新高考化学模拟试卷全解全析
(考试时间:75分钟 试卷满分:100分)
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要求.
1.【答案】B
【详解】
A.氦气是氮原子分子,故A错误;
B.钛合金为合金材料,硬度大,其强度、韧性高于纯钛金属,故B正确;
C.“祖冲之二号”中的半导体存储器主要成分为Si,故C错误;
D.磁铁矿主要成分为 SKIPIF 1 < 0 ,故D错误。
综上所述,答案为B。
2.【答案】D
【详解】
A. SKIPIF 1 < 0 的系统命名为1, SKIPIF 1 < 0 丁二烯,A错误;
B.过氧化氢的电子式为 ,B错误;
C. SKIPIF 1 < 0 原子核外共有33个电子,故简化的电子排布式为 SKIPIF 1 < 0 ,C错误;
D.顺-2-丁烯的结构简式 ,D正确;
故选D。
3.【答案】D
【详解】
A.硫酸亚铁是强酸弱碱盐,亚铁离子在溶液中水解使溶液中的阳离子数目增大,则1L1ml/L硫酸亚铁溶液含有的阳离子数大于1ml/L ×1L×NAml—1=NA,故A正确;
B.由结构可知,三聚三氧化硫分子中含有的σ键为12,则0.5ml三聚三氧化硫分子中含有的σ键的数目为0.5ml×12×NAml—1=6NA,故B正确;
C.由题意可知,绿矾受热分解的方程式为2FeSO4·7H2O SKIPIF 1 < 0 Fe2O3+SO2↑+SO3↑+7H2O,反应生成1ml三氧化铁,反应转移2ml电子,则生成16g三氧化铁时,转移电子数为 SKIPIF 1 < 0 ×2×NAml—1=0.2 NA,故C正确;
D.缺标准状况,无法计算22.4L二氧化硫的物质的量,且二氧化硫与水反应为可逆反应,可逆反应不可能完全进行,所以无法计算使溶液中亚硫酸、亚硫酸氢根、亚硫酸根的数目总和,故D错误;
故选D。
4.【答案】B
【详解】
A.题中涉及反应 SKIPIF 1 < 0 ,铜元素的化合价降低, SKIPIF 1 < 0 体现氧化性,A项不符合题意;
B.脂水指石油,燃烧过程中发生氧化反应,石油体现还原性,B项符合题意;
C.“胡粉得雌黄( SKIPIF 1 < 0 )而色黑(PbS)”过程中Pb元素化合价不变,胡粉未发生氧化还原反应,C项不符合题意;
D. SKIPIF 1 < 0 最终转化为Zn,Zn元素化合价降低,被还原, SKIPIF 1 < 0 作氧化剂,体现其氧化性,D项不符合题意。
故答案选B。
5.【答案】D
【详解】
X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能与其最高价氧化物对应水化物反应生成盐;X是N元素;Y元素原子的核外电子只有8种运动状态,Y是O元素;Z为短周期金属元素,其简单离子的半径在同周期中最小,Z是Al元素;基态W原子的未成对电子数为6,W是Cr元素。
A.Al是金属元素,第一电离能最小,N原子2p能级半充满,结构稳定,第一电离能大于同周期相邻元素,所以第一电离能: N>O>Al,故A正确;
B. SKIPIF 1 < 0 中N原子价电子对数为 SKIPIF 1 < 0 ,无孤电子对; SKIPIF 1 < 0 中N原子价电子对数为 SKIPIF 1 < 0 ,有1个孤电子对,所以键角 SKIPIF 1 < 0 > SKIPIF 1 < 0 ,故B正确;
C.W是Cr元素,价电子排布为3d54s1,为第四周期d区元素,故C正确;
D.NH3常温下为气体,H2O常温下为液体,H2O的沸点大于NH3,H2O更易液化,故D错误;
选D。
6.【答案】A
【详解】
A.图1装置为原电池,根据电流表可判断形成的原电池的正负极,Fe为负极,Cu为正极,可说明Fe比Cu活泼,A项正确;
B.导气管伸入饱和 SKIPIF 1 < 0 溶液中太长,导气管应在液面上,B项错误;
C.氨气会和无水 SKIPIF 1 < 0 反应生成 SKIPIF 1 < 0 ,应用碱石灰干燥,收集氨气用向下排空气法,C项错误;
D. SKIPIF 1 < 0 为气体分子数不变的反应,缩小容器体积,平衡不移动,气体颜色加深是因为缩小容器体积, SKIPIF 1 < 0 的浓度增大,D项错误。
故选A。
7.【答案】C
【详解】
A.由题干有机物结构简式可知,迷迭香酸中含有苯环,则属于芳香族化合物,含有氧原子,不属于烃,A错误;
B.由题干有机物结构简式可知,迷迭香酸分子式为C18H16O8,B错误;
C.由题干有机物结构简式可知,迷迭香酸含有羟基、羧基和酯基三种含氧官能团,且含有苯环,迷迭香酸可以发生水解反应、加成反应和酯化反应,C正确;
D.由题干有机物结构简式可知,迷迭香酸含有2个苯环,1个碳碳双键可以和H2加成,故1ml迷迭香酸最多能和7ml氢气发生加成反应,D错误;
故答案为:C。
8.【答案】D
【详解】
A.由图可知,a中 SKIPIF 1 < 0 的配位数为8,A正确;
B.a中两个最近的 SKIPIF 1 < 0 的距离为面对角线长的一半,故为 SKIPIF 1 < 0 ,B正确;
C.根据晶胞结构b可知,每个晶胞中含有 SKIPIF 1 < 0 个 SKIPIF 1 < 0 、8个 SKIPIF 1 < 0 、 SKIPIF 1 < 0 个 SKIPIF 1 < 0 ,则掺杂后的晶体的化学式为 SKIPIF 1 < 0 ,C正确;
D. SKIPIF 1 < 0 和 SKIPIF 1 < 0 的中心原子的价层电子对数均为6,D错误;
故选D。
9.【答案】A
【详解】
A.N2H4分子的共价键有N-H之间的 SKIPIF 1 < 0 键和N-N之间的 SKIPIF 1 < 0 ,A错误;
B.由题干信息可知,N2H4能够被CuO氧化生成N2,即N2H4具有还原性,而O2的氧化性强于CuO,故N2H4具有还原性,在一定条件下可被O2氧化,B正确;
C.由题干信息可知,②中反应物NH3‧H2O是足量的,但是反应产物是 SKIPIF 1 < 0 而不是 SKIPIF 1 < 0 ,说明 SKIPIF 1 < 0 相对较稳定,C正确;
D.根据氧化还原反应配平可知,③中发生反应: SKIPIF 1 < 0 ,D正确;
故答案为:A。
10.【答案】B
【详解】
二氧化铈( SKIPIF 1 < 0 )废渣加入盐酸、过氧化氢酸浸,得到含有 SKIPIF 1 < 0 的溶液,加入氨水中和过量的盐酸,加入萃取剂HA萃取后再加入酸反萃取,分离出水层,加入氨水、碳酸氢铵生成 SKIPIF 1 < 0 ;
A.由流程可知,“酸浸”过程中四价铈转化为三价铈,铈化合价降低为氧化剂,根据电子守恒可知,则 SKIPIF 1 < 0 中氧元素化合价升高,做还原剂,故A错误;
B.加氨水“中和”去除过量盐酸,降低氢离子浓度,利于平衡向萃取 SKIPIF 1 < 0 的方向移动,目的是提高 SKIPIF 1 < 0 的萃取率,故B正确;
C.根据萃取原理可知,“反萃取”中通过增大氢离子浓度使平衡逆向移动,有利于将有机层 SKIPIF 1 < 0 尽可能多地转移到水层,试剂a可为盐酸或硝酸,故C错误;
D.“沉淀”时 SKIPIF 1 < 0 、氨水、碳酸氢铵反应生成 SKIPIF 1 < 0 沉淀,反应的离子方程式为 SKIPIF 1 < 0 ,故D错误;
故选B。
11.【答案】C
【详解】
A.离子化合物的熔点和离子化合物的晶格能有关,钠离子半径比钾离子半径更小,硫化钠的晶格能更大, SKIPIF 1 < 0 中离子键强于 SKIPIF 1 < 0 中离子键,故 SKIPIF 1 < 0 的熔点更高,A正确;
B.硫离子水解导致溶液显碱性,pH大于7,B正确;
C.硫离子具有还原性、高锰酸钾具有强氧化性,反应中硫化钠过量,高锰酸钾不足,反应生成硫单质,生成的硫单质溶于硫化钠溶液而显黄色,C错误;
D.过氧化氢将硫离子氧化为硫单质,产生淡黄色沉淀,D正确;
故选C。
12.【答案】B
【详解】
A. SKIPIF 1 < 0 与 SKIPIF 1 < 0 , SKIPIF 1 < 0 在酸性条件下的氧化性比 SKIPIF 1 < 0 强,所以反应为: SKIPIF 1 < 0 ,A错误;
B. SKIPIF 1 < 0 溶液中通入 SKIPIF 1 < 0 ,生成黄绿色的 SKIPIF 1 < 0 离子,反应的离子方程式为: SKIPIF 1 < 0 ,B正确;
C. 溶液中加入少量盐酸,应先反应生成酚羟基,C错误;
D.泡沫灭火器的反应原理: SKIPIF 1 < 0 ,D错误;
故选B。
13.【答案】B
【详解】
该电池为碱性多硫化物---空气液流二次电池,所以放电时通入空气的一极为正极,即电极B为正极,电极A为负极,充电时电极B为阳极,电极A为阴极。
A.连接负载时为原电池,电极B为正极,A错误;
B.连接负载时为原电池,电极A为负极,发生氧化反应为阳极区,电极反应为2 SKIPIF 1 < 0 - 2e- = SKIPIF 1 < 0 ,B正确;
C.连接电源时为电解池,电极B反应为4OH--4e-=O2+2H2O,电极A反应为 SKIPIF 1 < 0 + 2e- =2 SKIPIF 1 < 0 ,不产生NaOH,C错误;
D.放电时,正极发生还原反应,反应为O2+2H2O+4e-=4OH-;负极发生氧化反应,反应为2 SKIPIF 1 < 0 - 2e- = SKIPIF 1 < 0 ;正极区氢氧根离子向左侧运动,离子交换膜b为阴离子交换膜;负极区钠离子向右侧运动,离子交换膜a为阳离子交换膜,D错误;
综上所述答案为B。
14.【答案】D
【详解】
A.根据题给平衡体系中方程式特点判断,两个反应均为吸热反应,温度升高,平衡均正向移动,乙烷的平衡转化率会增大,两个反应均为气体分子数增大的反应,压强增大,平衡逆向移动,乙烷的平衡转化率会减小,而图像中随着X的增大,乙烷的平衡转化率逐渐增大,则X代表温度,L代表压强,A项正确;
B.同一温度下, SKIPIF 1 < 0 对应的乙烷平衡转化率低于 SKIPIF 1 < 0 对应的,即 SKIPIF 1 < 0 代表的压强大于 SKIPIF 1 < 0 的,B项正确;
C.根据乙烯的选择性公式判断,反应中,乙烷转化成的乙烯的物质的量为 SKIPIF 1 < 0 ml,则乙烷转化成的CO的物质的量为 SKIPIF 1 < 0 ml,C项正确;
D.M点对应温度下,设平衡时 SKIPIF 1 < 0 、 SKIPIF 1 < 0 的物质的量分别为x ml、3y ml,根据物质的量关系可列出三段式:
SKIPIF 1 < 0
SKIPIF 1 < 0
结合图像可知, SKIPIF 1 < 0 , SKIPIF 1 < 0 ,解得 SKIPIF 1 < 0 , SKIPIF 1 < 0 ,则平衡时 SKIPIF 1 < 0 、 SKIPIF 1 < 0 、 SKIPIF 1 < 0 、 SKIPIF 1 < 0 、 SKIPIF 1 < 0 的物质的量分别为1 ml、1.8 ml、0.8 ml、1.6 ml、0.8 ml,反应Ⅰ的平衡常数 SKIPIF 1 < 0 ,D项错误。
故选D。
15.【答案】D
【详解】
A.根据NaOH溶液与HA溶液、 SKIPIF 1 < 0 溶液的反应可知,随着NaOH溶液的滴加,pH增大, SKIPIF 1 < 0 逐渐减小, SKIPIF 1 < 0 变大,所以线①代表滴定 SKIPIF 1 < 0 溶液时pM与溶液pH的变化关系,线②代表滴定一元酸HA溶液时pM与pH的变化关系,从线②与横坐标轴的交点可知 SKIPIF 1 < 0 时, SKIPIF 1 < 0 , SKIPIF 1 < 0 ,选项A正确;
B.根据上述分析可知,线①代表滴定 SKIPIF 1 < 0 溶液时pM与溶液pH的变化关系,选项B正确;
C.x点溶液呈酸性,则 SKIPIF 1 < 0 ,根据电荷守恒得 SKIPIF 1 < 0 ,所以 SKIPIF 1 < 0 ,再根据x点的pM>0,即 SKIPIF 1 < 0 ,可得 SKIPIF 1 < 0 ,C正确;
D.若发生反应 SKIPIF 1 < 0 ,则该反应的 SKIPIF 1 < 0 ,根据线①与横坐标轴的交点可知pM=0,即 SKIPIF 1 < 0 时, SKIPIF 1 < 0 ,所以 SKIPIF 1 < 0 , SKIPIF 1 < 0 ,故沉淀不能完全溶解,D错误;
答案选D。
二、非选择题:本题共4小题,共55分。
16.(14分)
【答案】
(1)四或4 Ⅷ
(2)A
(3) SKIPIF 1 < 0
(4)将 SKIPIF 1 < 0 氧化为 SKIPIF 1 < 0 7.4
(5)盐酸或稀硫酸 将 SKIPIF 1 < 0 与 SKIPIF 1 < 0 分离,并富集 SKIPIF 1 < 0
(6) SKIPIF 1 < 0 或 SKIPIF 1 < 0 SKIPIF 1 < 0
【详解】
钕铁硼废料中主要成分为 SKIPIF 1 < 0 等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物,先用浓盐酸浸出,金属转化为相应的盐酸盐,过滤出不溶物,滤液中加入草酸沉钕,滤渣2是 SKIPIF 1 < 0 ,在空气中煅烧得到 SKIPIF 1 < 0 ;滤液中首先加入氧化剂把亚铁离子氧化为铁离子,利用试剂2调节pH沉淀铝离子和铁离子,过滤向滤液中加入有机萃取剂萃取C2+,然后加入盐酸或稀硫酸进行反萃取得到含C2+的溶液,加入碳酸氢铵沉钴,最后在空气中灼烧得到 SKIPIF 1 < 0 ,据此解答。
(1)钴( SKIPIF 1 < 0 )元素的原子序数是27,在元素周期表第四周期第Ⅷ族。
(2)矿物油污的主要成分是烃类,能溶于有机溶剂,所以除去矿物油污可以选择的试剂是苯。答案选A。
(3)“沉钕”过程调 SKIPIF 1 < 0 ,得到 SKIPIF 1 < 0 晶体,草酸难电离,则生成沉淀的离子方程式为 SKIPIF 1 < 0 。
(4)根据表中数据可知氢氧化亚铁完全沉淀的pH较大,所以“沉钕”后的滤液中加入试剂1的作用是将 SKIPIF 1 < 0 氧化为 SKIPIF 1 < 0 ;氢氧化钴完全沉淀的pH是9.4,则溶度积常数是10-5×(10-4.6)2=10-14.2,若溶液中 SKIPIF 1 < 0 ,则氢氧化钴开始沉淀时氢氧根浓度为10-6.6ml/L,相应的pH为7.4,即加入试剂2调节 SKIPIF 1 < 0 范围是6~7.4。
(5)“萃取”时发生反应: SKIPIF 1 < 0 ,即萃取后溶液显酸性,则反萃取时需要增大氢离子浓度,即试剂3为盐酸或稀硫酸,设计萃取、反萃取的目的是将 SKIPIF 1 < 0 与 SKIPIF 1 < 0 分离,并富集 SKIPIF 1 < 0 。
(6)①根据图甲中原子A的坐标为 SKIPIF 1 < 0 和B为 SKIPIF 1 < 0 ,以及C原子的位置可判断C原子的坐标为 SKIPIF 1 < 0 或 SKIPIF 1 < 0 。
②根据晶胞结构可判断晶胞含有O个数是 SKIPIF 1 < 0 ,C个数是 SKIPIF 1 < 0 ,若阿伏加德罗常数的值为 SKIPIF 1 < 0 ,晶胞质量是 SKIPIF 1 < 0 ,晶胞体积为abd×10-21cm3,则晶体密度为 SKIPIF 1 < 0 SKIPIF 1 < 0 。
17.(13分)
【答案】
(1) SKIPIF 1 < 0 小于
(2) SKIPIF 1 < 0 或 SKIPIF 1 < 0
(3) SKIPIF 1 < 0 ③ SKIPIF 1 < 0 SKIPIF 1 < 0
【详解】
(1) SKIPIF 1 < 0 SKIPIF 1 < 0 (CO2)+ SKIPIF 1 < 0 ( SKIPIF 1 < 0 ) - SKIPIF 1 < 0 (CO)- SKIPIF 1 < 0 ( SKIPIF 1 < 0 ) =[ SKIPIF 1 < 0 +0-( SKIPIF 1 < 0 SKIPIF 1 < 0 )] SKIPIF 1 < 0 = SKIPIF 1 < 0 ;该反应为放热反应,则正反应活化能小于逆反应活化能。
(2)根据盖斯定律,Ⅱ= SKIPIF 1 < 0 (Ⅲ-I), SKIPIF 1 < 0 , SKIPIF 1 < 0 ,则 SKIPIF 1 < 0 = SKIPIF 1 < 0 = SKIPIF 1 < 0 。
(3)达到平衡时, SKIPIF 1 < 0 , SKIPIF 1 < 0 ,则 SKIPIF 1 < 0 ;温度升高,正逆反应速率均增大,k正、k逆均增大,则lgk正、lgk逆与 SKIPIF 1 < 0 成反相关,由(1)分析知该反应正反应为放热反应,升高温度化学平衡逆向移动,逆反应速率增大幅度大于正反应速率增大幅度,则lgk正随 SKIPIF 1 < 0 变化的曲线为③;曲线③表示lgk正随 SKIPIF 1 < 0 的变化关系,曲线④表示lgk逆随 SKIPIF 1 < 0 的变化关系,温度T1时lgk正-lgk逆= SKIPIF 1 < 0 =a-0.3-a+1=0.7,则反应Ⅱ的平衡常数 SKIPIF 1 < 0 SKIPIF 1 < 0 =100.7=5。设 SKIPIF 1 < 0 和 SKIPIF 1 < 0 的物质的量均为1ml,
SKIPIF 1 < 0
SKIPIF 1 < 0
SKIPIF 1 < 0
平衡时CH4为1ml×(1-60%)=0.4ml,H2O为(1-y-2z) ml,CO2为(y+z-x) ml,CO为(2x-y) ml,H2为(2x+y+4z) ml,则 SKIPIF 1 < 0 ,解得 SKIPIF 1 < 0 ,即平衡时CH4为0.4ml,H2O为0.2 ml,CO2为0.2ml,CO为0.4 ml,H2为2 ml,总物质的量为3.2ml, SKIPIF 1 < 0 ; SKIPIF 1 < 0 。
18.(14分)
【答案】
(1)稀盐酸 胶头滴管
(2) 澄清石灰水 SKIPIF 1 < 0 具有较强的氧化性, SKIPIF 1 < 0 具有较强的还原性,因此,当放置时间较长时,二者之间发生氧化还原反应,导致溶液红色变浅或从氧气将 SKIPIF 1 < 0 氧化解释,合理即可
(3)1~2 若pH太小, SKIPIF 1 < 0 与 SKIPIF 1 < 0 结合生成HSCN;若pH太大, SKIPIF 1 < 0 水解程度增强,容易产生胶状氢氧化铁,甚至产生红褐色沉淀
(4) SKIPIF 1 < 0 向溶液中滴加KSCN溶液,溶液变为血红色,证明药片中有 SKIPIF 1 < 0 ;向血红色溶液中慢慢滴加KF溶液,至溶液刚好褪色,然后滴加少量氯水(或稀硝酸),若裉色后的溶液又变为红色
【详解】
(1)由于 SKIPIF 1 < 0 易水解,应该将 SKIPIF 1 < 0 溶解在稀盐酸中再配制溶液,抑制 SKIPIF 1 < 0 水解;配制一定物质的量浓度的溶液的过程中,在定容时需要用到胶头滴管;
(2)①由抗坏血酸和脱氢抗坏血酸的结构可知,抗坏血酸与 SKIPIF 1 < 0 发生氧化还原反应生成脱氢抗坏血酸,根据得失电子守恒、质量守恒和电荷守恒可得反应的离子方程式: ;
②加入 SKIPIF 1 < 0 溶液产生了 SKIPIF 1 < 0 ,说明 SKIPIF 1 < 0 在此过程中作氧化剂,将 SKIPIF 1 < 0 氧化,另一种气体由于无色、无味、无毒,只能是 SKIPIF 1 < 0 , SKIPIF 1 < 0 可以用澄清石灰水检验;
③通过a、b实验的分析可知, SKIPIF 1 < 0 具有较强的氧化性, SKIPIF 1 < 0 具有较强的还原性,因此,当放置时间较长时,二者之间发生氧化还原反应,导致溶液红色逐渐褪去;还可能是空气中的氧气将 SKIPIF 1 < 0 氧化而导致溶液褪色;
(3)由图乙可以看出,溶液的pH为12时,吸光度(A)较大且数据稳定,所以进行该显色反应时应控制pH为1~2;若pH太小, SKIPIF 1 < 0 与 SKIPIF 1 < 0 结合生成HSCN,若pH太大, SKIPIF 1 < 0 的水解程度增强,容易产生胶状氢氧化铁,甚至产生红褐色沉淀;
(4)①由题给信息可知, SKIPIF 1 < 0 、
SKIPIF 1 < 0 , SKIPIF 1 < 0 ,
则 SKIPIF 1 < 0 的平衡常数 SKIPIF 1 < 0 ,②由①中分析可知, SKIPIF 1 < 0 很容易在 SKIPIF 1 < 0 存在时转化为 SKIPIF 1 < 0 ,即向 SKIPIF 1 < 0 溶液中慢慢滴加含 SKIPIF 1 < 0 的溶液,由于 SKIPIF 1 < 0 转化为 SKIPIF 1 < 0 导致溶液红色慢慢褪去,据此可以设计出证明药片部分变质的方案为:向溶液中滴加KSCN溶液,溶液变为血红色,证明药片中有 SKIPIF 1 < 0 ;向血红色溶液中慢慢滴加KF溶液,至溶液刚好褪色,然后滴加少量氯水(或稀硝酸),若裉色后的溶液又变为红色。
19.(14分)
【答案】
(1)取代反应 保护羟基,防止被氧化
(2)硝基
(3)B
(4)分子中的羟基、羧基能与水形成氢键
(5)6
(6) SKIPIF 1 < 0 SKIPIF 1 < 0
【详解】
由条件I可知,A为。
(1)A→B,-CH2Cl取代了-OH中的H,故反应类型为取代反应;D→E将-OCH2Cl转化为-OH,由A→B、D→E两个过程可知,该反应的目的是保护羟基,防止被氧化;
(2)C→D的过程中,被还原的官能团是硝基;
(3)A.由A结构可知,A的名称是2,6-二羟基苯甲酸乙酯,A项正确;
B.化合物B官能团为醚键、酯基,含2种不同官能团,B项错误;
C.化合物E含有官能团-COOH、-NH2,故既有酸性又有碱性,C项正确;
D.F中官能团为酚羟基、羧基,G中官能团为羰基、醚键、酚羟基,能与 SKIPIF 1 < 0 反应的只有羧基,故与 SKIPIF 1 < 0 溶液混合产生气泡的是F, SKIPIF 1 < 0 溶液可以鉴别F和G,D项正确;
答案选B;
(4)根据F结构,化合物F易溶于水,主要原因是分子中的羟基、羧基能与水形成氢键;
(5)符合条件的化合物E的同分异构体中,苯环上含1个-CONH2、3个-OH,中-CONH2位置有3种,中-CONH2位置有2种,中-CONH2位置有1种,共有2+3+1=6种;F→G,F的-COOH与苯环上6号碳的-OH参加反应,过程失去2个H2O,副产物H与化合物G互为同分异构体,故F→H,应为F的-COOH与苯环上2号碳的-OH参加反应,H的结构简式为;
(6)根据题中合成原理,及苯酚为原料合成呫吨酮路线为 SKIPIF 1 < 0 SKIPIF 1 < 0 。
新高考化学模拟试卷20(原卷版+教师版): 这是一份新高考化学模拟试卷20(原卷版+教师版),共16页。试卷主要包含了本试卷分第Ⅰ卷两部分等内容,欢迎下载使用。
新高考化学模拟试卷15(原卷版+教师版): 这是一份新高考化学模拟试卷15(原卷版+教师版),共11页。试卷主要包含了选择题的作答,非选择题的作答,酸在生产、实验中有广泛应用等内容,欢迎下载使用。
新高考化学模拟试卷14(原卷版+教师版): 这是一份新高考化学模拟试卷14(原卷版+教师版),共11页。试卷主要包含了选择题的作答,非选择题的作答,盐在生产、生活中有广泛应用等内容,欢迎下载使用。












