

所属成套资源:新高考化学二轮复习学案 (含解析)
新高考化学二轮复习学案第1部分 专题突破 专题16 溶液中的三大平衡及应用(含解析)
展开
这是一份新高考化学二轮复习学案第1部分 专题突破 专题16 溶液中的三大平衡及应用(含解析),共13页。
正误判断,正确的打“√”,错误的打“×”
(1)常温下,pH为2的盐酸由H2O电离出的c(H+)=1.0×10-12 ml·L-1( √ )
(2)同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7( × )
(3)室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7( × )
(4)25 ℃时,等体积、等浓度的硝酸与氨水混合后,溶液pH=7( × )
(5)用热的纯碱溶液洗去油污,是因为Na2CO3可直接与油污反应( × )
(6)NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同( × )
(7)施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合施用,是因为K2CO3与NH4Cl反应生成氨气,会降低肥效( √ )
(8)向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成,则Ksp(AgCl)>Ksp(AgI)( × )
(9)常温下,Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+的溶液中,c(Mg2+)≤5.6×10-4 ml·
L-1( √ )
(10)室温下,向浓度均为0.1 ml·L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀,所以Ksp(BaSO4)<Ksp(CaSO4)( × )
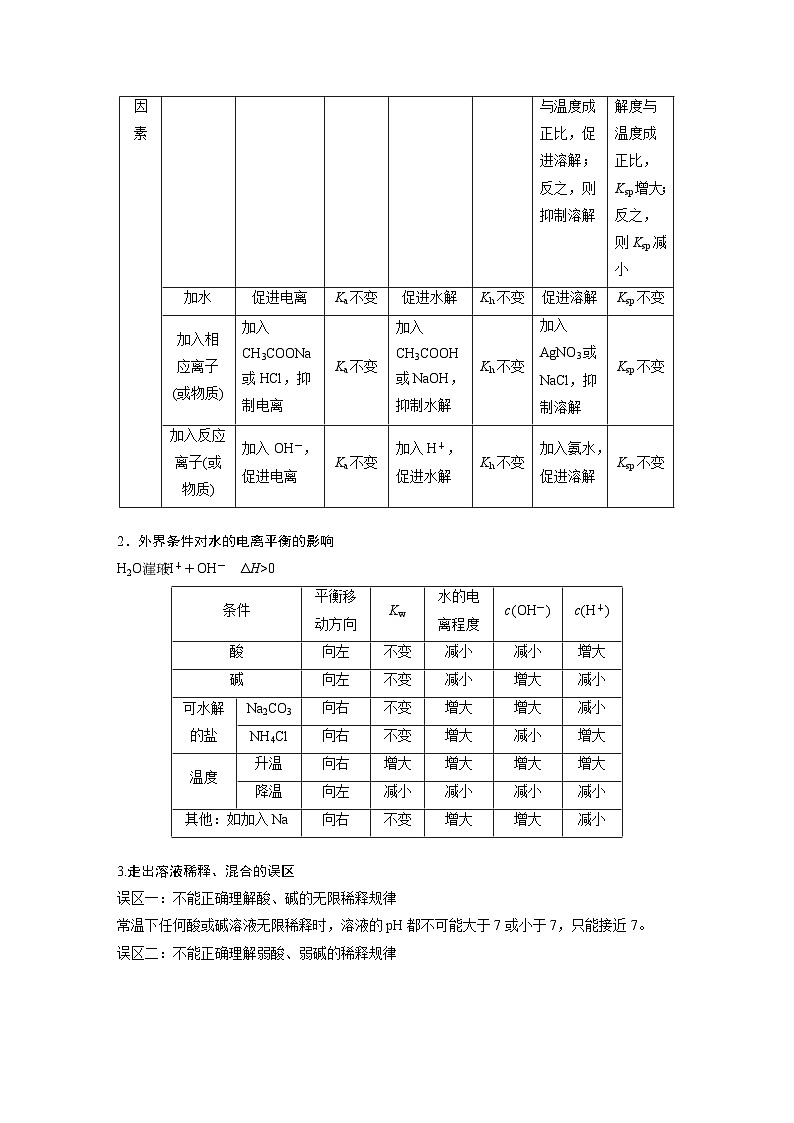
1.对比剖析“三大”平衡
2.外界条件对水的电离平衡的影响
H2OH++OH- ΔH>0
3.走出溶液稀释、混合的误区
误区一:不能正确理解酸、碱的无限稀释规律
常温下任何酸或碱溶液无限稀释时,溶液的pH都不可能大于7或小于7,只能接近7。
误区二:不能正确理解弱酸、弱碱的稀释规律
误区三:不能正确掌握混合溶液的定性规律
常温下,pH=n(n
相关学案
这是一份新高考化学二轮复习学案第1部分 专题突破 专题18 溶液的配制与滴定法的应用(含解析),共19页。
这是一份新高考化学二轮复习学案第1部分 专题突破 专题15 速率常数、平衡常数的分析应用(含解析),共23页。
这是一份新高考化学二轮复习学案第1部分 专题突破 专题14 化学反应速率与化学平衡归因分析(含解析),共21页。









