

广东省江门市第一中学2023-2024学年高二上学期10月第一次段考化学试题(含答案)
展开
这是一份广东省江门市第一中学2023-2024学年高二上学期10月第一次段考化学试题(含答案),共12页。试卷主要包含了白磷与氧可发生如下反应,下列说法正确的是,下列有关化学用语表示正确的是等内容,欢迎下载使用。
本试卷共8页,20小题,满分100分,考试时间75分钟。
相对原子质量:H:1C:12N:14
注意事项:
1.答题前,考生务必用黑色笔迹的钢笔或签字笔将自己的姓名、考号填写在答题卷上。
2.每小题选出答案后,用2B铅笔把答题卷上对应题目选项的答案信息点涂黑;非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
3.作答选做题时,请先用2B铅笔填涂选做题的题组号对应的信息点,再作答。漏涂、错涂、多涂的,答案无效。
第一部分选择题(共44分)
一、单项选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。每小题只有一个选项符合题意。
1.中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如下图所示。下列说法不正确的是
A.整个过程实现了光能向化学能的转换
B.过程II有O-O单键生成并放出能量
C.过程III发生的化学反应为:
D.整个过程的总反应方程式为:
2.叔丁基溴在稀的碱性水溶液中水解生成叔丁醇的反应分三步进行,反应中每一步的能量变化曲线如图所示,下列有关说法不正确的是
A.叔丁基溴在稀的碱性水溶液中生成叔丁醇的反应是放热反应
B. 和(CH3)3C-OH2为反应活性中间体
C.决定叔丁基溴水解生成叔丁醇反应的速率的是第二步反应
D.第三步反应为
3.在1200℃时,天然气脱硫工艺中会发生下列反应
①
②
③
④
则△H4的正确表达式为()
A. B.
C. D.
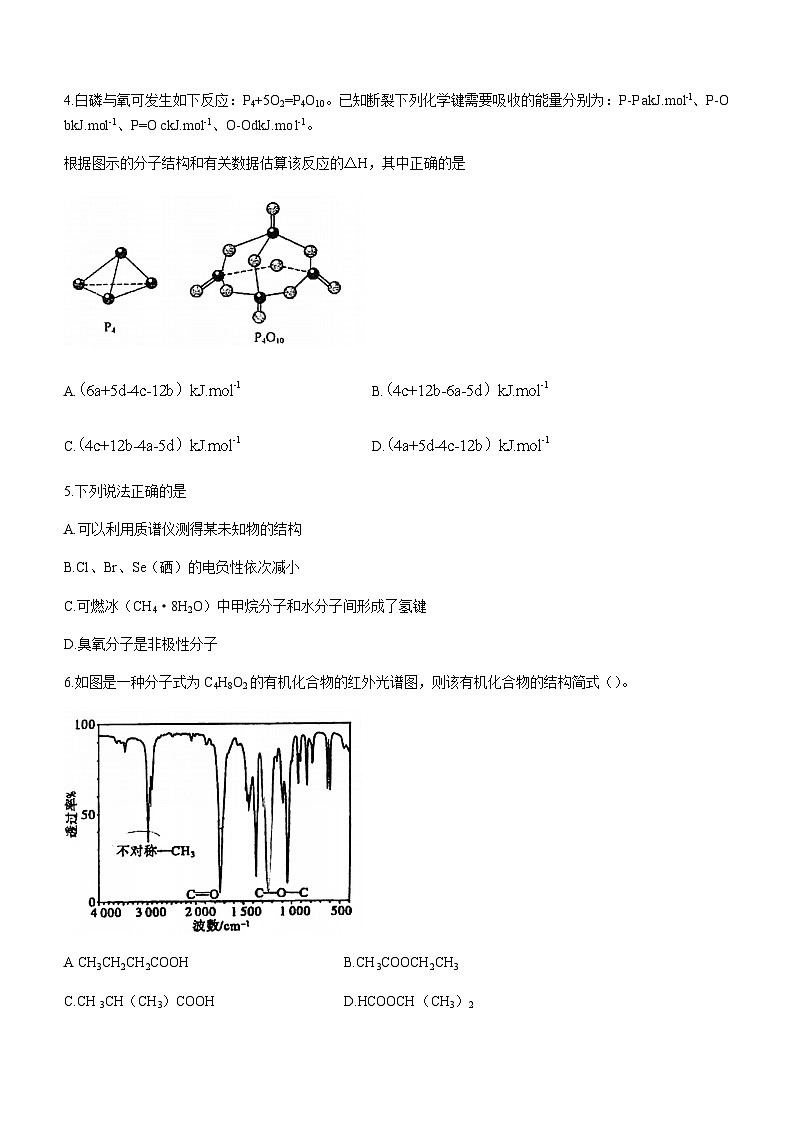
4.白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P akJ.ml-l、P-O bkJ.ml-1、P=O ckJ.ml-1、O-OdkJ.m1-1。
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
A.B.
C.D.
5.下列说法正确的是
A.可以利用质谱仪测得某未知物的结构
B.Cl、Br、Se(硒)的电负性依次减小
C.可燃冰(CH4·8H2O)中甲烷分子和水分子间形成了氢键
D.臭氧分子是非极性分子
6.如图是一种分子式为C4H8O2的有机化合物的红外光谱图,则该有机化合物的结构简式()。
A CH3CH2CH2COOHB.CH3COOCH2CH3
C.CH 3CH(CH3)COOHD.HCOOCH(CH3)2
7.下列关于C、Si及其化合物结构与性质的论述不正确的是
A.键能:C-C>Si-Si、C-H>Si-H,因此C2H6稳定性大于Si2H6
B.立方型SiC是与金刚石成键、结构均相似的晶体,因此具有很高的硬度
C.SiH4中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH4
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成p-Pπ键
8.下列有关化学用语表示正确的是()
A.空间填充模型可以表示二氧化碳分子,也可以表示水分子
B.用电子式表示MgCl2的形成过程:
C.Cl-Cl的p-pσ键电子云图形:
D.基态Cr原子的价层电子轨道表示式:
9.有X、Y两种活性反应中间体微粒,均含有1个碳原子和3个氢原子,其球棍模型如图所示:下列说法错误的是
A.X的组成为CH3+B.Y的组成为CH3-
C.X的价层电子对数为3D.Y中键角大于120°
10.动力电池赛道又跳出来一个竞争者“锑电池”。锑(51Sb)与砷(33As)属于同主族元素,下列关于锑元素说法正确的是
A.可能是半导体材料B.属于第四周期元素
C.最高正化合价为+3D.得电子能力比As的强
11.关于下表所列四种粒子的各项描述完全正确的选项是()
12.己知某些元素在周期表中的位置如图所示,下列说法错误的是
A.元素②和⑤位于同一区
B.元素③的基态原子中,未成对电子数为5
C.与元素④具有相同最外层电子数的元素只可能处于s区
D.s区(除元素①外)、d区和ds区的元素都是金属元素
13.现有三种元素的基态原子的电子排布式如下
①1s22s22p63s23p4②1s22s22p63s23p3③1s22s22p63s23p5,下列排序正确的是
A.第一电离能:③>①>②B.原子半径:③>②>①
C.含氧酸的酸性:③>①>②D.电负性:③>②>①
14.化合物XYZ4ME4可作肥料,所含的5种元素位于主族在每个短周期均有分布,仅有Y和M同挨。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为nsn-1,X与M同周期,E在地壳中含量最多。下列说法正确的是
A.元素电负性:E>Y>ZB.氢化物沸点:M>Y>E
C.第一电离能:X>E>YD.YZ3和YE3-的空间结构均为三角锥形
15.LiAlH4是重要的还原剂与储氢材料,。在120°C下的干燥空气中相对稳定,其合成方法为:下列说法正确的是
A.该反应可以在水溶液中进行
B.基态锂原子的电子排布式为1s22s1,核外电子的空间运动状态有2种
C.LiAlH4中A1原子采用sp3杂化,AlH4-离子的空间构型为正方形
D.上述所有物质中电负性最大的元素与电负性最小的元素形成的化合物,其电子式为Na+[:H]-
16.通过以下反应均可获取H2。下列有关说法正确的是()
①太阳光催化分解水制氢:
②焦炭与水反应制氢:
③甲烷与水反应制氢:
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,△H3减小
D.反应的△H=+
第二部分非选择题(56分)
17.(12分)根据物质结构和性质的知识,回答下列问题:
(1)下列物质中既有极性键,又有非极性键的极性分子是_______________。(填选项ABCD)
A.SO2B.SOC.H2O2D.C2H4
(2)某同学画出基态碳原子的核外电子排布图:,该电子排布图违背了_______________。
(3)BCl3在四氯化碳中的溶解度远大于HC1,原因是_______________。
④NH4H2PO4中,电负性最高的元素是_______________;P的_______________杂化轨道与O的2p轨道形成______________(填“σ”或“π”)键。
(5)有机物中,有_______________个手性碳,1ml该有机物含σ键的物质的量为_______________ml。
(6)可以用pKa(pKa=-1gKa)来衡量酸性的强弱,下表是部分酸的pKa数据:
从表中数据可知,酸性:ClCH2COOHA>B(1分)
(9)sp2(1分)sp3(1分)
C-F键的键能大于聚乙烯中C-H的键能,键能越大,化学性质越稳定(1分)
19.(共10分)
(1)第五周期B族;(1分)B(1分)
(2)H2S(1分)(SeO2)n(1分)
(3)sp3a(各1分)
(4)3d6(1分)SO42-的键角大于H2O,(1分)SO42-中S原子的价层电子对数为4、孤对电子对数为0,离子的空间构型为正四面体形,H2O分子中O原子的价层电子对数为4、孤对电子对数为2,分子的空间构型为V形(2分)
20.(14分)(除标注外,每空2分)I.(1)
(2)反应生成的物质是N2和H2O,对环境无污染
(3)玻璃搅拌器(1分)量筒(1分)
(4)①4.0②-53.5kJ/ml③acd
(5)不相等(1分)相等(1分)选项
A
B
C
D
分子或离子的化学式
ClO3
NO2-
H2F+
BH4-
中心原子的杂化轨道类型
sp3
sp2
sp
sp3
VSEPR模型名称
四面体形
平面三角形
直线形
正四面体形
分子或离子的空间结构名称
三角锥形
平面三角形
V形
三角维形
ClCH2COOH
Cl2CHCOOH
CCl3COOH
H2SO3
pKa(室温)
2.86
1.29
0.65
pKa1=1.9、pKa2=7.5
温度
实验次数
起始温度t1/℃
终止温度/℃
温度差平均值(t2-t1)/℃
H2SO4
NaOH
平均值
1
26.2
26.0
26.1
30.1
_
2
27.0
27.4
27.2
33.3
3
25.9
25.9
25.9
29.8
4
26.4
26.2
26.3
30.4
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
C
C
A
A
B
B
C
C
D
A
A
C
A
A
B
D
相关试卷
这是一份广东省江门市第一中学2023-2024学年高二上学期11月第二次段考化学(选考)试题含答案,共13页。试卷主要包含了如右图所示,曲线a表示放热反应,一定条件下,将,下列说法中正确的是等内容,欢迎下载使用。
这是一份广东省江门市鹤山市第一中学2023-2024学年高二上学期第二阶段考试化学试题含答案,共12页。试卷主要包含了12,4kJ/ml,则含20, 下列有关说法不正确的是,3的NaHCO3溶液等内容,欢迎下载使用。
这是一份广东省江门市新会第一中学2023-2024学年高二上学期期末考试化学试题,共7页。








