

所属成套资源:新教材适用2023_2024学年高中化学新人教版必修第一册课时作业(37份)
- 新教材适用2023_2024学年高中化学第3章铁金属材料检测试卷新人教版必修第一册 试卷 0 次下载
- 新教材适用2023_2024学年高中化学第3章铁金属材料第1节铁及其化合物第1课时铁的单质氧化物氢氧化物课时作业新人教版必修第一册 试卷 0 次下载
- 新教材适用2023_2024学年高中化学第3章铁金属材料第1节铁及其化合物第3课时铁及其化合物复习课课时作业新人教版必修第一册 试卷 0 次下载
- 新教材适用2023_2024学年高中化学第3章铁金属材料第2节金属材料第1课时铁合金铝和铝合金新型合金课时作业新人教版必修第一册 试卷 0 次下载
- 新教材适用2023_2024学年高中化学第3章铁金属材料第2节金属材料第2课时物质的量在化学方程式计算中的应用课时作业新人教版必修第一册 试卷 0 次下载
高中化学第一节 铁及其化合物第2课时同步练习题
展开
这是一份高中化学第一节 铁及其化合物第2课时同步练习题,共6页。试卷主要包含了下列除杂的操作正确的是等内容,欢迎下载使用。
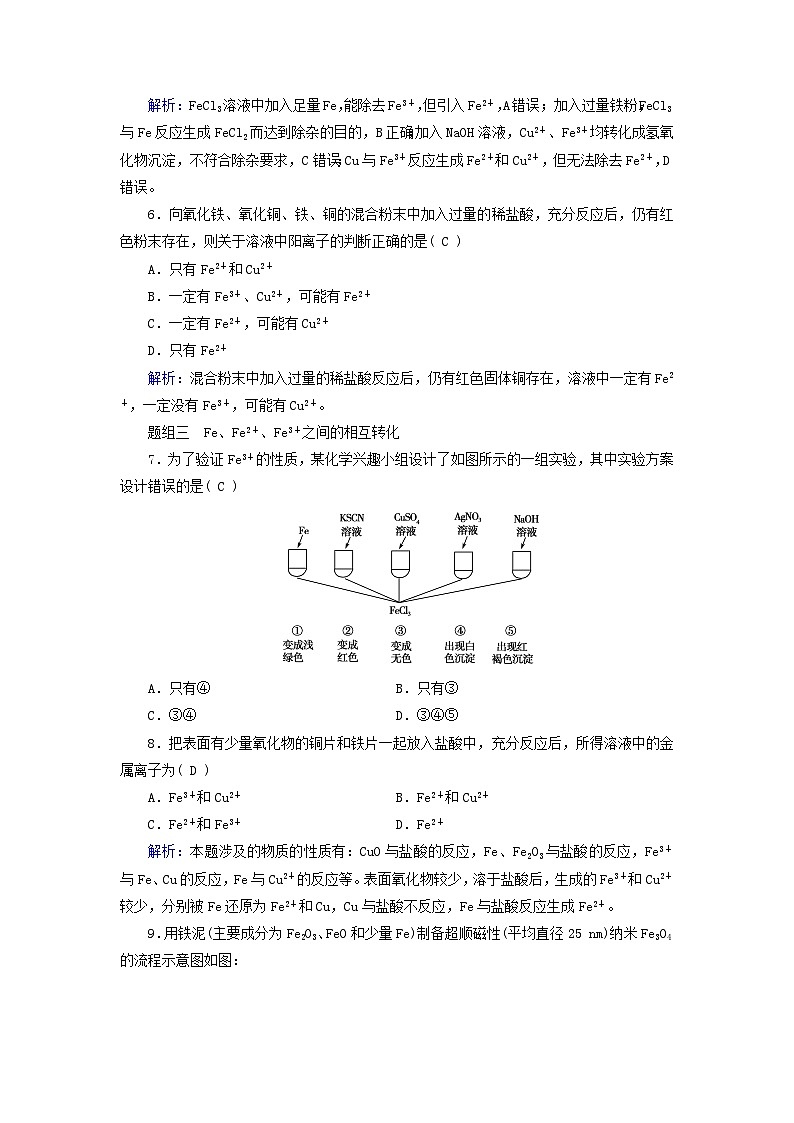
第三章 第一节 第2课时对点训练题组一 铁盐、亚铁盐的性质1.在下列有FeCl3溶液参加的反应中,与Fe3+的氧化性无关的是( C )A.FeCl3与Fe反应B.FeCl3使淀粉KI溶液变蓝C.FeCl3滴入沸水中制得Fe(OH)3胶体D.FeCl3用于腐蚀电路板解析:A、B、D中Fe3+分别将Fe、I-、Cu氧化为Fe2+、I2和Cu2+,表现氧化性;C的离子方程式为Fe3++3H2OFe(OH)3(胶体)+3H+,Fe3+的化合价没有变化,没有表现氧化性。2.下列实验设计及其对应的离子方程式均正确的是( B )A.把铁片插入CuSO4溶液中,验证古代湿法冶铜:2Fe+3Cu2+===2Fe3++3CuB.某溶液中滴入KSCN溶液显红色,说明含Fe3+:Fe3++3SCN-===Fe(SCN)3C.FeCl3溶液中加入铜粉:Fe3++Cu===Fe2++Cu2+D.若要求用两种单质和一种溶液来测定Zn、Cu、Ag三种金属的活动性顺序,可用Zn、Cu和AgNO3溶液反应:Zn+2Ag+===Zn2++2Ag3.除去FeCl2溶液中少量的FeCl3,最好的办法是( D )A.加入氢氧化钠溶液 B.通入氯气C.加入铜粉 D.加入铁粉题组二 Fe2+、Fe3+的检验和除杂4.检验硫酸亚铁中是否含有少量硫酸铁,选用的最佳试剂是( C )A.NaOH B.KMnO4C.KSCN D.氯水解析:亚铁离子遇KSCN溶液不显红色,铁离子遇KSCN溶液显红色,KSCN是检验是否含硫酸铁的最佳试剂。5.下列除杂的操作正确的是( B )A.MgCl2溶液中混有少量FeCl3:加入足量Fe充分反应后过滤B.FeCl2溶液中混有少量FeCl3:加入过量铁粉充分反应后过滤C.CuCl2溶液中混有少量FeCl3:加入NaOH溶液充分反应后过滤D.CuCl2溶液中混有少量FeCl3:先加入过量Cu粉将Fe3+还原成Fe2+,再过滤解析:FeCl3溶液中加入足量Fe,能除去Fe3+,但引入Fe2+,A错误;加入过量铁粉,FeCl3与Fe反应生成FeCl2而达到除杂的目的,B正确;加入NaOH溶液,Cu2+、Fe3+均转化成氢氧化物沉淀,不符合除杂要求,C错误;Cu与Fe3+反应生成Fe2+和Cu2+,但无法除去Fe2+,D错误。6.向氧化铁、氧化铜、铁、铜的混合粉末中加入过量的稀盐酸,充分反应后,仍有红色粉末存在,则关于溶液中阳离子的判断正确的是( C )A.只有Fe2+和Cu2+B.一定有Fe3+、Cu2+,可能有Fe2+C.一定有Fe2+,可能有Cu2+D.只有Fe2+解析:混合粉末中加入过量的稀盐酸反应后,仍有红色固体铜存在,溶液中一定有Fe2+,一定没有Fe3+,可能有Cu2+。题组三 Fe、Fe2+、Fe3+之间的相互转化7.为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计错误的是( C )A.只有④ B.只有③C.③④ D.③④⑤8.把表面有少量氧化物的铜片和铁片一起放入盐酸中,充分反应后,所得溶液中的金属离子为( D )A.Fe3+和Cu2+ B.Fe2+和Cu2+C.Fe2+和Fe3+ D.Fe2+解析:本题涉及的物质的性质有:CuO与盐酸的反应,Fe、Fe2O3与盐酸的反应,Fe3+与Fe、Cu的反应,Fe与Cu2+的反应等。表面氧化物较少,溶于盐酸后,生成的Fe3+和Cu2+较少,分别被Fe还原为Fe2+和Cu,Cu与盐酸不反应,Fe与盐酸反应生成Fe2+。9.用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备超顺磁性(平均直径25 nm)纳米Fe3O4的流程示意图如图:下列叙述不正确的是( D )A.可以用KSCN溶液检验滤液B中是否有Fe3+B.步骤②中,主要反应的离子方程式是2Fe3++Fe===3Fe2+C.步骤④中,反应完成后剩余的H2O2必需除去D.纳米Fe3O4属于胶体解析:根据题意可知,滤液B的溶质为氯化亚铁,可以用KSCN溶液检验滤液B中是否有Fe3+,故A正确;滤液A的溶质为氯化铁、氯化亚铁、过量的稀盐酸,加入铁粉还原铁离子和反应过量的盐酸,主要反应的离子方程式:2Fe3++Fe===3Fe2+,故B正确;步骤④中,防止其在步骤⑤中继续氧化+2价铁元素,反应完成后需再加热一段时间除去剩余H2O2,故C正确;Fe3O4粒子分散在水中,可形成胶体,但Fe3O4不能称为胶体,故D错误。 综合强化10.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( D )选项操作、现象解释A向KI-淀粉溶液中加入FeCl3溶液,溶液变蓝Fe3+能与淀粉发生显色反应B把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点铁在潮湿的空气中易生成Fe(OH)3C向盐酸中加入少量铁粉,有气泡产生说明Fe被氧化为Fe3+D新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色说明Fe(OH)2易被O2氧化成Fe(OH)3解析: A项中Fe3+将I-氧化为I2,淀粉遇碘单质变蓝;B项中红棕色斑点是Fe2O3;C项中铁与盐酸反应生成Fe2+。11.根据不同价态铁元素之间的相互转化关系,回答下列问题:(1)配制含Fe2+的溶液时,常常向溶液中加入少量_铁粉__,将被氧气氧化生成的Fe3+还原为Fe2+。(2)为除去废水中的Fe2+,常先将废水中的Fe2+氧化为_Fe3+__,再根据Fe3+的性质使Fe3+转化为红褐色的_Fe(OH)3__沉淀析出。(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为 Cu+2Fe3+===Cu2++2Fe2+ 。(4)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为 Cl2+2Fe2+===2Fe3++2Cl- ; Fe+2Fe3+===3Fe2+ ;处理过程中需定期添加的原料是_铁粉__。解析:(1)配制含Fe2+的溶液时,需利用还原剂防止亚铁离子被氧化,且不能引入新杂质,则加入铁粉(或铁钉)防止Fe2+被氧化。(2)为除去废水中的Fe2+,常先将废水中的Fe2+氧化为铁离子,铁离子极易转化为氢氧化铁沉淀。(3)FeCl3溶液与金属铜反应的化学方程式为2FeCl3+Cu===2FeCl2+CuCl2,离子方程式为Cu+2Fe3+===Cu2++2Fe2+。(4)Cl2与FeCl2溶液反应生成FeCl3,其反应的化学方程式为2FeCl2+Cl2===2FeCl3,离子方程式为Cl2+2Fe2+===2Fe3++2Cl-,铁粉与FeCl3反应生成FeCl2,其反应的化学方程式为2FeCl3+Fe===3FeCl2,离子方程式为Fe+2Fe3+===3Fe2+,根据两个反应可知,处理过程中消耗的原料是铁粉。12.下图是某儿童微量元素体检报告单的部分数据:北京市医疗机构临床检验结果报告单 分析项目检测结果单位参考范围1.锌(Zn)115.95μ mol·L-166~1202.铁(Fe)6.95m mol·L-17.52~11.823.钙(Ca)1.68m mol·L-11.55~2.10根据上表的数据,回答下列问题:(1)该儿童_铁__元素含量偏低。(2)报告单中“μ mol·L-1”是_浓度__(填“质量”“体积”或“浓度”)的单位。(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的_还原性__(填“氧化性”或“还原性”)。(4)缺铁性贫血患者应补充Fe2+。一些补铁剂以硫酸亚铁为主要成分,将硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是_防止Fe2+被氧化__。解析:(1)从检测结果与参考范围看, 该儿童铁元素的含量比参考范围略低。(2)μ mol·L-1为浓度的单位。(3)Fe3+转化为Fe2+,铁元素的化合价降低,发生还原反应,故维生素C体现还原性。(4)糖衣可以防止硫酸亚铁与空气接触,起到防止Fe2+被氧化的作用。13.某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知SCN-、Fe2+能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,并结合已学的知识设计了如下实验:①将药片除去糖衣研细后溶解、过滤。②取滤液分别加入两支试管中,在一支试管中加入酸性KMnO4溶液,在另一支试管中加入KSCN溶液。请完成下列问题:(1)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液后不变红,结论是_补铁药没有变质__。(2)若滴入酸性KMnO4溶液后不褪色,滴入KSCN溶液变红,结论是_补铁药完全变质__。(3)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液变红,结论是_补铁药部分变质__。(4)_不能__(填“能”或“不能”)将酸性KMnO4溶液和KSCN溶液滴入到同一支试管中进行验证,原因是_酸性KMnO4溶液呈紫红色,影响Fe3+的检验;KSCN具有还原性,影响Fe2+的检验__。解析:加入酸性KMnO4溶液褪色说明含有Fe2+,而加入KSCN溶液变红则说明含有Fe3+,所以前三问的答案很容易得出。第(4)问中的原因可归纳为两条,一是酸性KMnO4溶液呈紫红色,影响Fe3+的检验;二是KSCN具有还原性,可以被酸性KMnO4溶液氧化,影响Fe2+的检验。14.金属及其化合物在人类生活、生产中发挥着重要的作用。印刷电路板由高分子材料和铜箔复合而成,刻制印刷电路时,工业上常用FeCl3溶液作为“腐蚀液”,有CuCl2和FeCl2生成。如图是某工程师为了从使用过的腐蚀废液中回收铜并重新获得FeCl3溶液所采用的工艺流程图:请回答下列问题。(1)实验室中,检验溶液中存在Fe3+的试剂是_KSCN溶液__,证明Fe3+存在的现象是_溶液变成红色__。(2)写出FeCl3溶液与金属铜发生反应的离子方程式: 2Fe3++Cu===2Fe2++Cu2+ 。(3)写出上述流程图中加入或生成的有关物质的化学式:①_Fe__,②_FeCl2__,④_HCl__。(4)含有②的滤液与⑤反应的化学方程式为 2FeCl2+Cl2===2FeCl3 。解析:废液中含有FeCl2、CuCl2、FeCl3,向废液中加入过量Fe,发生的离子反应为2Fe3++Fe===3Fe2+、Cu2++Fe===Fe2++Cu,然后过滤,滤液中含有FeCl2,滤渣中含有Cu、Fe,向滤渣中加入过量盐酸,Fe溶解,Cu不溶解,然后过滤得到金属单质Cu,滤液中含有FeCl2,向含有FeCl2的滤液中通入过量Cl2,发生的离子反应为2Fe2++Cl2===2Fe3++2Cl-,从而得到FeCl3溶液。(1)Fe3+和KSCN溶液混合生成络合物硫氰化铁而使溶液呈红色,可以用KSCN溶液检验Fe3+。(2)氯化铁具有氧化性,能氧化Cu生成铜离子,自身被还原生成氯化亚铁,离子反应方程式为2Fe3++Cu===2Fe2++Cu2+。(3)通过以上分析知,①②④分别是Fe、FeCl2、HCl。(4)FeCl2与Cl2发生氧化还原反应生成FeCl3,化学方程式为2FeCl2+Cl2===2FeCl3。
相关试卷
这是一份人教版 (2019)必修 第一册第一节 铁及其化合物第2课时测试题,共7页。试卷主要包含了下列物质常温下不能与铁反应的是,下列离子的检验方法中合理的是等内容,欢迎下载使用。
这是一份高中第一节 铁及其化合物第2课时课后作业题,共7页。试卷主要包含了选择合适试剂完成甲、乙两组实验等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第一节 铁及其化合物达标测试,共7页。试卷主要包含了下列离子的检验方法中合理的是等内容,欢迎下载使用。









