




所属成套资源:【名校真题】各省名校高三上学期期中化学试题
【期中真题】天津市八校联考2022-2023学年高三上学期期中考试化学试题.zip
展开
这是一份【期中真题】天津市八校联考2022-2023学年高三上学期期中考试化学试题.zip,文件包含期中真题天津市八校联考2022-2023学年高三上学期期中考试化学试题原卷版docx、期中真题天津市八校联考2022-2023学年高三上学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
2022-2023学年度第一学期期中宝坻区八校联考试题
高三化学学科
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
第I卷(选择题共36分)
一、选择题(本题共12小题,每小题3分,共36分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1. 2022年9月17日,航天员蔡旭哲、陈冬从问天实验舱成功出舱,两名出舱航天员相互配合开展舱外助力手柄安装等作业。下列说法正确的是
A. 舱外助力手柄由合金制成,该手柄材料属于化合物
B. 问天实验舱使用了石墨烯导热索技术,石墨烯属于新型无机非金属材料
C. 问天实验舱上的太阳能电池板主要材料是高纯度二氧化硅
D. 轻质纳米真空绝热板应用于舱内低温实验保冷设备,该绝热板为胶体
【答案】B
【解析】
【详解】A.合金是混合物,不是化合物,A错误;
B.石墨烯是由碳元素形成的碳单质,属于新型无机非金属材料,B正确;
C.太阳能电池板的主要材料为晶体硅而不是二氧化硅,C错误;
D.轻质纳米真空绝热板不属于胶体,D错误;
故答案选B。
2. 下列化学用语或图示表达正确的是
A. N2的结构式:N≡N
B. 中子数为19的硫原子:S
C. 基态氮原子价电子的轨道表示式:
D. CO2的电子式:
【答案】A
【解析】
【详解】A.结构式是指用一根“—”表示一对共用电子的式子,故N2的结构式为:N≡N,A正确;
B.质量数等于质子数加中子数,故中子数为19的硫原子表示为:S,B错误;
C.根据洪特规则可知,当电子进入同一能级不同轨道时总是优先进入不同的轨道且自旋方向相同,故基态氮原子价电子的轨道表示式为:,C错误;
D.CO2的电子式为:,D错误;
故答案为:A。
3. 分类是科学研究的重要方法,下列物质分类正确的是
A. H2、D2、T2互为同位素
B. 同素异形体:臭氧、氧气、O
C. 非电解质:乙醇、二氧化碳、SO3、葡萄糖
D. 化合物:冰水混合物、烧碱、75%医用酒精、石膏
【答案】C
【解析】
【详解】A.同位素是指质子数相同而中子数不同的同一元素不同原子的互称,选项中各物质是分子,A错误;
B.同素异形体一定是单质,不是单质,B错误;
C.非电解质是指在水溶液中和熔化状态下都不能导电的化合物,选项中的物质都属于非电解质,C正确;
D.75%医用酒精属于混合物并不是化合物,D错误;
故答案选C。
4. 常温下,下列各组离子在指定溶液中能大量共存的是
A. 中性溶液中:Al3+、Fe3+、SO、ClO
B. 加入铝粉生成H2的溶液中:Na+、HCO、NO、NH
C. 无色溶液中:K+、SO、MnO、Na+
D. pH=1的溶液中:NH、Ca2+、Cl-、NO
【答案】D
【解析】
【详解】A.Al3+、Fe3+水解呈酸性不可能呈中性,A不符合;
B.加入铝粉生成H2,溶液既可以显酸性也可以显碱性,在酸性和碱性条件下都不共存,在碱性条件下不共存,B不符合;
C.在溶液中显紫色,C不符合;
D.pH=1溶液显酸性,离子之间不发生反应,D符合;
故答案为:D。
5. 下列说法中正确的是
A. HCl的形成过程为
B. 全部由非金属元素组成的化合物一定是共价化合物
C. 共价化合物H2O2只含共价键,离子化合物Na2O2只含离子键
D. H2O的沸点高于H2S的沸点
【答案】D
【解析】
【详解】A.HCl是共价化合物,HCl的电子式书写错误,HCl的形成过程为,A错误;
B.全部由非金属元素组成的化合物不一定是共价化合物,比如NH4Cl,是离子化合物,B错误;
C.共价化合物H2O2只含共价键,离子化合物Na2O2含有离子键和共价键,C错误;
D.H2O和H2S都是分子晶体,相对分子质量越大,分子晶体的沸点越高,但是H2O分子间存在氢键,使得H2O的沸点高于H2S,D正确;
故选D
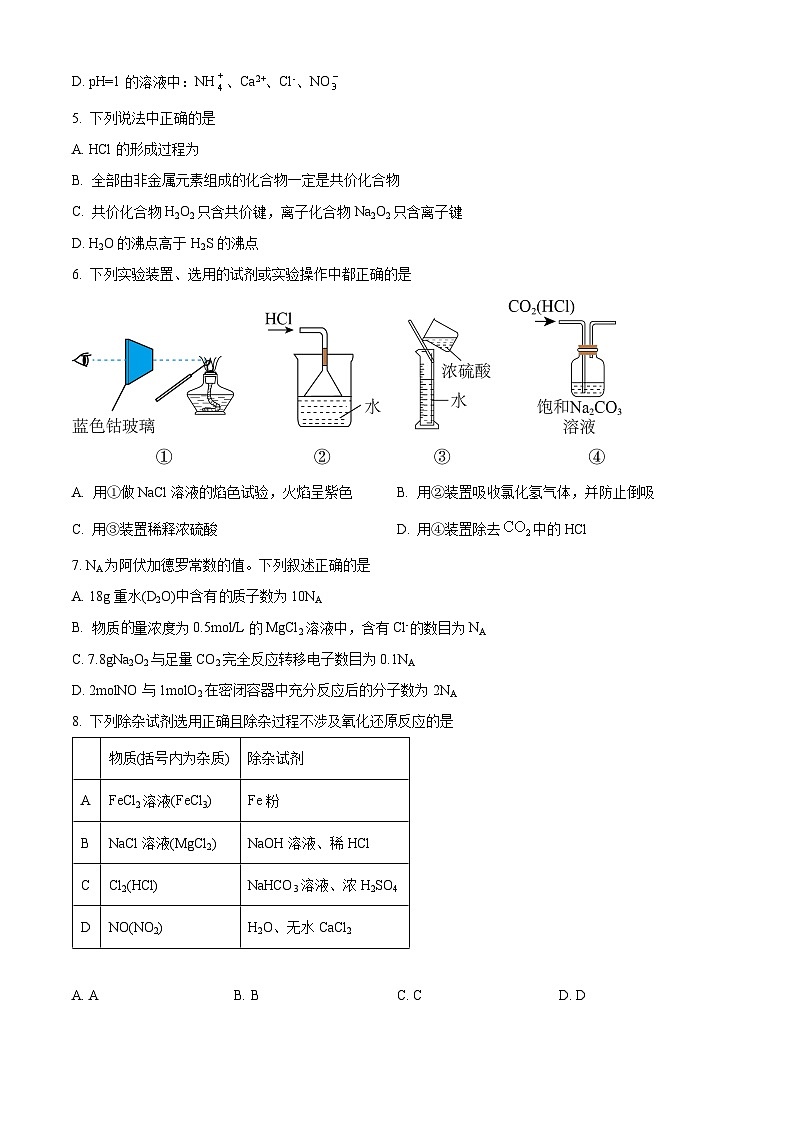
6. 下列实验装置、选用的试剂或实验操作中都正确的是
A. 用①做NaCl溶液的焰色试验,火焰呈紫色 B. 用②装置吸收氯化氢气体,并防止倒吸
C. 用③装置稀释浓硫酸 D. 用④装置除去中的HCl
【答案】B
【解析】
【详解】A.钠的焰色为黄色,用①做KCl溶液的焰色试验,火焰呈紫色,A错误;
B.HCl极易溶于水,用②装置既能充分吸收HCl,又能防止倒吸,B正确;
C.稀释浓硫酸应该在烧杯中进行,不能在量筒中进行,C错误;
D.除去CO2中的杂质HCl气体,应该使用饱和NaHCO3溶液,不能用饱和Na2CO3溶液,D错误;
故选B。
7. NA为阿伏加德罗常数的值。下列叙述正确的是
A. 18g重水(D2O)中含有的质子数为10NA
B. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-的数目为NA
C. 7.8gNa2O2与足量CO2完全反应转移电子数目为0.1NA
D. 2molNO与1molO2在密闭容器中充分反应后的分子数为2NA
【答案】C
【解析】
【详解】A.D2O的摩尔质量为20g/mol,18g重水的物质的量小于1mol,则含有的质子数小于10NA,A错误;
B.选项中并未说明MgCl2的体积,无法得知其物质的量,则无法确定氯离子的数目,B错误;
C.一个Na2O2与CO2反应转移1个电子,7.8gNa2O2物质的量为0.1mol,与足量二氧化碳反应转移电子数为0.1NA,C正确;
D.2molNO与1molO2反应生成2molNO2,NO2可转化为N2O4,该反应为可逆反应,容器中含有的分子数小于2NA,D错误;
故答案选C。
8. 下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质)
除杂试剂
A
FeCl2溶液(FeCl3)
Fe粉
B
NaCl溶液(MgCl2)
NaOH溶液、稀HCl
C
Cl2(HCl)
NaHCO3溶液、浓H2SO4
D
NO(NO2)
H2O、无水CaCl2
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.FeCl3与Fe反应生成FeCl2,则可用Fe除去 FeCl2溶液中的FeCl3,但反应中铁元素的化合价发生变化,属于氧化还原反应,A不符合;
B.氯化镁溶液和氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,过滤所得的氢氧化镁沉淀,可溶于盐酸,两个反应均为复分解反应、属于非氧化还原反应,提纯方法正确、B符合;
C.氯气与水反应:,盐酸能和碳酸氢钠发生反应、则氯气会被消耗,提纯方法错误,C不符合;
D.二氧化氮和水反应生成硝酸和一氧化氮,用水除去一氧化氮中的二氧化氮、并可用氯化钙固体干燥NO、提纯方法正确,但发生的是氧化还原反应,D不符合;
答案选B。
9. 下列反应的离子方程式书写正确的是
A. 已知氧化性Cl2>Br2>Fe3+,向FeBr2溶液中通入少量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+4Cl-
B. 向澄清石灰水中加入Ca(HCO3)2溶液:Ca2++OH-+HCO=CaCO3↓+H2O
C. 用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
D. 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO=BaSO4↓+H2O
【答案】B
【解析】
【详解】A.已知氧化性Cl2>Br2>Fe3+,则还原性Fe2+>Br-,向FeBr2溶液中通入少量的Cl2,发生反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,A错误;
B.向澄清石灰水中加入Ca(HCO3)2溶液,发生反应生成CaCO3和水,离子方程式为:Ca2++OH-+=CaCO3↓+H2O,B正确;
C.醋酸为弱酸,保留化学式,用醋酸除去水垢,离子方程式为2CH3COOH+CaCO3=Ca2++2CH3COO-+CO2↑+H2O,C错误;
D.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性,采用“以少定多”法,可设Ba(OH)2为1mol,需加入NaHSO42mol,离子方程式为:Ba2++2OH-+2H++=BaSO4↓+2H2O,D错误;
故选B。
10. 中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是
A. F、Cl、Br、I非金属性依次减弱;HF、HCl、HBr、HI的酸性也依次减弱
B. 通入CO2可增强漂白粉溶液漂白性;通入SO2也可增强漂白粉溶液漂白性(不考虑SO2溶解)
C Al(OH)3、Cu(OH)2受热易分解;Fe(OH)3受热也易分解
D. Na在空气中燃烧会生成Na2O2;Li在空气中燃烧也会生成Li2O2
【答案】C
【解析】
【详解】A.酸性与非金属性的关系是非金属性越强,其最高价氧化物对应水化物的酸性越强,氢化物不是最高价,故错误;
B.SO2具有还原性,次氯酸能把SO2氧化成,本身被还原成Cl-,故错误;
C.铁的活动性位于铝和铜之间,符合规律,故正确;
D.Li在氧气中反应只能生成Li2O,故错误。
答案选C。
11. 对下列事实的解释不正确的是
A. 二氧化氯具有氧化性,可用于自来水的杀菌消毒
B. 常温下,浓硝酸可以用铁制器皿贮存,说明铁与浓硝酸不反应
C. 液氨汽化时要吸收大量的热,可用作制冷剂
D. 漂白粉在空气中久置变质,是因为漂白粉中的Ca(ClO)2与空气中的CO2、H2O发生反应
【答案】B
【解析】
【详解】A.二氧化氯具有氧化性,能够使蛋白质变性,故可用于自来水的杀菌消毒,A正确;
B.常温下,铁遇到浓硝酸发生钝化,钝化是一种化学变化,故浓硝酸可以用铁制器皿贮存,并不是由于铁与浓硝酸不反应,B错误;
C.氨气易液化且液氨汽化时要吸收大量的热,可用作制冷剂,C正确;
D.漂白粉在空气中久置变质,是因为漂白粉中的Ca(ClO)2与空气中的CO2、H2O发生反应,Ca(ClO)2+H2O+CO2=CaCO3+2HClO、2HClO2HCl+O2↑,D正确;
故答案为:B。
12. 用如图装置制取气体(图中加热及气体收集装置均已略去;必要时可加热;a、b、c、d表示相应仪器中加入的试剂)。利用下列方案可得到干燥、纯净气体的是
选项
制备气体
a
b
c
d
A
浓盐酸
NaOH溶液
碱石灰
B
浓氨水
CaO
固体NaOH
C
NO
稀硝酸
Cu
D
稀硝酸
Zn
NaOH溶液
无水
A. A B. B C. C D. D
【答案】C
【解析】
【分析】
【详解】A.浓盐酸与共热可制备,但NaOH溶液会与反应,应选用饱和食盐水除杂,故A错误;
B.极易溶于水,不能通入水中,故B错误;
C.稀硝酸与铜反应生成NO,NO难溶于水,且不与反应,故可以用水除杂,用干燥,故C正确;
D.稀硝酸与Zn反应生成NO,不生成,故D错误;
故选C。
第II卷(非选择题共64分)
二、非填空题(本题共4小题,共64分。)
13. I.表中列出了第三周期的几种元素的部分性质:
元素编号
a
b
c
d
e
电负性
3.0
2.5
X
1.5
0.9
主要化合价
-1,+7
-2,+6
-3,+5
+3
+1
请按要求回答下列问题:
(1)写出基态a原子的价层电子排布式:____。
(2)表中元素原子半径最大的是(写元素符号)_____。
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)_____。
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为_____。
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)____。
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为____。
(7)下列说法合理的是____。
aSeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
【答案】(1)3s23p5
(2)Na (3)HCl>H2S>PH3
(4)Al(OH)3+OH-=AlO+2H2O或Al(OH)3+OH-=[Al(OH)4]-
(5)Na
相关试卷
这是一份【期中真题】河北省邢台市五校联考2022-2023学年高三上学期期中考试化学试题.zip,文件包含期中真题河北省邢台市五校联考2022-2023学年高三上学期期中考试化学试题原卷版docx、期中真题河北省邢台市五校联考2022-2023学年高三上学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。
这是一份【期中真题】江西省九校2021-2022学年高三上学期期中联考化学试题.zip,文件包含期中真题江西省九校2021-2022学年高三上学期期中联考化学试题原卷版docx、期中真题江西省九校2021-2022学年高三上学期期中联考化学试题解析版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。
这是一份【期中真题】江苏省南京市六校联合体2022-2023学年高三上学期11月联考化学试题.zip,文件包含期中真题江苏省南京市六校联合体2022-2023学年高三上学期11月联考化学试题原卷版docx、期中真题江苏省南京市六校联合体2022-2023学年高三上学期11月联考化学试题解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。









