




高中化学人教版 (2019)必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表教学课件ppt
展开经常把元素周期表中的同族元素放在一起研究,是因为他们之间存在着某种内在联系。那么,这种内在的联系是什么呢?我们将从他们的结构和性质的关系进行探讨。
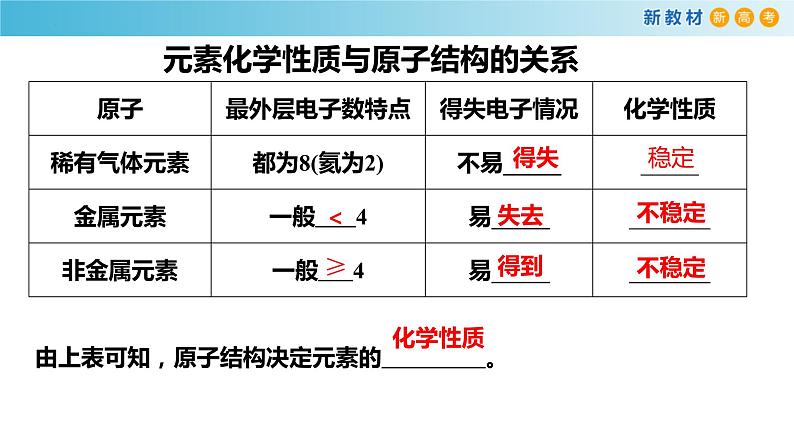
元素化学性质与原子结构的关系
由上表可知,原子结构决定元素的 。
第3课时原子结构与元素性质——碱金属
知道碱金属元素的原子结构及特点。
能说出碱金属元素化学性质的相似性及递变性。
初步学会根据原子结构的特点,推测元素的化学性质。
碱金属元素都位于周期表的第ⅠA族(元素Fr是一种放射性元素,高中阶段不探讨),化学性质很活泼,在自然界中都以化合态存在。
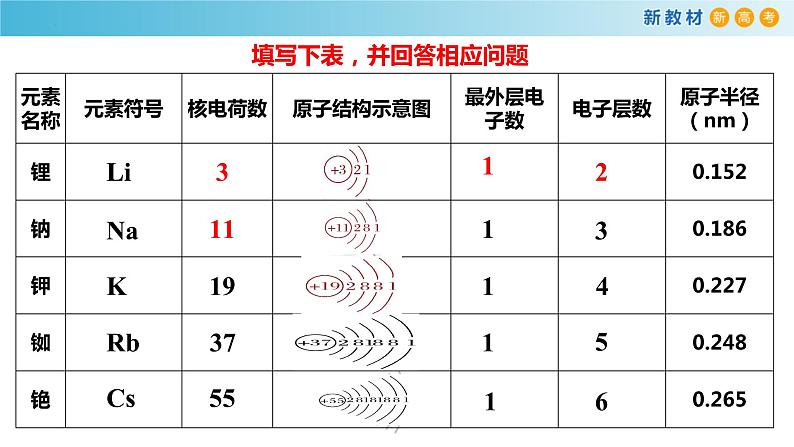
填写下表,并回答相应问题
(1) 在周期表中,从上到下碱金属元素原子的核电荷数、原子半径的变化有什么特点? (2) 观察碱金属元素的原子结构示意图,它们的原子核外电子排布有什么特点?
核电荷数递增,原子半径逐渐增大
随着核电荷数递增,电子层数增加,但最外层电子数都是1
思考:从结构推断碱金属元素的化学性质是否也具有相似性?
从上到下碱金属元素的核电荷数、原子半径的变化有什么特点?
他们的原子核外电子排布有什么特点?
从哪一点可以推测出碱金属元素化学性质具有相似性?
实验探究:碱金属元素的化学性质的比较
已有知识:钠的化学性质
4Na + O2 = 2Na2O
2Na + O2 Na2O2
2Na + 2H2O = 2NaOH + H2↑
合理推测:结合锂、钠、钾的原子结构特点,预测锂、钾可能具有的与钠相似的化学性质?
锂、钠、钾的原子核外最外层电子数都是1个,应该表现相似的化学性质,所以锂、钾与氧气、水应该都能发生反应
合理推测:结合钠、钾的原子结构特点,预测钾可能具有哪些与钠相似的化学性质?请你预测一下。
A.钾与 氧气、水都能发生反应
回忆第二章学过的知识,钠有哪些化学性质?
B.钾与 氧气、水都不能发生反应
C.钾与 氧气、水中的其中一个能发生反应
钾与氧气在加热条件下的反应现象是:
钾先熔化成小球,再剧烈燃烧,透过蓝色钴玻璃观察到紫色火焰。
演示实验:钾在空气中的燃烧
演示实验:钾与水的反应
钾与水的反应现象是::
浮、熔、游、响(轻微爆炸声并着火燃烧)、红
2K+2H2O=2KOH+H2↑
(1)钠钾有哪些相似的化学性质?
(2)比较钠钾与水反应的难易程度。
你能推断出锂与水反应的难易程度吗?
(3)碱金属与水反应的难易程度与其原子结构有什么关系?
由锂到铯,碱金属元素的原子电子层增加,原子半径增大,所以原子失电子能力增加,金属单质的活动性增强,其与水反应应该变得越来越容易
(3)通过比较碱金属与水反应的难易程度,你能发现与它们的原子结构有 什么关系? 由此,你能推断出碱金属的化学性质的相似性和递变规律吗?
由锂到铯,原子电子层逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,原子失去最外层电子的能力逐渐增强,金属性(还原性)逐渐增强。
都容易失去1个电子,都表现出还原性,都能与氧气、水反应
与O2、H2O的反应的反应越来越剧烈,由锂到铯,还原性逐渐增强。
(1)碱金属元素的相似性
碱金属元素的原子最外层都只有1个电子,在反应中容易失去,所以他们的化学性质相似,都能与氧气、水反应
(2)碱金属元素的递变性:
4Li + O2 2Li2O
2K + 2H2O = 2KOH + H2↑
随着核电荷数递增,碱金属元素的原子电子层增加,原子半径增大,所以原子失电子能力增加,原子核对最外层电子的引力逐渐减弱,原子失去最外层电子的能力逐渐增强,即由锂到铯,金属性逐渐增强。
碱金属性质的相似性和递变性
具体情况如下: ①与氧气反应 从Li→Cs,与氧气反应越来越剧烈,产物越来越复杂。如Li与O2生成Li2O,Na与O2生成Na2O、Na2O2,K与O2生成K2O、KO2。 ②与H2O(或酸)的反应 从Li→Cs,与H2O(或酸)反应越来越剧烈。如K与H2O反应能发生轻微爆炸,则Rb、Cs遇水会发生爆炸。
碱金属性质的相似性和递变性
1.从碱金属原子结构的角度解释。(1)碱金属元素的化学性质具有相似性。
提示 碱金属元素的最外层电子数相同,都是1个电子,故它们的化学性质相似。
(2)碱金属元素的性质具有递变性。
提示 随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,原子失电子的能力逐渐增强。
碱金属元素的主要物理性质
碱金属在物理性质上也表现出一些相似性和递变性。
碱金属元素的性质与结构
单质具有强还原性,可与氧气、水等反应
(1)从锂到铯,碱金属元素单质的密度依次增大( )(2)Li、Na、K在空气中燃烧均生成过氧化物( )(3)碱金属元素原子随核电荷数增加,其单质与水反应越来越剧烈( )(4)碱金属元素单质都应该保存在煤油中( )(5)K比Na活泼,故K可以从钠盐溶液中置换出Na( )(6)碱金属元素在自然界中能以游离态存在( )
一般情况下,元素的金属性强弱可以从其单质与水(或酸)反应置换出氢的难易程度来判断,也可以从它们的最高价氧化物对应的水化物——氢氧化物的碱性强弱来判断,请写出Li→Cs,氢氧化物碱性由弱至强的顺序为_______________________________。
LiOH
1.已知铷(Rb)是37号元素,其相对原子质量是85.5,与钠同主族,回答下列问题:(1)铷位于第____周期,其原子半径比钠元素的原子半径____(填大或小)。
(2)铷单质性质活泼,写出它与氯气反应的化学方程式:________________________。铷单质易与水反应,反应的离子方程式为________________________________,铷与水反应比钠与水反应______(填“剧烈”或“缓慢”)。遇水后沉在水_____(填“底”或“上”),铷的密度比水的密度_____(填“大”或“小”)。
===2Rb++2OH-+H2↑
(3)同主族元素的同类化合物的化学性质相似,写出过氧化铷与CO2反应的化学方程式:______________________________。
2Rb2O2+2CO2===2Rb2CO3+O2
2.下列叙述正确的是A.碱金属单质性质相似,均为银白色(铯除外)的柔软金属,密度都比 较小B.碱金属单质在空气中燃烧生成的都是过氧化物C.碱金属单质的熔、沸点随原子序数的增加而升高D.Li、Na、K都可以保存在煤油中
3.如图表示第ⅠA族金属(又称为碱金属)的某些性质与核电荷数的变化关系,则下列各性质不符合图示关系的是 A.金属性B.与水反应的剧烈程度C.阳离子的氧化性D.原子半径
人教版 (2019)必修 第一册第二节 金属材料教学课件ppt: 这是一份人教版 (2019)必修 第一册第二节 金属材料教学课件ppt,共20页。PPT课件主要包含了学习目标,特别注意,课堂小练,新型合金,记忆合金等内容,欢迎下载使用。
人教版 (2019)第一节 原子结构与元素周期表教学ppt课件: 这是一份人教版 (2019)第一节 原子结构与元素周期表教学ppt课件,共20页。PPT课件主要包含了学习目标等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二节 金属材料教学ppt课件: 这是一份人教版 (2019)必修 第一册第二节 金属材料教学ppt课件,共20页。PPT课件主要包含了学习目标,第2课时铝及铝合金,铝合金,常见的铝合金等内容,欢迎下载使用。













