

高中化学苏教版 (2019)必修 第二册第一单元 化学反应速率与反应限度测试题
展开
这是一份高中化学苏教版 (2019)必修 第二册第一单元 化学反应速率与反应限度测试题,共11页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
一、单选题
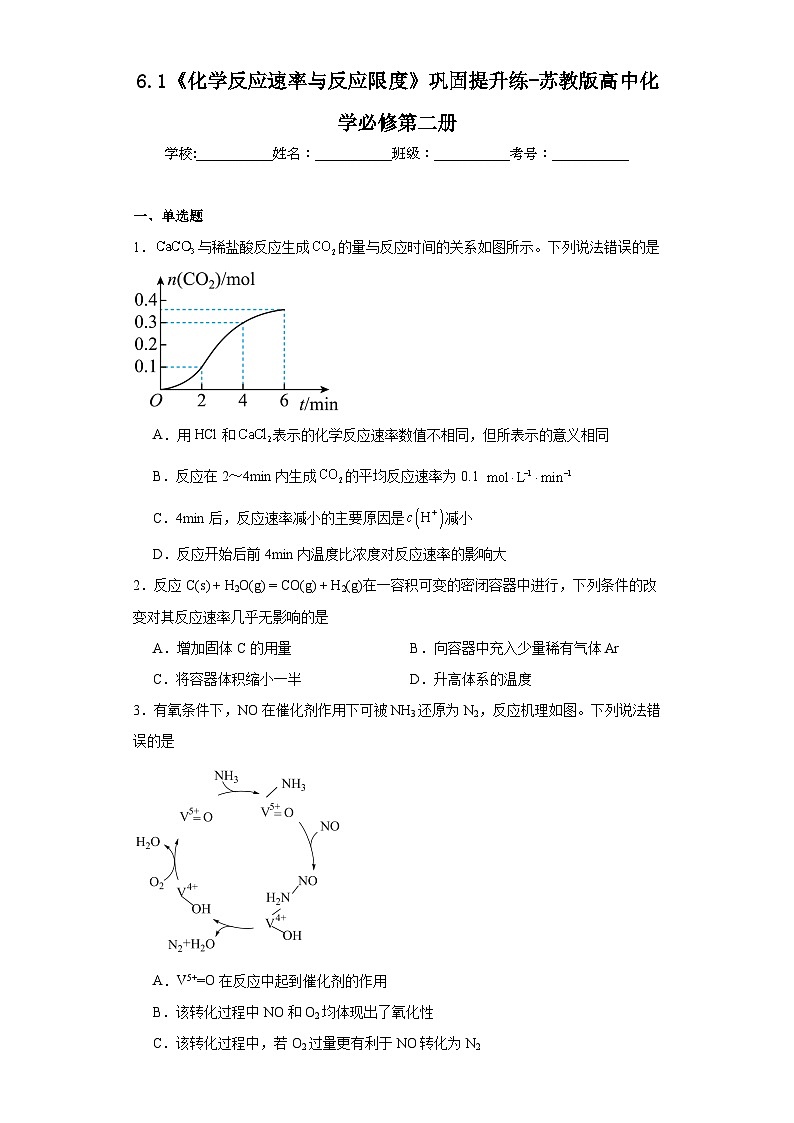
1.与稀盐酸反应生成的量与反应时间的关系如图所示。下列说法错误的是
A.用HCl和表示的化学反应速率数值不相同,但所表示的意义相同
B.反应在2~4min内生成的平均反应速率为0.1
C.4min后,反应速率减小的主要原因是减小
D.反应开始后前4min内温度比浓度对反应速率的影响大
2.反应C(s) + H2O(g) = CO(g) + H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.增加固体C的用量B.向容器中充入少量稀有气体Ar
C.将容器体积缩小一半D.升高体系的温度
3.有氧条件下,NO在催化剂作用下可被NH3还原为N2,反应机理如图。下列说法错误的是
A.V5+=O在反应中起到催化剂的作用
B.该转化过程中NO和O2均体现出了氧化性
C.该转化过程中,若O2过量更有利于NO转化为N2
D.该转化过程的总反应为4NH3+4NO+O24N2+6H2O
4.某温度下,将0.28 g铁粉投入100 mL、0.1 ml/L稀盐酸中,2 min时刚好反应结束。下列有关这个反应的说法,正确的是
A.反应前稀盐酸pH=1B.反应前稀盐酸中c(OH-)=1.0×10-13 ml/L
C.铁的平均反应速率是0.05 ml/(L·.min)D.反应结束后的溶液恰好呈中性
5.一定温度下,在容积可变的密闭容器中进行反应:N2(g)+3H2(g) ⇌2NH3(g)。说明该反应达到平衡状态的是
A.υ正(N2)=2υ逆(NH3)B.容器内的压强不再变化
C.混合气体的密度不再变化D.每断裂3mlH-H键,同时生成6mlN-H键
6.下列做法与化学反应速率无关的是
A.向门窗合页里注油
B.常用冰箱保存食物
C.食品抽真空包装
D.“冰墩墩”的制作材料在生产过程中添加抗老化助剂
7.一定温度下,一定体积的容器加入一定量的A(s)发生反应:3A(s)⇌B(g) +2C(g),下列描述中不能说明该反应达到平衡的是
①v(B)逆=2v(C)正; ②单位时间内生成 a ml B,同时消耗 2a ml C;
③容器中的压强不再变化; ④混合气体的密度不再变化;
⑤B的体积分数不再变化; ⑥混合气体的平均相对分子质量不再变化
A.①②③B.②③④C.①⑤D.①⑤⑥
8.已知:CO2氧化C2H6制C2H4的主反应热化学方程式为:
该反应的历程分为如下两步:
反应①: (快反应)
反应②: (慢反应)
下列说法正确的是
A.反应①的活化能反应②的活化能
B.相比于提高,提高对主反应速率影响更大
C.将液化分离,可以提高反应物的转化率
D.若反应①的,则该反应自发进行的最高温度T=1125K
9.下列有关可逆反应的说法不正确的是( )
A.可逆反应是指在同一条件下能同时向正逆两个方向进行的反应
B.可逆反应的速率越大,进行的限度也就越大
C.可逆反应达到平衡时,反应并未停止,但是用反应物或生成物表示的平均反应速率为0
D.存在平衡的不一定是可逆反应
10.下列说法正确的是
A.利用等质量、颗粒大小基本相同的锌粒分别与和的硫酸反应,比较两者收集氢气所用的时间,探究硫酸浓度对反应速率影响
B.实验用等浓度的和在不同温度下反应观察气泡产生速率,探究温度对反应速率的影响
C.向盛有溶液的试管中加入几滴酸化的溶液的现象为:溶液先变成棕黄色,一段时间后有气泡产生
D.很多离子都是有颜色的:蓝色、黄色、橙色、黄色
二、填空题
11.在一密闭容器中充入1 ml H2和1 ml I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) 2HI(g)
(1)保持容器容积不变,向其中充入1 ml H2,反应速率 (填“增大”、“减小”或“不变”,下同)。
(2)升高温度,反应速率 。
(3)扩大容器体积,反应速率 。
(4)保持容器内气体压强不变,向其中充入1 ml H2(g)和1 ml I2(g),反应速率 。
12.化学反应进行的快慢和程度是研究化学反应的重要方向。请完成下列填空。
Ⅰ.在某一容积为4L的密闭容器中,A、B、C、D四种物质的物质的量随时间的变化曲线如图所示,完成下列问题:
(1)该反应的化学方程式为 。
(2)前用A的浓度变化表示的化学反应速率为 。
Ⅱ.是一种常用的还原剂。一定条件下,反应的速率方程为(k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示:
(3)根据表中测定结果,推断出a= 、b= 。
(4)改变下列反应条件,反应速率增大的是___________(填字母)。
A.降温B.缩小体积C.加入催化剂D.减压
(5)可以判断反应已经达到平衡状态的是 。
A.的物质的量分数保持不变
B.体系中气体颜色不变
C.等温等容,体系中气体密度保持不变
D.等温等压,体系压强不再发生变化
E.消耗的同时生成
F.若反应在绝热体系中进行,体系温度不再变化
13.通过实验测定反应速率的方法有多种,如:
①比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的 来实现;
②在KMnO4与H2C2O4反应中,KMnO4与H2C2O4反应的离子方程式: 。可通过测定 来测定该反应的速率;
③在Na2S2O3和H2SO4反应中,反应方程式为: 该反应的速率可通过 来测定。
14.某温度时,在一个容积为2L的密闭容器中,A、B、C三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
(1)该反应的化学方程式为 。
(2)反应从开始至2min末,用C的浓度变化表示的平均反应速率为v(C)= 。
(3)①2min时,正反应速率 逆反应速率(填“>”“
相关试卷
这是一份苏教版 (2019)必修 第二册专题9 金属与人类文明第一单元 金属的冶炼方法课后作业题,共10页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
这是一份苏教版 (2019)第二单元 探究铁及其化合物的转化随堂练习题,共10页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
这是一份高中苏教版 (2019)第二单元 食品中的有机化合物同步训练题,共10页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。










