



人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt
展开
这是一份人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt,共21页。PPT课件主要包含了产生蓝色沉淀,产生白色沉淀,Cl-,反应前,反应后,CO2↑,SO42-,NO3-,有水生成,有气体生成等内容,欢迎下载使用。
什么条件下复分解反应才能发生呢?
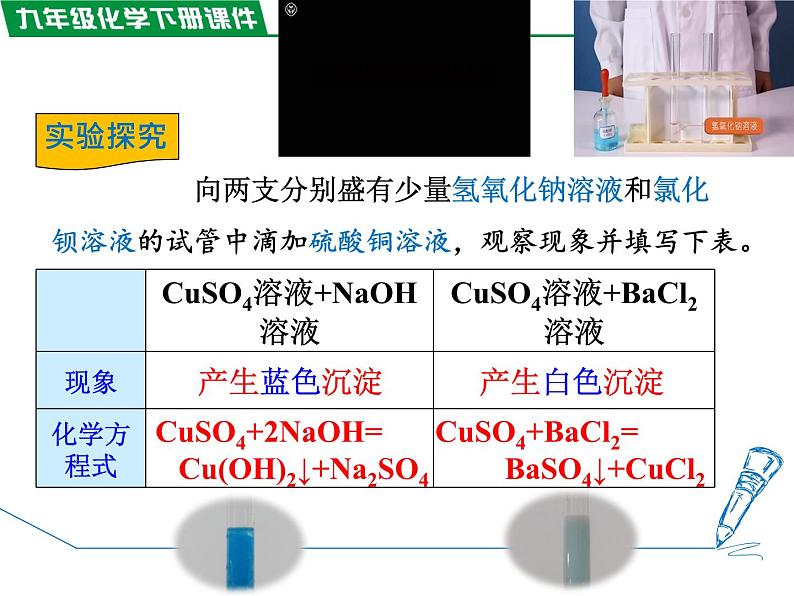
复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应。
特点:双交换,价不变。
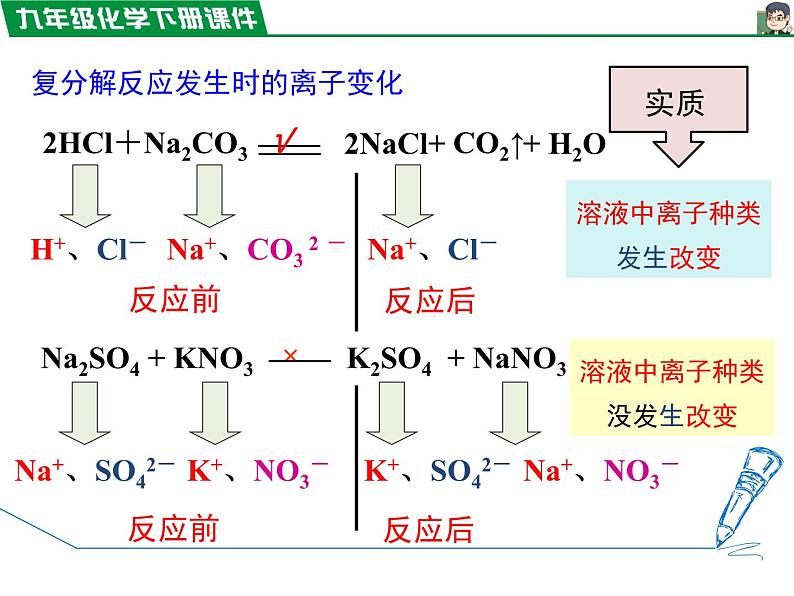
向两支分别盛有少量氢氧化钠溶液和氯化钡溶液的试管中滴加硫酸铜溶液,观察现象并填写下表。
CuSO4+2NaOH= Cu(OH)2↓+Na2SO4
CuSO4+BaCl2= BaSO4↓+CuCl2
上述两个反应是否属于复分解反应?观察到的现象有什么共同之处?
前面学过的酸碱中和反应是否也属于复分解反应?中和反应的生成物中,相同的生成物是什么?
碳酸钠、碳酸钙等含碳酸根的盐溶液与盐酸发生复分解反应时,可观察到的共同现象是什么?
生成沉淀:当反应中有难溶或微溶的物质生成,溶液中就会出现沉淀(即通常所说“变浑浊”)。
复分解反应发生的条件:
①生成水;②生成气体;③生成沉淀。(满足一条即可)
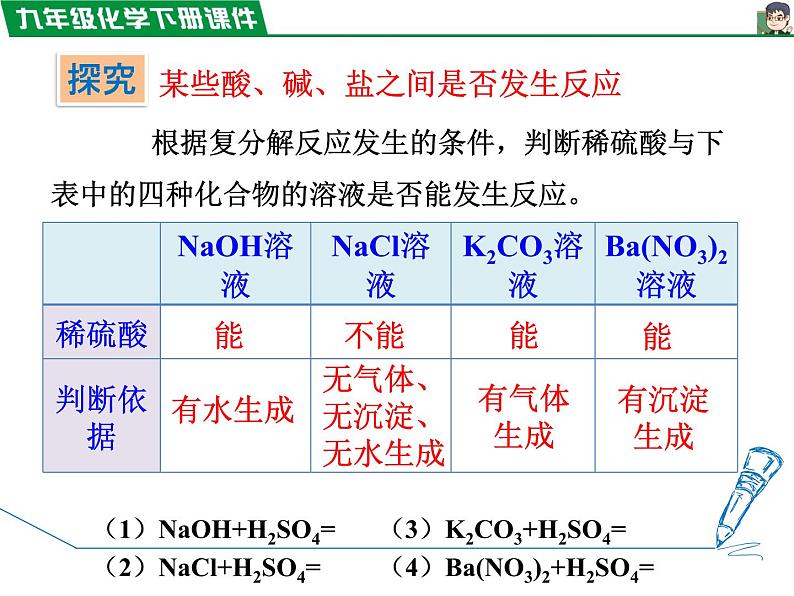
Na+、CO3 2 -
溶液中离子种类发生改变
2HCl+Na2CO3 ——
2NaCl+ + H2O
复分解反应发生时的离子变化
K2SO4 + NaNO3
Na2SO4 + KNO3 ——
溶液中离子种类没发生改变
根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液是否能发生反应。
无气体、无沉淀、无水生成
某些酸、碱、盐之间是否发生反应
(1)NaOH+H2SO4=(2)NaCl+H2SO4=
(3)K2CO3+H2SO4=(4)Ba(NO3)2+H2SO4=
下列化学反应属于复分解反应的是( )
A.Zn+H2SO4=ZnSO4+H2↑ B.2KMnO4==K2MnO4+MnO2+O2↑
C.CaO+H2O=Ca(OH)2 D.CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
1、金属+盐→新盐+新金属
反应条件: (1)盐必须溶于水 (2)金属单质除K、Ca、Na外;Fe参加的 置换反应生成+2价的亚铁 (3)金属的活动性比盐中金属活动性强
Fe + CuSO4 = FeSO4 + Cu
2、盐+酸→新盐+新酸
反应条件:生成物中有沉淀或气体或水
3、盐+碱→新盐+新碱
反应条件:反应物两者均可溶;生成物有沉淀或气体或水
AgNO3 + HCl = AgCl↓+ HNO3BaCl2 + H2SO4 = BaSO4 ↓ + 2HCl
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOHFeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
AgNO3 + NaCl = AgCl ↓ + NaNO3BaCl2 + Na2SO4 = BaSO4 ↓ + 2NaCl
4、盐+盐→新盐+新盐
反应条件:反应物两者均可溶;生成物有沉淀
1、盐 + 金属 = 新盐 + 新金属
2、盐 + 酸 = 新盐 + 新酸
3、盐 + 碱 = 新盐 + 新碱
4、盐 + 盐 = 新盐 + 新盐
【例2】下列各组溶液,两两混合后,能发生反应,且溶液的总质量不发生改变的是( )A.氯化钠溶液与硝酸钾溶液B.碳酸钠溶液与稀盐酸C.氢氧化钠溶液与稀盐酸D.硝酸银溶液和氯化铁溶液
盐+金属→新盐+新金属盐+酸→新盐+新酸盐+碱→新盐+新碱盐+盐→新盐+新盐
通式:AB + CD === AD + CB酸、碱、盐的溶解性应用:物质共存、除杂质、鉴别
1、下列物质间不能发生复分解反应的是( )A.碳酸钙和稀盐酸 B.硝酸钠溶液和氯化钾溶液C.氯化钡溶液和硫酸钾溶液 D.氯化铁溶液和氢氧化钠溶液
2、 (2019临沂)下列物质混合,能发生化学反应且现象不明显的是( )A.铝与硫酸铜溶液B.氢氧化钠溶液与稀盐酸C.澄清石灰水与纯碱溶液D.硫酸钠溶液与氯化铜溶液
3、(2019重庆)下列试剂分别滴入Ca(OH)2、H2SO4、Na2SO4三种溶液中,会出现三种不同现象的是( ) A.Na2CO3溶液 B.MgCl2溶液 C.Ba(NO3)2溶液 D.酚酞溶液
4.下列反应,属于化合反应的是( ),属于分解反应的是( ),属于置换反应的是( ),属于复分解反应的是( )属于中和反应的是( )A.Fe + H2SO4 ==== FeSO4 + H2↑B.H2CO3 ==== H2O + CO2↑ C.2NaOH + H2SO4 ==== Na2SO4 +2H2O D.S + O2 ==== SO2E.2NaOH + CuSO4 ==== Na2SO4 +Cu(OH)2↓
酸、碱、盐的溶解性(20℃)
钾盐、钠盐、铵盐、硝酸盐都可溶;盐酸盐只有氯化银不可溶;硫酸盐只有硫酸钡不可溶;碳酸盐只溶钾、钠、铵,剩下都不溶。
注意:AgCl、BaSO4既不溶于水,也不溶于稀硝酸。
BaSO4(白色沉淀) AgCl(白色沉淀)CaCO3 (白色沉淀) BaCO3 (白色沉淀)Mg(OH)2(白色沉淀) Cu(OH)2(蓝色沉淀)
盐的水溶液的颜色铜盐溶液一般呈蓝色 铁盐溶液一般呈黄色亚铁盐溶液一般呈浅绿色 高锰酸钾溶液呈紫红色
离子共存的条件:相互之间不发生反应生成水、气体、沉淀。
下列离子在水中能大量共存,并形成无色溶液的是( )A.Fe3+ Na+ NO3﹣ Cl﹣B.K+ Na+ OH﹣ SO42﹣C.H+ K+ SO42﹣ OH﹣D.Ba2+ NO3﹣ CO32﹣ Cl﹣
碳酸根(碳酸氢根)离子的检验
②通入澄清石灰水,现象:
CaCO3 +2HCl === CaCl2 + H2O + CO2↑
Ca(OH)2 + CO2=== CaCO3↓+H2O
H2SO4 + BaCl2 === BaSO4 ↓+ 2HCl
Na2SO4 + BaCl2 === BaSO4↓ + 2NaCl
HCl + AgNO3 === AgCl↓ + HNO3
NaCl + AgNO3 === AgCl↓ + NaNO3
①滴加氢氧化钠溶液,现象:
②用红色石蕊试纸检验,现象:
或用沾有无色酚酞的棉花检验,现象:
NH4Cl + NaOH === NaCl + NH3↑ + H2O
有四种澄清透明的溶液:①MgCl2溶液 ②Cu(NO3)2溶液 ③K2SO4溶液 ④KOH溶液。不用其他试剂就可进行鉴别,鉴别出来的先后顺序是( )A.④①②③ B.②④①③C.③②①④ D.②①③④
1、食盐、食醋、纯碱均是家庭厨房中常用的物质,利用这些物质,我能够完成的实验是( )①检验自来水中是否含有氯离子 ②除去热水瓶中的水垢 ③区分食盐和纯碱 ④检验鸡蛋壳中是否含有碳酸钙A.①② B.①③ C.①④ D.②③④
相关课件
这是一份初中化学人教版九年级下册课题1 生活中常见的盐获奖教学ppt课件,共20页。PPT课件主要包含了复分解反应,化合物1,化合物2,化合物3,化合物4,复分解反应的概念,复分解反应的表达式,复分解反应的特点,化学反应类型,化合反应等内容,欢迎下载使用。
这是一份初中人教版课题1 生活中常见的盐教学课件ppt,共21页。PPT课件主要包含了NaCl,氯化钠NaCl,碳酸钠Na2CO3,高锰酸钾KMnO4,碳酸钙CaCO3,碳酸氢钠NaHCO3,碳酸盐,易溶于水的白色粉末,碳酸钠的用途,洗涤剂等内容,欢迎下载使用。
这是一份人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt,共21页。PPT课件主要包含了亚硝酸钠NaNO2,盐的概念,HCl,CaOH2,NaCl,H2SO4,NaOH,Na2CO3,NaHCO3,CaCO3等内容,欢迎下载使用。










