



人教版九年级下册课题2 溶解度集体备课ppt课件
展开氯化钠能溶于水,那么一滴水能溶解1吨氯化钠吗?
今天我们就一同来探讨这个问题。
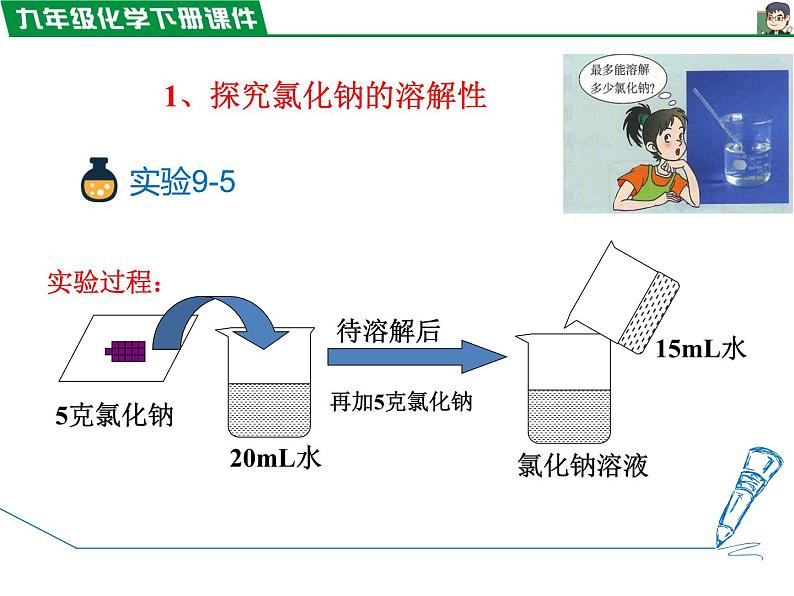
1、探究氯化钠的溶解性
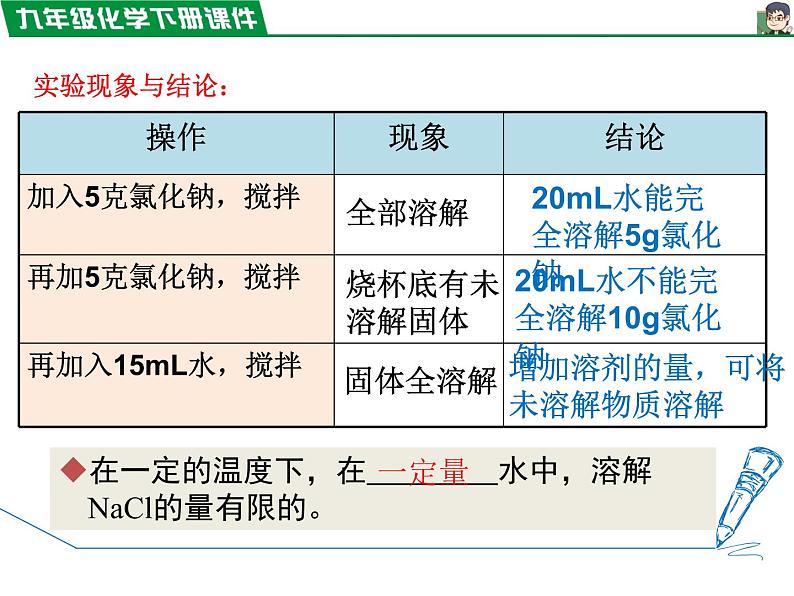
20mL水能完全溶解5g氯化钠
20mL水不能完全溶解10g氯化钠
增加溶剂的量,可将未溶解物质溶解
在一定的温度下,在 水中,溶解NaCl的量有限的。
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做这种溶质的饱和溶液。 还能继续溶解的溶液叫做这种溶质的不饱和溶液。
如何判断一种溶液是否饱和呢?
(2)保持温度和溶剂不变;加入少量原溶质,能继续溶解溶质则是不饱和溶液;不能继续溶解溶质则是饱和溶液。
(1)根据溶液中是否有剩余的溶质固体判断;在一定条件下,若溶液底部有稳定存在的溶质固体;且该固体不再减少,则该溶液属于饱和溶液。
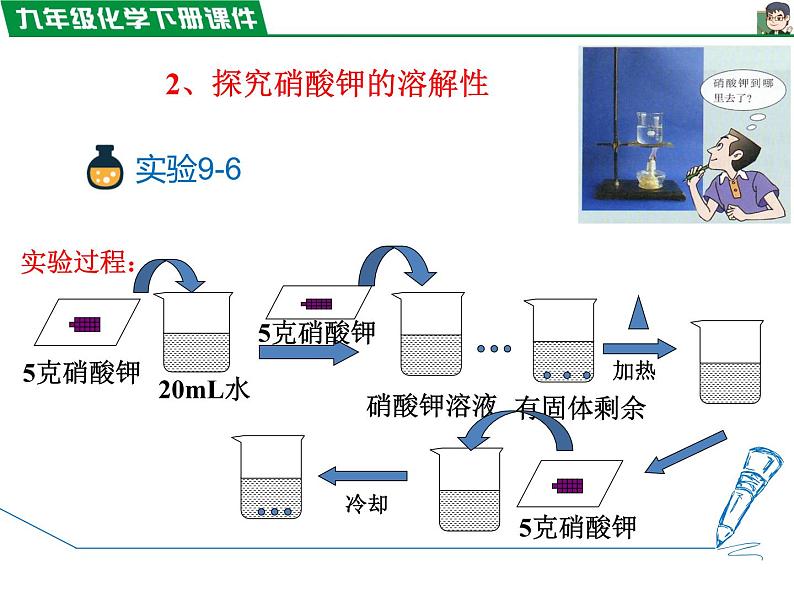
2、探究硝酸钾的溶解性
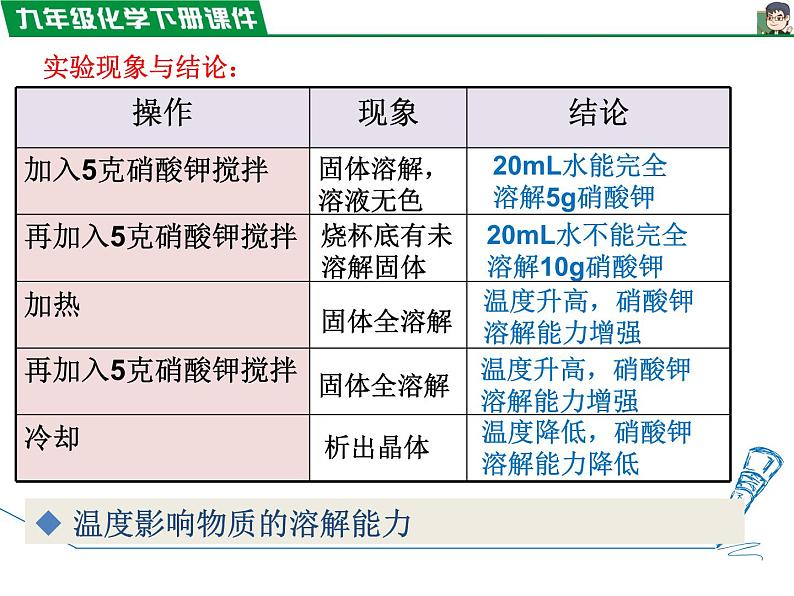
20mL水能完全溶解5g硝酸钾
20mL水不能完全溶解10g硝酸钾
温度升高,硝酸钾溶解能力增强
温度降低,硝酸钾溶解能力降低
温度影响物质的溶解能力
取少量冷却后的饱和硝酸钾溶液于小试管中,加入少量高锰酸钾固体,观察高锰酸钾能否溶解?
1、影响饱和溶液的因素
饱和溶液是指在一定温度下、一定量的溶剂里,不能继续溶解这种溶质的溶液,但还能溶解其他溶质。因此,表述某溶质的饱和溶液要指明溶质。如氯化钠饱和溶液、硝酸钾饱和溶液。
有一瓶接近饱和的硝酸钾溶液,欲使其成为饱和溶液,可采用的方法有哪些?
加入硝酸钾、蒸发掉一些水、降低温度
将硝酸钾的饱和溶液配成不饱和溶液,可采用的方法有哪些?
增加溶质、蒸发溶剂、降低温度
不饱和溶液 饱和溶液
增加溶剂、升高温度
加入溶质、蒸发溶剂、降低温度
2、饱和溶液与不饱和溶液的相互转化
(1)对于大多数物质:
加入溶质、蒸发溶剂、升温
20℃时,往盛有饱和食盐水的烧杯中加入5g食盐,加入食盐后的溶液中,质量不变的是( ) A.溶剂的质量 B.溶质的质量 C.溶液的质量 D.溶剂、溶质、溶液的质量
饱和溶液不包括未溶解的固体!
在同量的溶液中:含溶质较多的溶液——浓溶液 含溶质较少的溶液——稀溶液
不同的溶质:浓溶液不一定是饱和溶液, 稀溶液不一定是不饱和溶液。相同溶质、相同温度:饱和溶液一定比不饱和溶液浓。
溶液在一定条件下可分为饱和溶液和不饱和溶液
不给定条件可分为浓溶液和稀溶液
①同一种物质的饱和溶液一定比不饱和溶液浓。
②在一定温度下,向硝酸钾溶液中加入少量硝酸 钾,如果溶液质量不变,则该溶液是饱和溶液。
③同一种物质的饱和溶液一定比不饱和溶液中的溶质多。
④在一定温度下,溶质的质量不改变,则无法使不饱和溶液变成饱和溶液。
⑤在一定温度下的氯化钠饱和溶液,一定不能继续溶解硝酸钾。
⑥两种不同溶质的饱和溶液混合,依然是饱和溶液。
溶解在溶液中的溶质从溶液中以晶体形式析出,这一过程叫做结晶。
(1)降温结晶:(冷却热的饱和溶液)
适用于溶解能力受温度影响较大的物质,如:从硝酸钾溶液中获得KNO3晶体。
结晶后所得到的溶液是饱和溶液。
适用于溶解能力受温度影响较小的物质,[可加热蒸发、也可自然蒸发],如:从海水中获得NaCl晶体。
蒸发操作过程中的注意事项:
a、蒸发皿的溶液不超过蒸发皿容积的2/3;b、加热过程中要不断搅拌,以免溶液溅出;c、不能蒸干,应当析出大量晶体时就熄灭酒精灯,利用余热蒸发至干。
析出晶体后的溶液叫母液,对于析出的溶质来说是饱和溶液。
不饱和溶液 饱和溶液
饱和溶液:溶质不能继续溶解
不饱和溶液:溶质能继续溶解
蒸发结晶(海水提取食盐)
1、(2019温州)如图,将红砂糖倒入一杯开水中,充分溶解。能作为判断砂糖水是饱和溶液的依据是( )A.砂糖水颜色很深B.砂糖水味道很甜C.砂糖溶解得很快D.砂糖固体有剩余
2、填空 20度时,将33克食盐放入100克水中,食盐全部溶解,此时溶液质量为 克,再向此溶液加入3克食盐又恰好全部溶解,则溶质为 克,现在溶液恰好饱和,此时溶液的质量为 克,再向此溶液加入3克食盐,溶液的质量是 克。
3、对结晶后的溶液,下列说法中正确的是( )A.一定是饱和溶液 B.一定是不饱和溶液C.一定是浓溶液 D.一定是稀溶液
4、下列关于饱和溶液的说法中,错误的是( )A、在温度不变时,KNO3的饱和溶液不能再溶解KNO3 B、当温度升高时,饱和溶液一定能继续溶解溶质C、稀溶液一定是不饱和溶液,浓溶液一定是饱和溶液D、改变温度可以使不饱和溶液变成饱和溶液
初中化学人教版九年级下册课题2 溶解度优秀ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度优秀ppt课件,共24页。PPT课件主要包含了学习目标,情境导入,全部溶解,部分溶解,KNO3析出,+5gNaCl,+15mL水,+5gKNO3,探究新知,分析概念等内容,欢迎下载使用。
人教版九年级下册课题2 溶解度图文ppt课件: 这是一份人教版九年级下册课题2 溶解度图文ppt课件,文件包含1第1课时饱和溶液与不饱和溶液pptx、921-1氯化钠在水中的溶解mp4、921-2硝酸钾在水中的溶解mp4等3份课件配套教学资源,其中PPT共19页, 欢迎下载使用。
9.2.1饱和溶液 不饱和溶液【预习课程】+【知识精讲】课件PPT: 这是一份9.2.1饱和溶液 不饱和溶液【预习课程】+【知识精讲】课件PPT,文件包含化学九年级-921知识精讲饱和溶液不饱和溶液pptx、化学九年级-921预习课程饱和溶液不饱和溶液pptx等2份课件配套教学资源,其中PPT共19页, 欢迎下载使用。













