





人教版课题3 溶液的浓度教学演示课件ppt
展开为什么会出现这样的奇景?
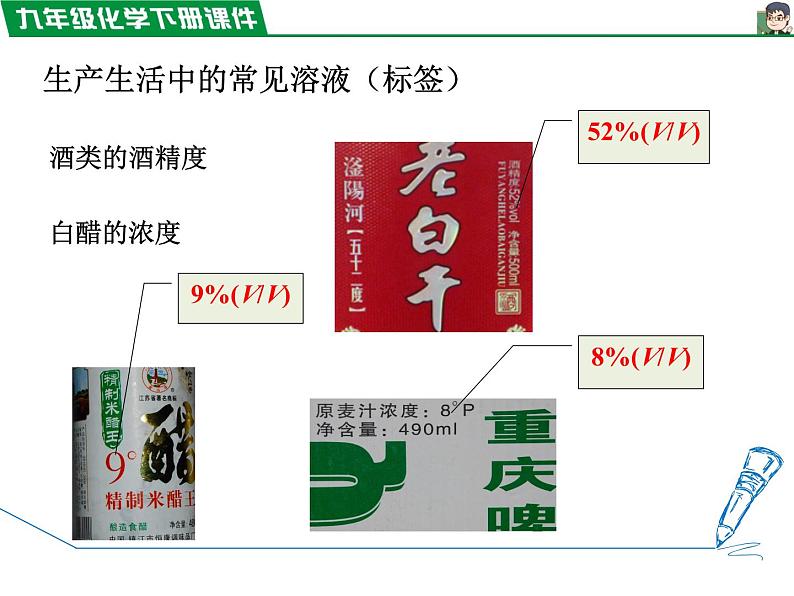
生产生活中的常见溶液(标签)
生理盐水中NaCl的含量
溶液中溶质质量的多少如何表示呢?
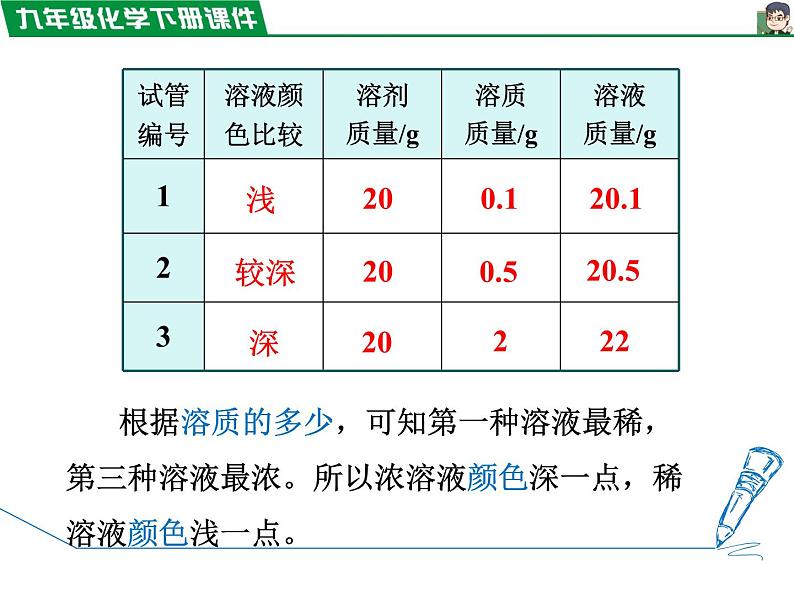
三种浓稀不同的硫酸铜溶液,哪种溶液最浓?哪种最稀?你的判断依据是什么?
根据溶质的多少,可知第一种溶液最稀,第三种溶液最浓。所以浓溶液颜色深一点,稀溶液颜色浅一点。
对于有色溶液来说,根据颜色的深浅可以区分溶液是浓还是稀。但这种方法比较粗略,不能准确地表明一定量的溶液里究竟含有多少溶质。
表示溶液组成的方法有多种,这里主要认识溶质的质量分数。
化学纯 500mL 浓盐酸(HCl) 含HCl 37 % 密度为1.18 g/cm3
1.定义:溶质质量与溶液质量之比
溶质质量 = 溶液质量× 溶质的质量分数
溶液质量 = 溶质质量/ 溶质的质量分数
结论:一般而言,有色溶液的颜色深些其溶质的质量分数大些。
2、按规定的量配制氯化钠溶液
在室温下,根据下表规定的质量配制氯化钠溶液,观察现象(能否全部溶解),并计算溶液中溶质的质量分数。
结论:溶液中溶质的质量分数越大,溶液浓度越大。
计算式中溶质质量是指被溶解的那部分溶质的质量,没有被溶解的那部分溶质质量不能计算在内。
已知200C时,氯化钠的溶解度是36g。有人说:“200C时氯化钠饱和溶液中溶质的质量分数为36%”这种说法对吗?为什么?
36 100 136
溶质的质量分数表示溶质质量与溶液质量之比,并不是溶质质量与溶剂质量之比。
饱和溶液的溶质质量分数=
溶质的质量分数36%是指: 每100g溶液中含有36g溶质。溶质T℃时溶解度36g是指: 在T℃时,100g水最多溶解该溶质36g。
表示溶液中溶质质量的多少
溶质质量分数与溶解度的比较
下列叙述中正确的是( )
A.浓度大的溶液一定是饱和溶液B.饱和溶液的浓度一定大C.通过溶液中溶质的质量分数可以换算出该溶质的溶解度D.通过饱和溶液中溶质的溶解度可以换算出该溶质的质量分数
答:需要24kg氯化钠和126kg水。
例1:在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
分析:解决这道题的关键是什么?
溶液稀释前后溶质的质量不变
设稀释后溶液的质量为x。
50g× 98%= x × 20%
x=245g 需要水的质量=245g-50g=195g
答:需要水的质量为195g。
例2: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
解法2:设需要加水的质量为x,则稀释后溶液的质量为(50g+x), 根据稀释前后溶液中溶质的质量不变, 50g×98%=(50g+x)×20% 解得:x=195g。
有关溶液稀释问题的计算 解题依据:溶液稀释前后,溶质的质量不变。 若有某溶液Ag,其溶质的质量分数为a%,稀释后得到溶质质量分数为b%的溶液Bg。则有:
Ag×a% = Bg×b%(稀释前)(稀释后)
溶液的稀释(A×a% = B×b%)
1、定义:溶质质量与溶液质量之比
1、对10%的氯化钠溶液含义的解释错误的是( ) A.100g水中溶解了10g氯化钠 B.100g氯化钠溶液中含有10g氯化钠 C.将10g氯化钠溶于90g水中所得的溶液 D.氯化钠与溶液的质量之比是1∶10
2、一定温度下,将溶液用水稀释,一定不发生变化的量是( )A.溶液的质量 B.溶质的质量C.溶剂的质量 D.溶质的质量分数
3、 (2019金华)甲是60 ℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )A.甲一定是不饱和溶液B.丙和丁一定是饱和溶液C.乙的溶质质量分数一定比甲大D.甲和丙的溶质质量分数一定不相等
初中化学人教版九年级下册课题3 溶液的浓度课文ppt课件: 这是一份初中化学人教版九年级下册课题3 溶液的浓度课文ppt课件,共1页。
初中化学课题3 溶液的浓度多媒体教学课件ppt: 这是一份初中化学课题3 溶液的浓度多媒体教学课件ppt,共1页。
人教版九年级下册课题3 溶液的浓度评课课件ppt: 这是一份人教版九年级下册课题3 溶液的浓度评课课件ppt,文件包含1第1课时溶质的质量分数pptx、931有色溶液浓度的判断mp4等2份课件配套教学资源,其中PPT共15页, 欢迎下载使用。













