





初中化学人教版九年级下册课题3 溶液的浓度教学ppt课件
展开如何准确表示溶液的浓稀程度?
一定量的溶液里所含溶质的量。
1.定义:溶质的质量与溶液的质量之比2.定义式: 溶液的溶质质量分数= ×100%
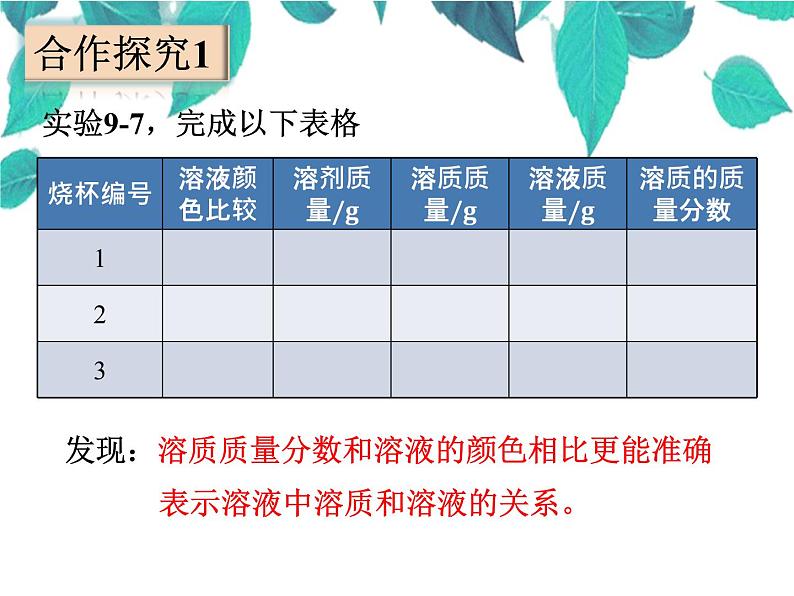
实验9-7,完成以下表格
发现:溶质质量分数和溶液的颜色相比更能准确 表示溶液中溶质和溶液的关系。
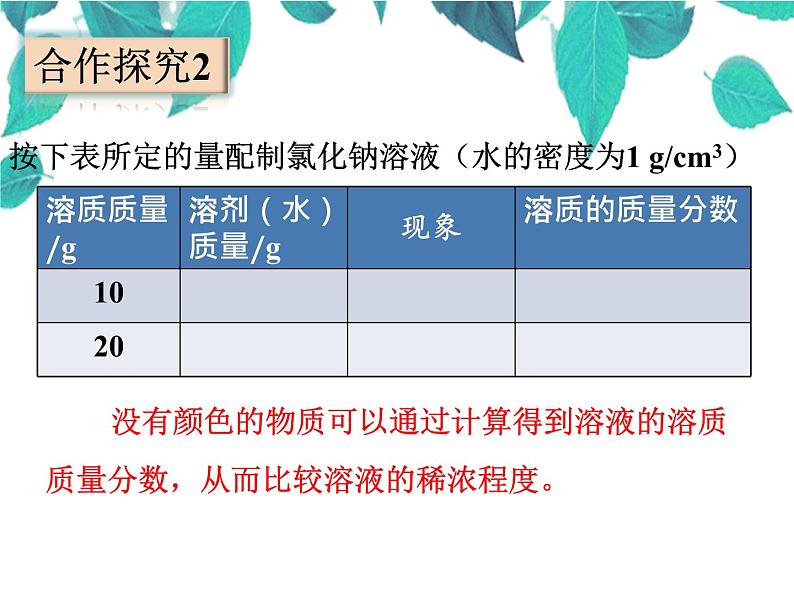
按下表所定的量配制氯化钠溶液(水的密度为1 g/cm3)
没有颜色的物质可以通过计算得到溶液的溶质质量分数,从而比较溶液的稀浓程度。
1.溶液参加化学反应,一般来讲真正反应的物质 是溶液中的溶质。2.在计算过程中对待溶液要一分为二,例如: 100 g 10%的氯化钠溶液。 一是溶质质量为:100 g×10% = 10 g; 二是溶剂质量为:100 g-10 g = 90 g。3.配制一定溶质质量分数的溶液步骤。
在农业生产中,常需要用质量分数为16%的氯化钠溶液选种。现需要配置150 kg这种溶液,需要氯化钠和水的质量各是多少?
解:溶质的质量分数= ×100%溶质质量=溶液质量×溶质的质量分数 =150 kg×16%=24 kg溶剂质量=溶液质量-溶质质量 =150 kg-24 kg=126 kg答:配置150 kg质量分数为16%的氯化钠溶液,需24 kg氯化钠和126 kg水。
化学实验室现有质量分数为98%的浓硫酸,但在实验室中常需要用较稀的硫酸。要把50 g上述浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
分析:溶液稀释前后,溶质质量不变。解 设:稀释后溶液的质量为 x。50 g×98%= x×20%解方程: x =245 g需要水的质量=245 g-50 g=195 g答:要把50 g质量分数为98%的硫酸稀释为 质量分数为20%的硫酸,需要水195 g。
100 g某硫酸溶液恰好与13 g锌完全反应。试计算这种硫酸溶液中溶质的质量分数。
x =19.6 g
答:这种硫酸溶液中溶质的质量分数为19.6%。
分析:与化学方程式结合起来的题目寻找溶质、溶剂、溶液的量。
配制一定溶质质量分数的溶液
1. 计算 2.称量 3.量取 4.溶解
托盘天平、药匙、量筒、玻璃杯、胶头滴管、烧杯
下图是小明配制100 g溶质质量分数为12%的NaCl溶液的有关实验操作示意图。 (1)配制过程中使用的四种玻璃仪器,分别是广口瓶、_______、 ________、______。(2)正确的操作顺序应该是____________。(3)请你指出图中一处错误操作,并分析该操作可能造成的后 果。______________________________________________。(4)图②、图③表示的操作步骤分别是____________。
称量过程中氯化钠和砝码放反,造成氯化钠质量偏小
1.向l00 g 10% NaOH溶液中加入12.5 g NaOH固体, 完全溶解后,所得溶液中溶质质量分数为( ) A.12. 5% B.20.0% C.22.5% D.25%
2.农业上常用16%的氯化钠溶液来选种。下列方法能 配制出该选种溶液的是( ) A.4 g氯化钠和16 g水 B.16 g 20%的氯化钠溶液和5 g水 C.10 g 8%的氯化钠溶液蒸发4 g水 D.14 g 10%的氯化钠溶液和1 g氯化钠
3. 有100 g 10%的食盐溶液,要使其质量分数变为 20%,有三种方法,按要求填空: (1)继续加入食盐,其质量为______g; (2)蒸发水分,其质量为____g; (3)与质量分数大于20%的浓食盐溶液混合,若混入 25%的食盐溶液,其溶液质量为____ g。
化学九年级下册课题3 溶液的浓度教课免费ppt课件: 这是一份化学九年级下册课题3 溶液的浓度教课免费ppt课件,共49页。PPT课件主要包含了实验9-7,分析实验结论,溶质质量,溶液质量,100%,溶质质量分数,实验9-8,溶质质量溶剂质量,实验用品,实验步骤等内容,欢迎下载使用。
人教版九年级下册课题3 溶液的浓度课文配套课件ppt: 这是一份人教版九年级下册课题3 溶液的浓度课文配套课件ppt,文件包含课题3溶质质量分数第1课时pptx、课题3溶质质量分数第3课时pptx、课题3溶质质量分数第2课时pptx、3份氯化钠加入不同量水中mp4、三种浓度不同的硫酸铜溶液剪后mp4、哪个更甜1勺2勺糖mp4、哪个更甜mp4、溶质质量分数的概念mp4等8份课件配套教学资源,其中PPT共54页, 欢迎下载使用。
初中化学课题3 溶液的浓度优秀课件ppt: 这是一份初中化学课题3 溶液的浓度优秀课件ppt,共60页。PPT课件主要包含了溶液的浓度,溶液的配制,实验步骤,过程方法,实验器材,注意事项,1计算,装瓶贴标签,固体+水,步6器8注意等内容,欢迎下载使用。













