

适用于新高考新教材2024版高考化学二轮复习热点提速练12电解原理的创新应用(附解析)
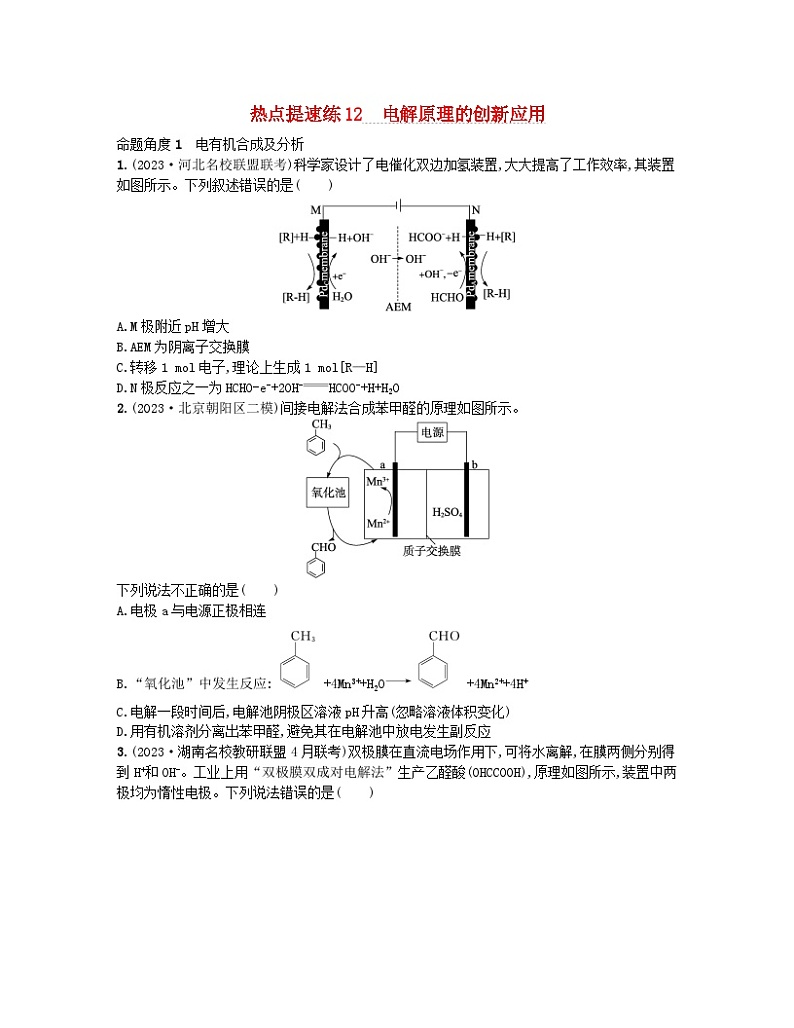
展开1.(2023·河北名校联盟联考)科学家设计了电催化双边加氢装置,大大提高了工作效率,其装置如图所示。下列叙述错误的是( )
A.M极附近pH增大
B.AEM为阴离子交换膜
C.转移1 ml电子,理论上生成1 ml[R—H]
D.N极反应之一为HCHO-e-+2OH-HCOO-+H+H2O
2.(2023·北京朝阳区二模)间接电解法合成苯甲醛的原理如图所示。
下列说法不正确的是( )
A.电极a与电源正极相连
B.“氧化池”中发生反应:+4Mn3++H2O+4Mn2++4H+
C.电解一段时间后,电解池阴极区溶液pH升高(忽略溶液体积变化)
D.用有机溶剂分离出苯甲醛,避免其在电解池中放电发生副反应
3.(2023·湖南名校教研联盟4月联考)双极膜在直流电场作用下,可将水离解,在膜两侧分别得到H+和OH-。工业上用“双极膜双成对电解法”生产乙醛酸(OHCCOOH),原理如图所示,装置中两极均为惰性电极。下列说法错误的是( )
A.a为阳极,b为阴极
B.b极上草酸发生的反应为H2C2O4+2e-+2H+OHCCOOH+H2O
C.HBr的作用是增强阳极液的导电能力和充当间接电氧化的媒介
D.两极均产生2.24 L(标准状况)气体时,理论上可得到乙醛酸7.4 g
4.(2023·河南名校联盟联考)近日,中国科学院大连化学物理研究所团队利用固体氧化物(γ-Al2O3)电解质实现了乙烷电化学脱氢制乙烯,其工作原理如图所示。下列说法正确的是( )
A.a为电源的负极
B.M极电极反应为C2H6+2e-C2H4+2H+
C.每生成0.5 ml C2H4,N极消耗标准状况下11.2 L CO2
D.每生成56 g CO,电路中转移电子的物质的量为2 ml
命题角度2 电解法制备无机物
5.(2023·北京房山区二模)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示:
下列说法不正确的是( )
A.电极a为阴极
B.金属锂在电极a上生成
C.电解过程中b极附近溶液pH逐渐减小
D.b极仅产生一种气体,电极反应为2Cl--2e-Cl2↑
6.(2023·湖南怀化二模)利用催化剂和电化学装置还原氮气制备铵盐和O2的原理如图所示。下列相关说法错误的是( )
A.B电极反应为2H2O-4e-O2↑+4H+
B.H+经过质子交换膜移向A电极
C.POM2在催化剂表面转化为POM1的反应为氧化反应
D.生成1 ml O2理论上可还原33.6 L N2(标准状况)
7.(2023·黑龙江哈尔滨二模)连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂。工业上常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正确的是( )
A.b电极应该接电源的负极
B.装置中所用离子交换膜为阴离子交换膜
C.电路中每转移1 ml e-消耗SO2的体积为11.2 L
D.a电极的电极反应为2HS+2e-+2H+S2+2H2O
命题角度3 电解法治理环境污染
8.(2023·广东汕头二模)间接电解法可对大气污染物NO进行无害化处理。其工作原理如图所示(质子膜只允许H+通过)。下列有关说法错误的是( )
A.电极b接电源正极,电解过程中附近溶液的pH增大
B.电极a的电极反应为2HS+2e-+2H+S2+2H2O
C.电解过程中右侧Na2SO4的浓度增大
D.电解过程中有4 ml H+通过质子膜时,可处理60 g NO
9.(2023·湖北联考协作体联考)用铁板作电极电解污水,可使其中的杂质离子转化为沉淀而除去,其电解装置如图所示。下列说法正确的是( )
A.a接电源负极,Y为阴离子交换膜
B.X溶液可能为NaOH溶液或者Na2SO4溶液
C.若处理含Cr2的污水,左池会生成Fe(OH)2和Cr(OH)3两种沉淀
D.若处理含Mn的污水,发生反应:5Fe2++Mn+4H2O5Fe3++Mn(OH)2↓+6OH-
10.(2023·福建莆田二模)铁碳微电解技术是处理酸性废水的一种工艺,装置如图所示。若上端口打开,并鼓入空气,可得到强氧化性中间体羟基自由基(·OH);若上端口关闭,可得到强还原性中间体氢原子(·H)。下列说法正确的是( )
A.无论上端口是关闭还是打开,正极反应均为Fe-2e-Fe2+
B.1 ml O2完全转化为羟基自由基(·OH)时转移2 ml电子
C.若处理含酚类的酸性废水,则上端口应关闭
D.若处理含Cr2的酸性废水,则上端口应打开并鼓入空气
热点提速练12 电解原理的创新应用
1.C 该装置为电解池,M为阴极,电极反应为[R]+H2O+e-[R—H]+OH-,生成OH-,碱性增强,附近pH增大,A正确;OH-从M极透过AEM膜进入N极,则AEM为阴离子交换膜,B正确;M极和N极都生成[R—H],由M极的[R]+H2O+e-[R—H]+OH-,N极[R]+H[R—H],可知转移1ml电子,理论上生成2ml[R—H],C错误;N为阳极,电极反应为HCHO-e-+2OH-HCOO-+H+H2O,D正确。
2.C 根据题图中信息可知,左侧a电极反应为Mn2+-e-Mn3+,为阳极,与电源正极相连,则b电极为阴极,电极反应为2H++2e-H2↑,阳极得到的Mn3+进入“氧化池”将甲苯氧化为苯甲醛,发生的反应为+4Mn3++H2O+4Mn2++4H+,A、B正确;电解过程中阴极b电极发生反应2H++2e-H2↑,同时电解质溶液中有等量的H+通过质子交换膜,从而电解池阴极区溶液pH几乎不变(忽略溶液体积变化),C错误;苯甲醛有强还原性,容易在电解池阳极上放电,所以用有机溶剂分离出苯甲醛,避免其在电解池中放电发生副反应,D正确。
3.D 根据图示,a极H2O生成O2,发生氧化反应,则a为阳极;b极H+生成H2,发生还原反应,则b为阴极,A正确;阴极上的反应为H2C2O4+2e-+2H+OHCCOOH+H2O、2H++2e-H2↑,B正确;OHCCHO属于非电解质,HBr的作用是增强阳极液的导电能力,Br-在阳极发生失电子的氧化反应生成Br2,Br2将OHCCHO氧化为OHCCOOH,HBr充当间接电氧化的媒介,C正确;当阳极生成标准状况下2.24LO2时,转移电子物质的量为0.4ml,生成乙醛酸aml,当阴极b极生成标准状况下2.24LH2时,转移电子物质的量为0.2ml,生成乙醛酸bml,根据电子守恒可得:×4+2aml=×2+2bml,解得b-a=0.1,理论上可得到乙醛酸的质量一定大于0.1ml×74g·ml-1=7.4g,D错误。
4.C M电极乙烷发生氧化反应生成乙烯,M为阳极,a为电源的正极,A错误;M极乙烷失电子发生氧化反应生成乙烯,反应为C2H6+O2--2e-C2H4+H2O,B错误;阳极发生反应C2H6+O2--2e-C2H4+H2O,阴极发生反应CO2+2e-CO+O2-,每生成0.5mlC2H4,转移1ml电子,N极消耗0.5mlCO2,标准状况下的体积为11.2L,C正确;阴极发生反应CO2+2e-CO+O2-,每生成56gCO,电路中转移电子的物质的量为×2=4ml,D错误。
5.D 电子由负极经外电路流入电极a,电极a为阴极,A正确;锂离子透过选择性膜向a极迁移,金属锂在电极a上生成,B正确;电极b发生反应2Cl--2e-Cl2↑,还会发生反应2H2O-4e-O2↑+4H+,使得b极附近溶液pH逐渐减小,有两种气体产生,C正确,D错误。
6.D B为电解池阳极,H2O在B电极失电子发生氧化反应生成氧气,电极反应为2H2O-4e-O2↑+4H+,A正确;A电极为电解池阴极,B为电解池阳极,根据离子迁移规律,氢离子由阳极移向阴极,即由B电极经过质子交换膜移向A电极,B正确;A电极为电解池阴极,电解液中POM1得电子转化为POM2的过程为还原反应,则POM2在催化剂表面转化为POM1的反应为氧化反应,C正确;B电极反应为2H2O-4e-O2↑+4H+,生成1mlO2转移4ml电子,N2转化为N的过程中N元素由0价下降到-3价,当转移4ml电子时可还原mlN2,标准状况下的体积为ml×22.4L·ml-1≈14.9L,D错误。
7.D 由装置图中物质转化关系可知,左边由NaHSO3得到电子转化为Na2S2O4,右边由SO2失去电子转化为H2SO4,则a电极接电源的负极,b电极接电源的正极,A错误;a电极的反应为2HS+2e-+2H+S2+2H2O,b电极的反应为SO2+2H2O-2e-S+4H+,则装置中离子交换膜为阳离子交换膜,B错误,D正确;由电极反应可知,每转移1mle-消耗SO20.5ml,但没有给气体的温度和压强,故SO2气体的体积无法计算,C错误。
8.A 由装置可知,电极b上水放电生成氧气,电极反应为2H2O-4e-O2↑+4H+,电极b附近溶液的pH减小,A错误;电极a上发生反应HS转化为S2,电极反应为2HS+2e-+2H+S2+2H2O,B正确;电极b上水放电生成氧气,反应生成的氢离子通过质子膜进入左侧,电解过程中损失水,则右侧Na2SO4的浓度增大,C正确;电解过程中有4mlH+通过质子膜时,电路中转移4ml电子,则生成2mlS2,S2与NO反应生成氮气和HS,反应为2S2+2NO+2H2O4HS+N2,2mlS2可处理2mlNO,质量为60g,D正确。
9.B 右池产生氢气,右侧铁板为电解池阴极,左侧铁板为电解池阳极,所以a接电源正极,左侧生成的Fe2+与污水中离子反应,右侧产生的OH-向左侧做定向移动,Y为阴离子交换膜,A错误;右侧放氢气生成碱,X溶液可能为NaOH溶液或者Na2SO4溶液,B正确;若处理含Cr2的污水,发生反应Cr2+6Fe2++10OH-+7H2O6Fe(OH)3↓+2Cr(OH)3↓,左池会生成Fe(OH)3和Cr(OH)3两种沉淀,C错误;若处理含Mn的污水,发生反应5Fe2++Mn+9OH-+4H2O5Fe(OH)3↓+Mn(OH)2↓,D错误。
10.B 正极发生得电子的反应,负极发生失电子的氧化反应,无论是否鼓入空气,Fe易失去电子生成Fe2+,作负极,电极反应为Fe-2e-Fe2+,A错误;若上端口打开,并鼓入空气,可得到强氧化性的羟基自由基,电极反应为2H++2e-+O22·OH,故1mlO2完全转化为羟基自由基(·OH)时转移2ml电子,B正确;除去含酚类的酸性废水,需要氧化性的物质,上端口需要打开,可生成羟基自由基氧化酚类,C错误;Cr2在酸性条件下具有强氧化性,需要还原剂,则上端口需要关闭,可得到强还原性中间体氢原子(·H),D错误。
适用于新高考新教材2024版高考化学二轮复习热点提速练14电解质溶液中的图像及分析(附解析): 这是一份适用于新高考新教材2024版高考化学二轮复习热点提速练14电解质溶液中的图像及分析(附解析),共8页。试卷主要包含了常温下,分别用0,1×10-3、6,常温下,用0,25 ℃时,向0,61 ml·L-1,二元有机酸的电离常数=1等内容,欢迎下载使用。
适用于老高考旧教材2024版高考化学二轮复习热点提速练11电解原理的创新应用(附解析): 这是一份适用于老高考旧教材2024版高考化学二轮复习热点提速练11电解原理的创新应用(附解析),共7页。
适用于老高考旧教材2024版高考化学二轮复习热点提速练12电解质溶液中的图像及分析(附解析): 这是一份适用于老高考旧教材2024版高考化学二轮复习热点提速练12电解质溶液中的图像及分析(附解析),共7页。试卷主要包含了05 ml·L-1,25,已知,22,赖氨酸等内容,欢迎下载使用。












