

陕西省渭南市尚德中学2023-2024学年高三上学期期中考试化学试卷(含答案)
展开
这是一份陕西省渭南市尚德中学2023-2024学年高三上学期期中考试化学试卷(含答案),共12页。试卷主要包含了5),下列说法错误的是,下列化学用语使用正确的是,设为阿伏加德罗常数的值,下列各组物质的鉴别方法错误的是,用下列仪器或装置,丁位辛内酯H可作为一种食品香料等内容,欢迎下载使用。
(可能用到的相对原子质量: H 1 — B 11 — C 12 — N 14 — O 16 — Na 23 — S 32 — Cl 35.5)
一、选择题:(本题共14个小题,每小题3分。共42分,在每小题给出的四个选项中,只有一项是符合题目要求的。)
1.下列说法错误的是( )
A.华为麒麟990芯片采用7nm工艺,芯片的主要成分为晶体硅
B.分解时吸收大量的热,可用作阻燃剂
C.生产N95口罩的核心材料聚丙烯属于无机非金属材料
D.白葡萄酒含维生素C等多种营养成分,通常添加微量的,目的是防止营养成分被氧化
2.下列化学用语使用正确的是( )
A.在氮原子中,质子数为7而中子数不一定为7
B.的乙醇和丙醇混合液完全燃烧生成的为 (标准状况)
C.的电子式为
D.的结构示意图为
3.《本草纲目》中“石碱”条目下写道:“出山东济宁诸处。彼人采蒿蓼之属,开窖浸水,漉起,晒干烧灰,以原水淋汁,每百引入粉面二、三斤,久则凝淀如石,连汁货之四方,浣衣发面……”下列说法错误的是( )
A.“以原水淋汁”涉及的分离操作是浸取、过滤
B.“浣衣发面”中利用了石碱的碱性
C.“久则凝淀如石”是结晶析出的过程
D.“石碱”的主要成分是KOH
4.设为阿伏加德罗常数的值。和在一定条件下发生反应:。下列叙述错误的是( )
A.上述反应生成时断裂H—N键的数目为
B.(标准状况)参与反应时生成氧化产物的分子数为
C.11.2L(标准状况)还原剂反应时转移的电子数为
D.常温下,参与反应时,生成还原产物的分子数为
5.某天然有机物M具有抗肿瘤生物活性的作用,其结构如图所示,下列有关M的说法正确的( )
A.含3种官能团
B.遇溶液会发生显色反应
C.能发生氧化、取代、加成、消去反应
D.分子中至少有11个碳原子一定共面
6.能正确表示下列反应的离子方程式是( )
A.向次氯酸钙溶液通入过量CO2∶Ca2++2ClO-+H2O+CO2===CaCO3↓+2HClO
B.向次氯酸钙溶液通入SO2∶Ca2++2ClO-+H2O+SO2===CaSO3↓+2HClO
C.氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO3-===CaCO3↓+H2O
D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-===3Fe3++2H2O+NO↑
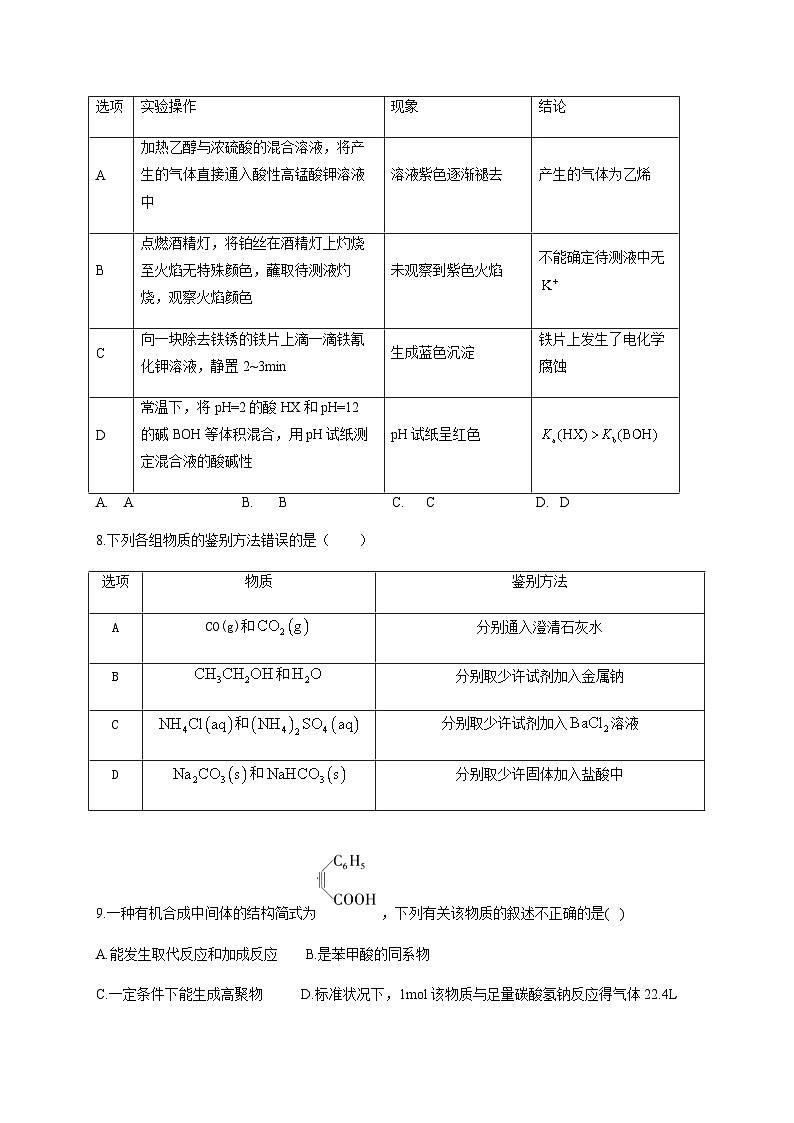
7.由下列实验操作及现象能得出相应结论的是( )
A B. B C. C D. D
8.下列各组物质的鉴别方法错误的是( )
9.一种有机合成中间体的结构简式为,下列有关该物质的叙述不正确的是( )
A.能发生取代反应和加成反应 B.是苯甲酸的同系物
C.一定条件下能生成高聚物 D.标准状况下,1ml该物质与足量碳酸氢钠反应得气体22.4L
10.用下列仪器或装置(图中部分夹持装置已省略)进行相应实验,能达到实验目的的是( )
11..某小组为了探究KI的性质,设计了如下实验:(注:实验Ⅳ在实验Ⅲ反应后的基础上进行。)
下列推断正确的是( )
A.实验I、Ⅱ发生反应的离子方程式相同 B.实验Ⅱ足以说明
C.由实验Ⅲ知,还原性: D.由实验Ⅳ知:具有氧化性
12.一种安全、低成本、快速动力学和低应变的无机框架钾离子电池正极材料结构如图所示,X、Y、Z、Q、W是原子序数依次增大的短周期主族元素且X、Y、Z、Q在同一周期,Z、W在同一主族。下列说法正确的是( )
A.最高正价:Q>Z=W>Y>X
B.简单氢化物的稳定性:Q>Z>Y>X
C.该离子导体中含有离子键、极性共价键、非极性共价键
D.该离子导体中各原子最外层均达到了8电子稳定结构
13.铁粉与稀硝酸反应的化学方程式为。下列有关说法正确的是( )
A.作氧化剂的是参与反应的HNO的10%
B.若铁粉过量,则氧化剂与还原剂的物质的量之比为3:8
C.氧化性:
D.在反应后的混合物中滴加少量氢氧化钠溶液,有气体逸出
14.利用假单胞菌分解有机物的电化学原理如图所示。下列说法正确的是( )
A.该电池能在高温下工作 B.该电池工作时,电流由A电极经用电器流入B电极
C.A电极是负极,电极反应式为 D.电池工作过程中,从右室透过质子交换膜移动到左室
二、非选择题:(共58分)
15.(16分)某小组设计实验探究的性质,装置如图所示。
观察到的实验现象如下:
已知:NO能被酸性氧化成,与碱石灰不反应。
回答下列问题:
(1)实验室制宜选择下列试剂中的______(填标号)。
A.粉末和浓硝酸D.粉末和10%盐酸
B.粉末和70%浓硫酸C.粉末和30%稀硝酸
(2)依据实验现象判断在______(填化学式)存在下表现漂白性,预测C中现象是______。
(3)D中产生的白色沉淀是______(填化学式),D中发生反应的离子方程式为______。
(4)E中现象表明具有的性质是______(填标号)。
a.漂白性b.酸性c.氧化性d.还原性
(5)为了证明的漂白性是暂时性的,请设计一个补充实验:______。
(6)为处理上述实验尾气,下列装置中可供选择的是______(填标号)。
16.(14分)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如图所示:
已知:最高价含铬酸根在酸性介质中以形式存在,在碱性介质中以形式存在。
回答下列问题:
若铬钒渣中铬的含氧酸盐为,则“煅烧”过程中发生反应的化学方程式为________。若在实验室中进行煅烧铬钒渣,________(填“能”或“不能”)用陶瓷坩埚,理由是________。
(2)是________(填“酸性”、“碱性”或“两性”)氧化物,写出它在日常生活中的一种用途:________。
(3)“沉淀”步骤中生成反应的离子方程式为________。
(4)“还原”步骤中氧化剂与还原剂的物质的量之比为________。
17.(12分)氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
(1).Ⅰ、根据图1数据计算反应的__________。
Ⅱ、在一定温度、催化剂存在的条件下,密闭容器中CO与转化为与,相关反应如下:
①
②
③
(1)则反应I:的_________。
2)合成氨工厂以“水煤气”和为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、、、的混合气体,在反应器A进行合成氨,其催化剂Ⅲ铁触媒,在500℃活性最大,反应器B中主要发生的反应为,装置如图2。
19题图2
①温度比较:气流a 气流b(填“>”“<”或“=”)。
②气体流速一定,经由催化剂Ⅰ到催化剂Ⅱ,原料转化率有提升,其可能原因是: 。
③下列说法正确的是 。
A.合成氨是目前自然固氮最重要的途径
B.利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气流速,有利于水煤气生成
C.体系温度升高,可能导致催化剂失活,用热交换器将原料气可预热并使反应体系冷却
D.终端出口2得到的气体,通过液化可分离出
(3)LiH-3d过渡金属复合催化剂也可用于催化合成氨,已知先被吸附发生反应,紧接着被吸附发生的反应方程式 。
18(16分).丁位辛内酯H()可作为一种食品香料。其合成路线为:
回答下列问题:
(1)A的化学名称是________________。A的两种同分异构体结构分别为和,其沸点M________________N(填“高于”或“低于”)。
(2)写出反应D→E的化学方程式________________。
(3)E具有的官能团名称是________________。
(4)反应B→C中,X的结构简式为________________。
(5)E→F的反应类型是________________。
(6)Q是B的同分异构体,满足下列条件的Q的结构共有________________种(不考虑同一碳原子上存在两个双键的情况)。
①Q中不含环和三键;②能与NaOH溶液反应但不能与NaHCO3溶液反应;③不能发生银镜反应若Q有下列转化关系:一定条件下氧化,则Q的结构简式是________________。
化学答案
1.C 2.A 3.D 4.B 5.D 6.D 7.B 8.D 9.B 10.C 11.C 12.B 13.A 14.C
15.(16分)(1)B (2);紫色石蕊溶液变红
(3)(1分);
(4)c
(5)微热装置B,溶液变红
(6)D
16(14分)(1)(或,或其他合理答案,;
不能;
、NaOH均能与陶瓷坩埚中的发生反应(或其他合理答案,
(2)碱性;用作红色颜料
(3)
(4)2:3
17(12分).(1)① ②
(2)①<
②气流若在催化剂Ⅰ层达平衡流出,经中间热交换,温度降低,反应平衡正移,转化率增大;气流若在催化剂Ⅰ层未达平衡,则与催化剂Ⅱ接触,继续反应,转化率增大③BCD
(3)
18(16分).答案:(1)间苯二酚(或1,3-苯二酚);高于
(2)
(3)羰基、酯基)
(4)
(5)还原反应
(6) 10 ; 选项
实验操作
现象
结论
A
加热乙醇与浓硫酸的混合溶液,将产生的气体直接通入酸性高锰酸钾溶液中
溶液紫色逐渐褪去
产生的气体为乙烯
B
点燃酒精灯,将铂丝在酒精灯上灼烧至火焰无特殊颜色,蘸取待测液灼烧,观察火焰颜色
未观察到紫色火焰
不能确定待测液中无
C
向一块除去铁锈的铁片上滴一滴铁氰化钾溶液,静置2~3min
生成蓝色沉淀
铁片上发生了电化学腐蚀
D
常温下,将pH=2的酸HX和pH=12的碱BOH等体积混合,用pH试纸测定混合液的酸碱性
pH试纸呈红色
选项
物质
鉴别方法
A
CO(g)和
分别通入澄清石灰水
B
和
分别取少许试剂加入金属钠
C
和
分别取少许试剂加入溶液
D
和
分别取少许固体加入盐酸中
A
B
C
D
除去中少量的
利用铜和稀硝酸反应,制取、净化、收集NO
测量的体积
分离苯和溴苯
操作图示
实验
试剂X
现象
Ⅰ
溶液
产生黄色沉淀
Ⅱ
浊液
产生黄色沉淀
Ⅲ
溶液和淀粉溶液
溶液变为蓝色
Ⅳ
溶液
溶液由蓝色变为无色
装置标号
A
B
C
D
E
现象
溶液不褪色
溶液变无色
?
产生白色沉淀
产生黄色浑浊
相关试卷
这是一份陕西省渭南市尚德中学2023-2024学年高二上学期期中质量检测化学试卷(含答案),共7页。试卷主要包含了选择题等内容,欢迎下载使用。
这是一份陕西省渭南市尚德中学2022-2023学年高二上学期期中质量检测化学试题(Word版含答案),共9页。试卷主要包含了单选题等内容,欢迎下载使用。
这是一份2021渭南尚德中学高二下学期第二次质量检测化学试卷含答案









