



高中化学人教版 (2019)选择性必修3第二节 烯烃 炔烃教学课件ppt
展开
这是一份高中化学人教版 (2019)选择性必修3第二节 烯烃 炔烃教学课件ppt,共24页。PPT课件主要包含了学习目标,新课导入,产生了大量的乙炔气体,知识点一,乙炔C2H2,乙炔的组成与结构,球棍模型,空间充填模型,思考讨论,直线型键角1800等内容,欢迎下载使用。
1.通过乙炔的物理性质的学习,了解炔烃的物理性质及其变化规律。2.通过学习乙炔的结构,能从化学键的饱和性等微观角度理解炔烃的结构特点。3.通过学习乙炔的化学性质,掌握炔烃的化学性质。4.通过乙炔的实验室制法的探究,掌握一般物质制备的流程。
观看电石(CaC2)遇水反应的实验视频,分析爆炸原因
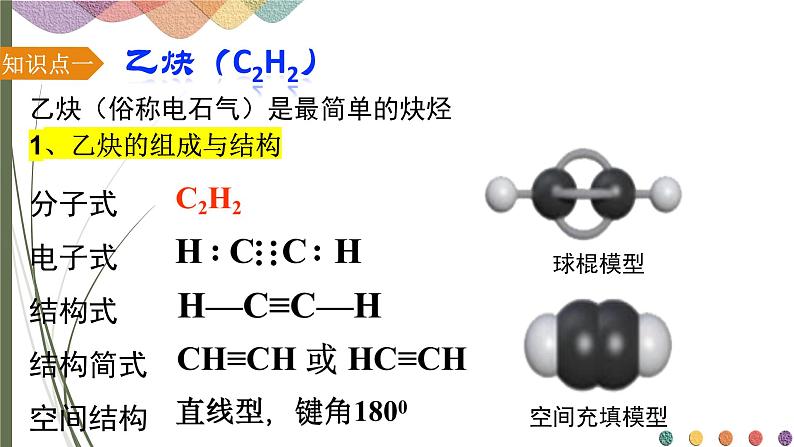
乙炔(俗称电石气)是最简单的炔烃
分子式电子式结构式结构简式空间结构
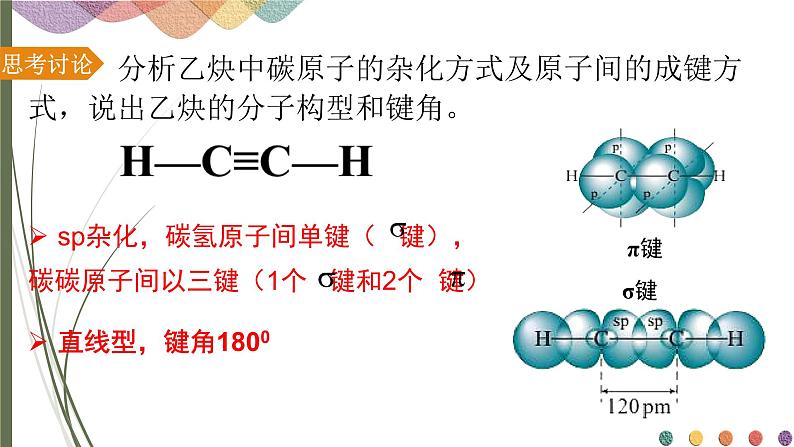
分析乙炔中碳原子的杂化方式及原子间的成键方式,说出乙炔的分子构型和键角。
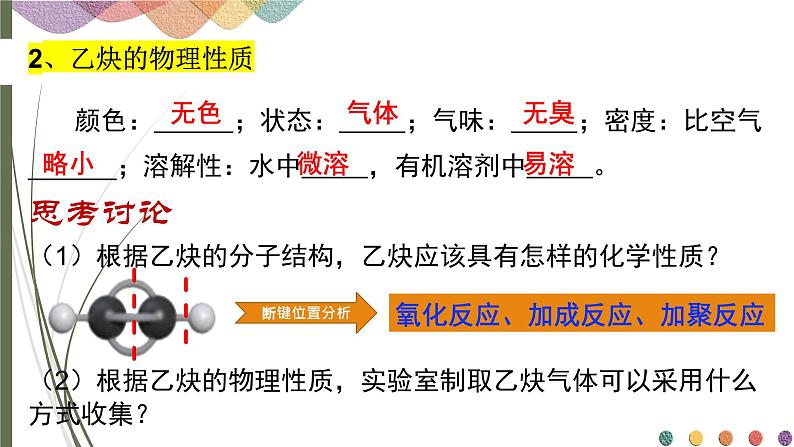
颜色: ;状态: ;气味: ;密度:比空气______;溶解性:水中 ,有机溶剂中 。
(1)根据乙炔的分子结构,乙炔应该具有怎样的化学性质?
(2)根据乙炔的物理性质,实验室制取乙炔气体可以采用什么方式收集?
氧化反应、加成反应、加聚反应
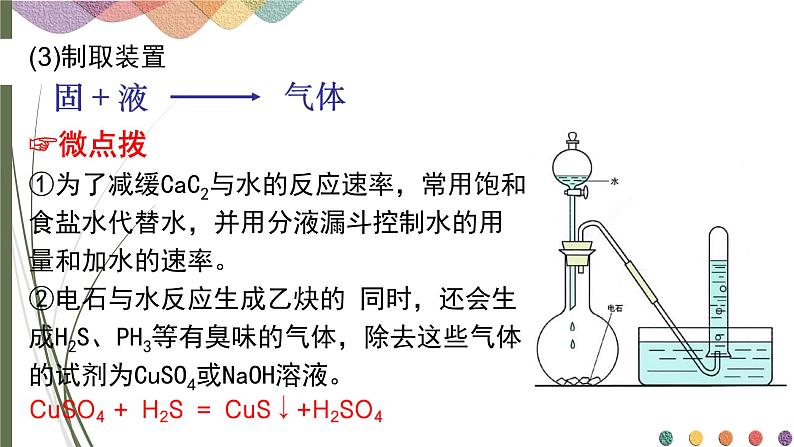
「资料」阅读教材P37,总结实验室制备乙炔的实验原理,实验试剂,并选择合适的发生装置。
碳化钙(CaC2),俗名电石,常含有磷化钙,硫化钙等杂质
☞微点拨①为了减缓CaC2与水的反应速率,常用饱和食盐水代替水,并用分液漏斗控制水的用量和加水的速率。②电石与水反应生成乙炔的 同时,还会生成H2S、PH3等有臭味的气体,除去这些气体的试剂为CuSO4或NaOH溶液。
能否用启普发生器制取乙炔?
(1)碳化钙吸水性强,与水蒸气也能剧烈反应,因此不能随开随用、随关随停。(2)反应过程中放出大量的热,易使启普发生器炸裂。(3)生成的Ca(OH)2呈糊状,易堵塞球形漏斗或导气管。
与制CO2、H2、H2S相似,但不可用启普发生器。
反应装置作用:产生乙炔。
除杂装置作用:除去杂质H2S、PH3。
检验装置作用:检验乙炔是否产生。
反应装置作用:乙炔与溴的四氯化碳溶液反应。
尾气处理装置点燃前需验纯作用:去除未反应的乙炔。
反应剧烈,放热,有其他产生
乙炔跟空气的混合物遇火会发生爆炸,在生产和使用乙炔时,点燃前要验纯!
②使酸性KMnO4溶液褪色
2KMnO4+ 3H2SO4+ C2H2→ 2MnSO4+ K2SO4+2CO2↑+ 4H2O
含碳量不同导致燃烧现象有所不同,可用于三者鉴别
与溴水、X2、H2、HCN、HX、H2O等在一定条件下发生加成反应
1 , 2 —二溴乙烯
1 , 1 , 2 , 2 —四溴乙烷
乙炔与水加成后的产物乙烯醇(CH2=CH—OH不稳定,很快转化为乙醛)
⑴乙炔是一种重要的基本有机原料,可以用来制备氯乙烯、聚氯乙烯和乙醛等。
⑵乙炔燃烧时产生的氧炔焰可用来切割或焊接金属。
分子里含有-C≡C-的不饱和链烃叫炔烃。
CnH2n-2(n≥2)
(2)链状单炔烃的通式
CH ≡ CCH2CH2CH3
CH3C ≡ CCH2CH3
炔烃物理性质的递变与烷烃烯烃的相似
颜色:无色溶解性:难溶于水密度:均小于水熔沸点:一般随着分子中碳原子数n的增加而升高;同碳时,支链越多熔沸点越低状态:一般随着分子中碳原子数的增加,在常温下的状态由气态变为液态,再到固态
炔烃的结构和性质与乙炔的相似
烷烃、烯烃和炔烃的化学性质
甲烷、乙烯、乙炔均为常见的有机化工原料,现将三种气体均分别燃烧、通入酸性高锰酸钾溶液、通入溴的四氯化碳溶液。问题1:燃烧前是否都要验纯?燃烧时的现象有什么不同?问题2:酸性高锰酸钾溶液都褪色吗?为什么?问题3:溴的四氯化碳溶液都褪色吗?为什么?
提示:是,可燃性气体燃烧前都需要验纯。含碳量越高,火焰越亮,烟越浓
提示:通入甲烷的不褪色,通入乙烯和乙炔的均褪色。因为乙烯和乙炔中含有不饱和碳原子,能被高锰酸钾氧化。
提示:通入甲烷的不褪色,通入乙烯和乙炔的均褪色。因为乙烯和乙炔中含有不饱和碳原子,能与溴发生加成反应。
烷烃、烯烃、炔烃的结构和化学性质的比较
1.(2022·山东青岛期末)下列关于乙炔的化学性质说法不正确的是( )A.乙炔与氢气加成的产物不一定是乙烯B.乙炔与氯化氢反应的产物可能是氯乙烯C.乙炔与氯化氢反应的产物也可能是氯乙烷D.乙炔也能发生聚合反应
2.(2021·河北张家口期末)两分子乙炔在一定条件下可生成乙烯基乙炔(HC≡C—CH CH2)。下列关于乙烯基乙炔的说法错误的是( )A.能使酸性KMnO4溶液褪色B.能发生加聚反应生成高分子化合物C.分子中所有碳原子都在一条直线上D.没有顺反异构现象
相关课件
这是一份高中化学人教版 (2019)选择性必修3第二节 烯烃 炔烃优秀ppt课件,共83页。PPT课件主要包含了第一部分炔烃的结构,知识新授,炔烃的结构,碳碳三键,-C≡C-,-2H,单烯烃CnH2n,单炔烃,直线形,键能kJmol等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修3第二节 烯烃 炔烃优质ppt课件,共40页。
这是一份2020-2021学年第二章 烃第二节 烯烃 炔烃课文内容ppt课件,共8页。










