
江苏省江阴市华士高级中学2023-2024学年高一上学期12月学情调研化学试卷
展开命题人: 复核人:
考生注意:
1、可能用到的相对原子质量:H 1 C 12 O 16 Na23 Cl 35.5 K 39 Mn 55 Fe 56
2、客观题请用2B铅笔填涂在答题卡上,主观题用黑色的水笔书写在答题卷上。
选择题(共42分)
一、单项选择题:本题共14小题,每小题3分,共42分。
1. 2022年11月29日,神舟十五号载人飞船成功发射。下列说法不正确的是
A. 飞船外壳材料使用的是钛合金,其熔点高于纯钛
B. 新一代运载火箭使用的液氢和液氧均为非金属单质
C. 光束通过空间站使用的纳米气凝胶时,可观察到丁达尔效应
D. 空间站使用石墨烯存储器,石墨烯与金刚石互为同素异形体
2. 工业上通过反应制备。下列说法正确的是
A. Cl-结构示意图:B. Cl2的电子式:
C. 中子数为10的氧原子:D. NaOH的电离方程式:
盐酸
3. 下列选项所示的转化在指定条件下能够实现的是
A Fe(s)Fe2O3(s) ─────→FeCl3
B. O3
C
D.
4. 下列物质中,既含有离子键又含有共价键的是
A. B. C. D.
5. 下列指定反应的离子方程式正确的是
A. 片投入足量稀盐酸:2Fe+6H+=2Fe3++3H2↑更多课件教案等优质滋元可 家 威杏 MXSJ663 B 片投入溶液中:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
C. 稀溶液中通入少量:
D. 溶液中加入稀硫酸:
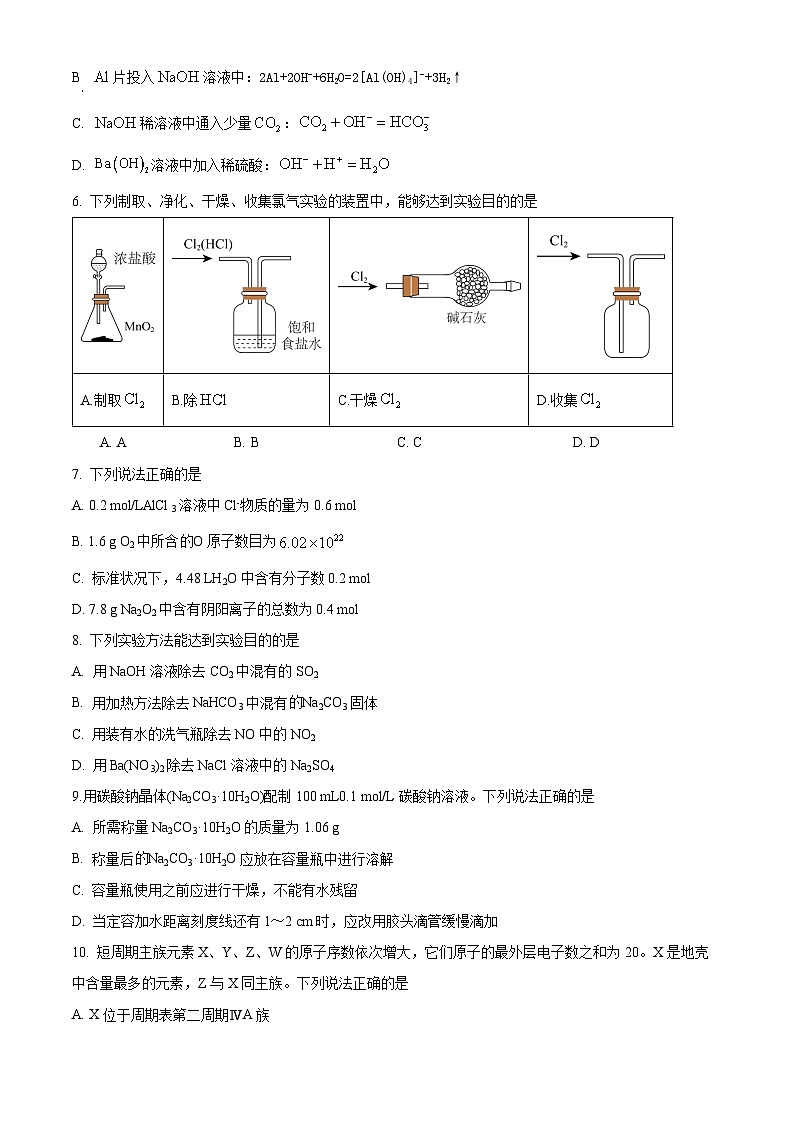
6. 下列制取、净化、干燥、收集氯气实验的装置中,能够达到实验目的的是
A. AB. BC. CD. D
7. 下列说法正确的是
A. 0.2 ml/LAlCl3溶液中Cl-物质的量为0.6 ml
B. 1.6 g O2中所含O原子数目为
C. 标准状况下,4.48 LH2O中含有分子数0.2 ml
D. 7.8 g Na2O2中含有阴阳离子的总数为0.4 ml
8. 下列实验方法能达到实验目的的是
A. 用NaOH溶液除去CO2中混有的SO2
B. 用加热方法除去NaHCO3中混有Na2CO3固体
C. 用装有水的洗气瓶除去NO中的NO2
D. 用Ba(NO3)2除去NaCl溶液中的Na2SO4
9.用碳酸钠晶体(Na2CO3·10H2O)配制100 mL0.1 ml/L碳酸钠溶液。下列说法正确的是
A. 所需称量Na2CO3·10H2O的质量为1.06 g
B. 称量后Na2CO3·10H2O应放在容量瓶中进行溶解
C. 容量瓶使用之前应进行干燥,不能有水残留
D. 当定容加水距离刻度线还有1~2 cm时,应改用胶头滴管缓慢滴加
10. 短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为20。X是地壳中含量最多的元素,Z与X同主族。下列说法正确的是
A. X位于周期表第二周期ⅣA族
B. 原子半径:r(X)
D. W的最高价氧化物对应水化物的酸性比Z的强
11. 室温下,下列实验探究方案能达到探究目的的是
A. AB. BC. CD. D
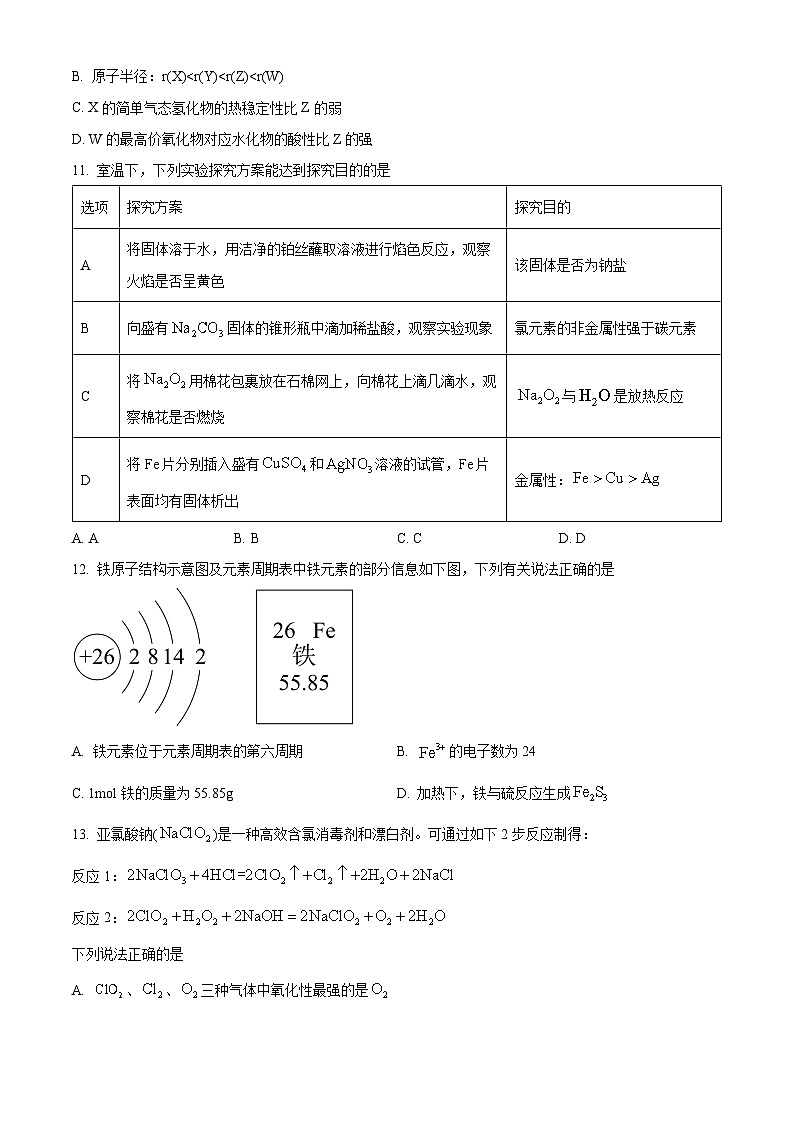
12. 铁原子结构示意图及元素周期表中铁元素的部分信息如下图,下列有关说法正确的是
A. 铁元素位于元素周期表的第六周期B. 的电子数为24
C. 1ml铁的质量为55.85gD. 加热下,铁与硫反应生成
13. 亚氯酸钠()是一种高效含氯消毒剂和漂白剂。可通过如下2步反应制得:
反应1:
反应2:
下列说法正确的是
A. 、、三种气体中氧化性最强的是
B. 反应1中只表现出还原性
C. 反应2中作还原剂,被氧化
D. 反应1中中的元素均来自于
14. 对FeCl3溶液腐蚀铜线路板后产生废液X进行回收处理,流程如下图。下列说法正确的是
A. 废液X中一定存在
B. 溶液B为FeCl3溶液
C. 实验室中进行操作①②时,需用到的玻璃仪器有烧杯、分液漏斗和玻璃棒
D. 将操作②得到的Cu与溶液A混合,充分反应后,所得溶液与废液X成分完全相同
非选择题(共4大题,共58分)
15.(14分)利用分类和氧化还原反应的知识能实现物质的转化。
(1)请从下列试剂中选择最合适的完成指定转化(试剂可以重复选择)。
试剂:溶液、氨水、溶液、溶液、溶液、稀盐酸、AlCl3溶液
①溶液→溶液的离子方程式: 。
②溶液溶液的化学方程式: 。
③NH3→NH4+的离子方程式: 。
④Na2CO3溶液与稀盐酸反应的离子方程式: 。
⑤AlCl3溶液与氨水反应的离子方程式: 。
(2)生物浸出法可有效回收含硫矿石中的有色金属,酸性条件下,某生物浸出法主要物质转化如图。
①步骤Ⅰ发生反应的离子方程式为 。
②步骤Ⅱ发生反应的离子方程式为 。
16.(14分)下图是元素周期表的一部分。按要求填写下列空白:
(1)元素⑤在周期表中的位置为 ;
(2)①~⑧元素的最高价氧化物中,具有两性的是___________(填化学式);
(3)元素⑦的最简单气态氢化物的电子式是___________;元素③形成单质的电子式 。
(4)④、⑤、⑥、⑦对应简单离子的半径最小的是___________(填离子符号);
(5)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式 ;
(6)下列方案中不能证明非金属性⑧比⑦强的是___________(填选项字母)。
A. 最高价氧化物对应水化物的酸性⑧比⑦的强
B. 单质与变价金属反应,产物的价态⑧比⑦的高
C. 简单气态氢化物对应水溶液的酸性⑧比⑦的强
D. ⑧的单质可将⑦的单质从其化合物中置换出来
17.(16分)海水是资源的宝库,以海水为原料可以制取粗盐、Br2等多种物质。
(1)粗盐中主要含NaCl,还含有少量CaCl2、MgCl2和Na2SO4。可选择的试剂:碳酸钠溶液、氢氧化钠溶液、氯化钡溶液。
①将粗盐提纯的方法是:将粗盐溶于水,向里面依次加入稍过量的 , , (填
依次加入试剂的化学式),过滤,将滤液用盐酸酸化后,蒸发结晶。
②实验中,加过量碳酸钠溶液的目的是 。
(2)浓缩海水中含有NaCl、NaBr等物质。从浓缩海水中提取溴的流程如下:
①写出“氧化Ⅰ”反应的离子方程式: 。
②“吸收”时是用SO2水溶液吸收空气吹出的溴蒸汽。写出“吸收”时(产物中生成两种强酸,其中一种为硫酸)发生反应的化学方程式 ,并在你所写的化学方程式上用单线桥标出电子转移的方向和数目。
③“蒸馏”时单质溴从溶液中蒸出,蒸馏后所剩溶液中的溶质是_______。
18.( 14分)纯碱在纺织、肥皂、造纸、玻璃、火药等行业有着广泛的应用,人类在制碱方法的工业化道路上不断探索。“索尔维制碱法”以、、和水等为原料获得和。
某化学小组用如图装置进行模拟实验。
(1)配制溶液所需要的玻璃仪器有量筒、烧杯、胶头滴管、_______、_______。
(2)装置丙需控制温度在30~35℃,实验中可采取的加热方法是_______。
(3)饱和食盐水中先通入后通入的原因是 。
(4)写出在丙装置中发生的化学方程式: 。
(5)写出转化为的方程式: 。
(6)由装置丙中产生的制取时,需要进行的实验操作有过滤、洗涤、灼烧,其中检验洗涤是否干净的操作是 。A.制取
B.除
C.干燥
D.收集
选项
探究方案
探究目的
A
将固体溶于水,用洁净的铂丝蘸取溶液进行焰色反应,观察火焰是否呈黄色
该固体是否为钠盐
B
向盛有固体的锥形瓶中滴加稀盐酸,观察实验现象
氯元素的非金属性强于碳元素
C
将用棉花包裹放在石棉网上,向棉花上滴几滴水,观察棉花是否燃烧
与是放热反应
D
将Fe片分别插入盛有和溶液的试管,Fe片表面均有固体析出
金属性:
①
②
③
④
⑤
⑥
⑦
⑧
江苏省江阴市某校2023-2024学年高二上学期12月学情调研化学(选修)试卷含答案: 这是一份江苏省江阴市某校2023-2024学年高二上学期12月学情调研化学(选修)试卷含答案,共9页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
江苏省江阴市2023-2024学年高二上册12月学情调研化学(选修)试卷(附答案): 这是一份江苏省江阴市2023-2024学年高二上册12月学情调研化学(选修)试卷(附答案),共9页。
江苏省江阴市华士高级中学2023-2024学年高二上学期12月学情调研化学(选修)试卷: 这是一份江苏省江阴市华士高级中学2023-2024学年高二上学期12月学情调研化学(选修)试卷,共7页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。












