

所属成套资源:统考版2024届高考化学二轮专项分层特训卷多份(附解析)
统考版2024届高考化学二轮专项分层特训卷仿真模拟冲刺标准练三(附解析)
展开
这是一份统考版2024届高考化学二轮专项分层特训卷仿真模拟冲刺标准练三(附解析),共12页。试卷主要包含了5 K-39 Rh-103,7L,5) eq \f 偏低,3≤pH<6等内容,欢迎下载使用。
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
7.科技助力北京2022年冬奥会。雪上项目是冬奥会重要项目之一,下列有关滑雪材料所对应材质的说法错误的是( )
A.滑雪板板心木质材料的主要成分为纤维素,属于天然有机高分子
B.开幕式专用演出服为石墨烯智能发热材料,属于新型无机非金属材料
C.首钢滑雪大跳台的钢结构赛道为铁合金,属于金属材料
D.冬奥会比赛的雪橇为碳纤维材料,属于有机高分子材料
8.下列对应离子方程式书写错误的是( )
A.向BaCl2溶液中通入CO2气体:
Ba2++CO2+H2O===BaCO3↓+2H+
B.向FeCl2溶液中通入Cl2:
2Fe2++Cl2===2Fe3++2Cl-
C.向NaClO溶液中通入过量SO2:
ClO-+SO2+H2O===Cl-+SO eq \\al(\s\up1(2-),\s\d1(4)) +2H+
D.向NH4Al(SO4)2溶液中加入同体积同浓度的Ba(OH)2溶液:2Al3++3SO eq \\al(\s\up1(2-),\s\d1(4)) +3Ba2++6OH-===3BaSO4↓+2Al(OH)3↓
9.中成药莲花清瘟胶囊对于治疗轻型和普通型的新冠肺炎有确切的疗效。其有效成分绿原酸及其水解产物M的结构简式如下图,下列有关说法正确的是( )
A.两种分子中所有原子可能共平面
B.M的分子式为C9H10O4
C.绿原酸和M都能发生加成、取代和加聚反应
D.绿原酸和M最多都能与3mlBr2发生反应
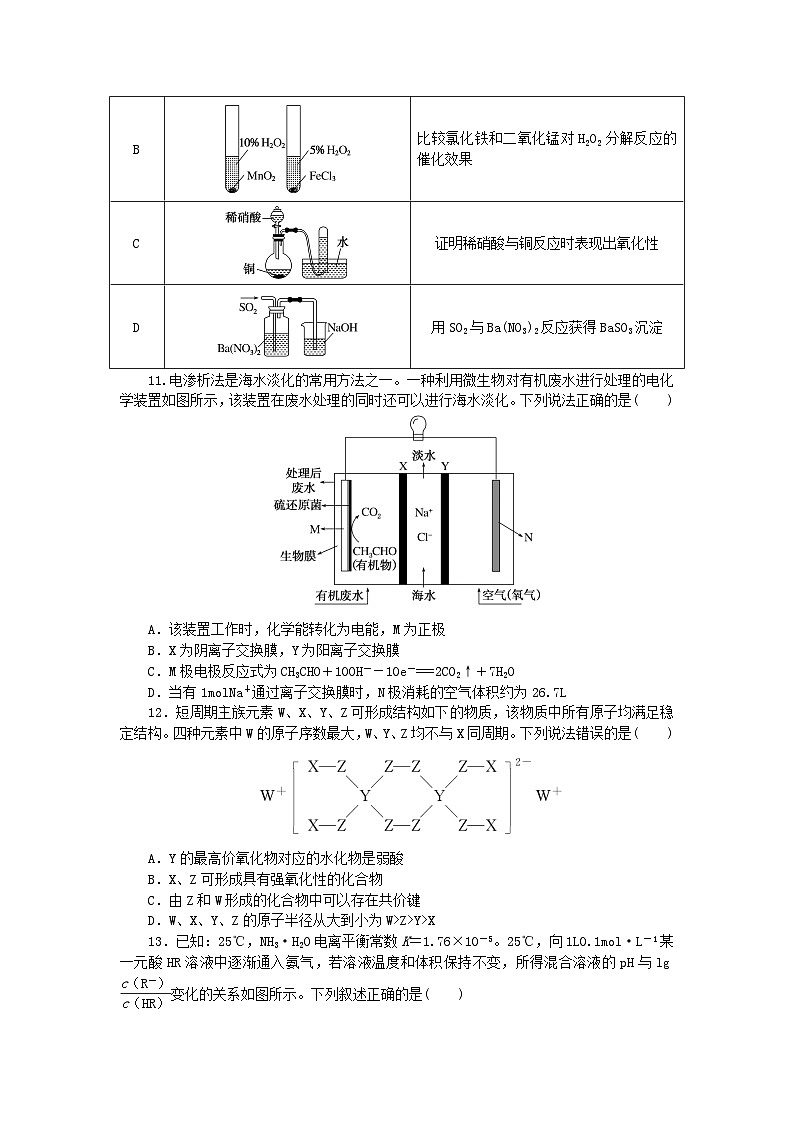
10.下列实验能达到相应目的的是( )
11.电渗析法是海水淡化的常用方法之一。一种利用微生物对有机废水进行处理的电化学装置如图所示,该装置在废水处理的同时还可以进行海水淡化。下列说法正确的是( )
A.该装置工作时,化学能转化为电能,M为正极
B.X为阴离子交换膜,Y为阳离子交换膜
C.M极电极反应式为CH3CHO+10OH--10e-===2CO2↑+7H2O
D.当有1mlNa+通过离子交换膜时,N极消耗的空气体积约为26.7L
12.短周期主族元素W、X、Y、Z可形成结构如下的物质,该物质中所有原子均满足稳定结构。四种元素中W的原子序数最大,W、Y、Z均不与X同周期。下列说法错误的是( )
A.Y的最高价氧化物对应的水化物是弱酸
B.X、Z可形成具有强氧化性的化合物
C.由Z和W形成的化合物中可以存在共价键
D.W、X、Y、Z的原子半径从大到小为W>Z>Y>X
13.已知:25℃,NH3·H2O电离平衡常数K=1.76×10-5。25℃,向1L0.1ml·L-1某一元酸HR溶液中逐渐通入氨气,若溶液温度和体积保持不变,所得混合溶液的pH与lgeq \f(c(R-),c(HR))变化的关系如图所示。下列叙述正确的是( )
A.由图可推知:25℃,0.1ml·L-1NaR溶液的pH约为10
B.当通入0.1mlNH3时,所得溶液中:
c(NH eq \\al(\s\up1(+),\s\d1(4)) )>c(R-)>c(OH-)>c(H+)
C.pH=7时,所得溶液中:
c(HR)>c(R-)=c(NH eq \\al(\s\up1(+),\s\d1(4)) )
D.pH=10时,所得溶液中:c(R-)>c(HR),c(NH eq \\al(\s\up1(+),\s\d1(4)) )>c(NH3·H2O)
二、非选择题:共58分。第26~28题为必考题,每个试题考生都必须作答。第35~36题为选考题,考生根据要求作答。
(一)必考题:共43分。
26.(14分)光卤石是制取钾肥的重要原料,也是提炼金属镁的重要原料。纯净的光卤石的组成可表示为KCl·MgCl2·nH2O。某化学小组为了测定纯净的光卤石的组成,进行如下实验:
实验Ⅰ:用下图所示装置测定纯净的光卤石中结晶水的含量。
(1)装置A的作用是______________________。装置B中的试剂是________。装置D的作用是__________________________________。
(2)实验步骤包括:
①点燃装置C处的酒精灯
②打开装置A处的分液漏斗的活塞
③组装仪器,并检查装置的气密性
④装入药品
⑤关闭装置A处的分液漏斗的活塞
⑥熄灭装置C处的酒精灯
上述实验步骤的先后顺序为______________(填序号)。
(3)写出装置C中硬质玻璃管内发生反应的化学方程式:__________________________________(光卤石用“KCl·MgCl2·nH2O”表示)。
(4)若装置C中硬质玻璃管的质量为ag,实验前称量得硬质玻璃管和样品的总质量为bg,充分反应并冷却后,称量得硬质玻璃管和剩余固体的总质量为cg。则KCl·MgCl2·nH2O中n=________(用含a、b、c的代数式表示)。
实验Ⅱ:测定纯净的光卤石中Mg2+的质量分数。
取wg纯净的光卤石溶于适当过量的稀硝酸中,再用水稀释,配制成250mL溶液。取25.00mL所配制的溶液于锥形瓶中,滴几滴K2CrO4溶液(作指示剂),用cml·L-1AgNO3标准溶液滴定至终点,消耗AgNO3标准溶液VmL。
(5)纯净的光卤石中所含Mg2+的质量分数为________%(用含w、c、V的代数式表示)。
(6)若滴定开始时仰视读数,滴定终点时俯视读数,则测得的结果会________(填“偏高”“偏低”或“无影响”)。
27.(14分)铬及其化合物有许多独特的性质和用途。如炼钢时加入一定量的铬可得到不锈钢,K2Cr2O7是实验中常用的强氧化剂之一,利用含有铬、锌、铁、镉(Cd)、钴(C)等单质的工业废料回收铬的生产流程如图:
几种金属离子生成氢氧化物沉淀的pH见表:
请回答下列问题:
(1)写出提高酸浸速率的措施__________________________________(写出两点)。
(2)酸浸时形成的金属离子的价态均相同,料渣中含有大量的CAs合金,写出除钴时反应的离子方程式________________________________;若仅从试剂的经济角度考虑,试剂X最好是________;氧化过程中铁、铬形成的离子均被氧化,则调pH时应将pH控制在________范围内,单质铬与试剂Y反应时,反应中二者消耗量n(Cr)∶n(Y)=________。
(3)设计实验检验废液中是否含有Fe3+:______________________________________________。
(4)已知常温下Ksp(CdCO3)=5.2×10-12,Ksp(CdS)=3.6×10-29。试剂Z是________(填“Na2CO3”或“Na2S”)时,Cd2+的去除效果较好。若用Na2S溶液处理CdCO3后,达到沉淀溶解平衡时溶液中c(S2-)=aml·L-1,则c(CO eq \\al(\s\up1(2-),\s\d1(3)) )=________________。
28.(15分)2021年6月17日神舟十三号载人飞船与空间站成功对接,航天员进入天和核心舱。空间站处理CO2的一种重要方法是CO2的收集、浓缩与还原。
(1)H2还原CO2制CH4的部分反应如下:
①CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41kJ·ml-1
②CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ·ml-1
③CO(g)+H2(g)⇌C(s)+H2O(g) ΔH3=-131kJ·ml-1
反应2C(s)+2H2O(g)⇌CH4(g)+CO2(g)的ΔH=________kJ·ml-1。
(2)在催化剂作用下CO2加氢可制得甲醇,该反应历程如图所示(吸附在催化剂表面的物质用*标注,如*CO2表示CO2吸附在催化剂表面;图中*H已省略)。
上述合成甲醇的反应速率较慢,该反应过程中决定反应速率的步骤是____________________________________(用化学方程式表示)。
(3)在一定条件下,向某0.5L恒容密闭容器中充入xmlCO2和ymlH2,发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-50kJ·ml-1。
①图1中能表示该反应的平衡常数K与温度T之间的变化关系的是曲线________(填“m”或“n”),判断依据是______________________________________________________________。
②若x=2、y=3,测得在相同时间内,不同温度下H2的转化率如图2所示,v(a)逆________v(c)逆(填“>”“”或“AlO eq \\al(\s\up1(-),\s\d1(2)) >NH3·H2O>Al(OH)3,向NH4Al(SO4)2溶液中加入同浓度的Ba(OH)2溶液,先生成氢氧化铝,再生成NH3·H2O,再生成AlO eq \\al(\s\up1(-),\s\d1(2)) ,当n(OH-)∶n(Al3+)
相关试卷
这是一份统考版2024届高考化学二轮专项分层特训卷仿真模拟冲刺标准练二(附解析),共12页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份统考版2024届高考化学二轮专项分层特训卷仿真模拟冲刺标准练一(附解析),共11页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份统考版2024届高考化学二轮专项分层特训卷仿真模拟冲刺标准练四(附解析),共11页。试卷主要包含了5 Fe-56 Cu-63等内容,欢迎下载使用。








